4. Cellules et
fonctionnement intégré de l'être vivant
(en travaux 2005)
retour partie précédente du cours de
1èreS, plan du cours,
accueil
Remarques
sur cette partie (reportées en fin de page)
Plan de cette page:
TP-TD : Les
systèmes de communication de
l'organisme
4.1 Le système nerveux a pour
fonction principale l'adaptation rapide de l'organisme au milieu
Le TP-TD précédent nous a permis de
comprendre les grandes lignes de l'organisation du système
nerveux dont la mise en place embryonnaire, pour passionnante qu'elle
soit, est hors programme. Le système nerveux est un
système homogène dont
l'homogénéité provient avant tout d'une
origine embryonnaire unique (tube nerveux et vésicules
céphaliques ectodermiques des
vertébrés).
Qu'est-ce que le système nerveux ?
Un ensemble de cellules.
On peut ainsi dire que c'est avant tout un système,
c'est-à-dire un ensemble de cellules regroupées en
tissus et organes et assurant une même fonction (ou
un même ensemble de fonctions) participant au
travail de relation.
En tant que système issu du feuillet embryonnaire le plus
externe (ectoderme) et reliant les cellules et les organes
(voir
TP-TD), le système nerveux
est le système de coordination tourné vers
l'extérieur, le système d'accès à la
vie sensitive, à la communication avec le milieu
extérieur, à l'adaptation au milieu, au
déplacement rapide...Le rôle dans la fonction de
nutrition (au cours de l'effort) que nous avons vu en classe de
seconde entre bien dans ce cadre: les tonus
cardioaccélérateurs et modérateurs cardiaques
permettent une adaptation du rythme cardiaque à la demande des
organes au travail (voir cours
de seconde). De
façon imagée, en ayant à l'esprit la formation
de la gouttière neurale, peut-être pourrait-on dire, que
le système nerveux est le résultat d'une
infinité d'invaginations de la limite
milieu-extérieur-milieu intérieur jusqu'au niveau des
organes les plus internes. Une sorte de réseau
trachéolaire qui serait enfermé (car les parties les
plus denses du système, les centres, sont bien
internalisées) dans l'organisme et qui nous relierait au
monde. C'est l'image du monde extérieur en nous. (De la
même manière, l'appareil digestif, qui nous permet de
consommer nos proies, étant donné notre
allotrophie,
est aussi le résultat d'une internalisation lors de la
gastrulation embryonnaire). D'une façon plus classique,
on peut dire que :
|
le système nerveux a
pour fonction principale l'adaptation rapide de l'organisme
au milieu
|
1ère
partie - Un réseau de neurones
Cette partie ne présente
qu'une illustration de notions scolaires classiques sans
l'indispensable remise en cause remise à plus
tard.
4.11 Un réflexe myotatique est la contraction involontaire
d'un muscle squelettique en réponse à son
étirement
a - les éléments d'un réflexe
Un récepteur qui reçoit un signal,
réalise la transduction et transmet un message
sensitif. Une voie centripète (sensitive) qui
transmet le message sensitif à un centre
intégrateur. Le centre somme (intègre) les
données sensitives et élabore une réponse
réflexe (motrice). Une voie centrifuge (motrice)
transmet le message moteur à un effecteur qui
réalise la réponse.
TP EXAO 1 - enregistrement
d'électromyogrammes du soléaire lors du
réflexe myotatique achilléen (stimulation du tendon
d'Achille et contraction réflexe du muscle extenseur du pied
ou soléaire) (Bordas p 178-179); électromyogramme du
soléaire après stimulation du tendon d'Achille avec
contraction simultanée du muscle antagoniste (jambier
antérieur); électromyogrammes simultanés du
jambier antérieur et du soléaire lors de
légères flexions et extensions volontaires du pied.
(Bordas p 186)
b - un réflexe myotatique
Un réflexe myotatique est la contraction d'un muscle en
réponse à son étirement. Celui qui a
été étudié en TP est le réflexe
achilléen (Bordas p 178). Schéma
général du réflexe (doc B4 p 185). C'est un
réflexe monosynaptique puisqu'il y a une seule synapse au
niveau de la corne ventrale de la moelle épinière.
C'est un réflexe très rapide puisque le délai
synaptique (temps de transfert du message nerveux au niveau d'une
synapse est de l'ordre de 0,5 ms. La vitesse de
conduction du message nerveux dans les fibres sensitives et motrices
est de l'ordre de quelques mètres à quelques dizaines
de mètres par seconde (donc si l'on estime le parcours aller
retour talon d'Achille-ME à environ 2m cela fait un temps
d'environ 0,1 s à 20 m.s-1).
Pour une page de connaissances plus précise
voir les
réflexes myotatiques.
4. 12 Le récepteur élabore le message sensitif
a - un récepteur à l'étirement
Les fuseaux neuro-musculaires sont des récepteurs
à l'étirement (mécanorécepteur)
stimulés lors des réflexes myotatiques (TP et Bordas p
184).
C'est au sein du récepteur que le signal mécanique
(étirement des fibres musculaires modifiées) est
transformé (transduction) en signal électrique (une
dépolarisation d'amplitude plus ou moins grande du dendrite de
la cellule sensitive ganglionnaire).
b - le signal nerveux est une somme de potentiels d'action
(PA)
TP EXAO 2 - Enregistrement d'un
signal nerveux propagé le long du nerf de la patte de crabe
stimulée électriquement - Variation d'amplitude avec
des stimulations d'intensité croissante (Bordas p
196-199)
b1- un PA obéit à la loi du tout ou
rien
Les cellules excitables sont des cellules
polarisées c'est-à-dire qui présentent
un potentiel de repos (PR). Lors d'une stimulation
elle présentent une brusque variation de leur potentiel de
membrane qui est le potentiel d'action (PA). Les PA sont
propagés sans atténuation à la surface des
membranes des cellules excitables.
Schéma PA et Exercice
Bordas n°1 p 214
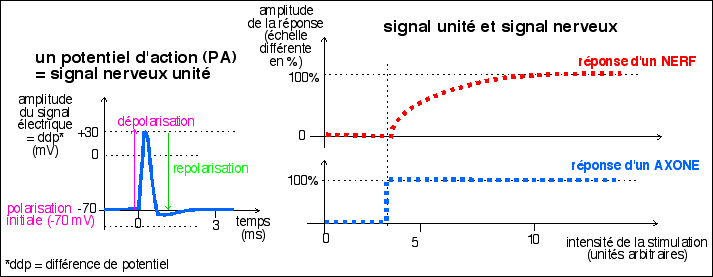
La réponse d'un axone, prolongement d'un neurone (voir TP)
obéit à la loi du tout ou rien: à partir d'un
certain seuil l'axone présente un signal d'amplitude
identique quelque soit l'intensité de la stimulation: ce
signal est le signal unité ou potentiel d'action (PA). Par
contre, le nerf, composé de très nombreux axones (et
d'autres cellules, non excitables, voir TP) a une réponse
proportionnelle à l'intensité de la stimulation; la
réponse se fait aussi à partir d'un certain seuil
(premières fibres stimulées qui répondent) et
elle atteint un maximum lorsque toutes les fibres du nerf sont
stimulées et répondent (l'analogie avec un fil de
téléphone composé de plusieurs fils est assez
éclairante).
b2 - les nerfs propagent un signal (influx nerveux) qui
résulte de la somme des signaux élémentaires
(PA) propagés par chacune des fibres qui les
composent
Le terme de PA du nerf est à proscrire.
Il est de loin préférable de désigner par ce
nom le seul signal élémentaire d'une fibre
isolée.
Des vitesses de conduction croissantes sont observées selon
le diamètre de la fibre et sa myélinisation (petits
axones nus < petits axones myélinisés < gros
axones nus < gros axones myélinisés) depuis un
vitesse faible de l'ordre de 0,2 m.s-1 à une
vitesse rapide de l'ordre de 120 m.s-1.
b3 - les PA sont propagés le long des membranes des
cellules excitables
Exercice Bordas n°2 p 215 Mesure de vitesse
c - le message sensitif est codé en modulation de
fréquence
Exercice Bordas n°3 p 215
4. 13 Les centres intègrent les messages sensitifs et
élaborent des messages moteurs
a - la moelle épinière : un centre qui traite
très rapidement des messages sensitifs simples
a1 - un réflexe myotatique est un
réflexe monosynaptique
a2 - le fonctionnement coordonné des muscles d'un
membre fait intervenir l'innervation réciproque des muscles
antagonistes
schéma de synthèse à apprendre Bordas p
187 ou 191
Exercice Bordas n°2 p 193
|
Un "exercice" autour d'un modèle
simplissime
|
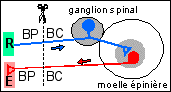
Les expériences historiques de
section-stimulation de nerfs permettant d'une
façon fruste de déterminer la nature
sensitive ou motrice d'un nerf
dans le cadre d'un schéma
réflexe simple quasi-théorique
(récepteur (R) - nerf sensitif - centre - nerf
moteur - effecteur (E)). Il faut impérativement
que le nerf ne comporte qu'un seul type de fibres
(motrices ou sensitives) et qu'elles soient
reliées au même organe (ce qui n'est pas
généralement le cas, les nerfs comportant
de nombreuses fibres issues d'organes différents;
plus rarement des fibres sensitives avoisinant des fibres
motrices). La propagation du message nerveux est à
sens unique, du fait des synapses qui ne transmettent
l'information que dans un seul sens (voir chapitre
suivant). Le bout central (BC) d'un nerf
est en liaison avec le centre (en gris) et le bout
périphérique (BP) avec un
récepteur (pour un nerf sensitif) ou un effecteur
(pour un nerf moteur).
|
|
On peut déduire deux composantes du message
nerveux par ces expériences:
- si lors de la section d'un nerf, on observe une
modification de l'activité d'un effecteur,
c'est donc qu'il existait en permanence un message qui
transitait par celui-ci. Pour un nerf moteur on parle
de TONUS. Pour un nerf sensitif on parle
d'activité permanente du
récepteur.
- si l'on stimule le BP d'un nerf
sensitif sectionné, on
en doit pas observer de réponse (puisque que
l'on a pris comme hypothèse que ce nerf
était issu d'un récepteur). De la
même façon si l'on stimule le BC d'un
nerf moteur sectionné,
il ne doit pas y avoir de réponse puisque le
message nerveux ne peut pas aller dans le sens
moteur->sensitif du fait de la synapse
sensitivo-motrice.
- si l'on stimule le BC d'un nerf
sensitif sectionné,
comme le BP d'un nerf moteur
sectionné, on doit obtenir une
réponse de l'effecteur en liaison avec ce
nerf.
|
b - le cortex sensitif et le cortex moteur sont des centres
supérieurs qui reçoivent d'innombrables informations
sensitives et élaborent des réponses complexes
Une structure motrice est définie
par une réponse musculaire à une stimulation
directe (électrique principalement) et/ou l'apparition
de troubles du mouvement suite à son ablation. En toute
rigueur seules les structures génératrices de
mouvements de la musculature striée (motricité
somatique) doivent être qualifiées de motrices. Les
structures impliquées dans les mouvements des muscles lisses
peuvent être rapportées à une motricité
viscérale qui reste peu importante étant donné
que l'on considère que le
système nerveux végétatif fonctionne d'une
façon autonome, par voie réflexe (cœur, muscles
assurant les mouvements respiratoires ou
péristaltiques...).
Une structure sensitive est
définie par la réception de signaux à la
suite d'une stimulation de récepteurs
périphériques mais surtout par la perte de
sensibilité à la suite d'une
lésion-ablation.
Un signal n'est signifiant que s'il est reçu et
interprété. La réception est du domaine de la
sensation. L'interprétation du domaine de la
perception. La sensibilité d'un organisme dépend
donc des récepteurs qu'il possède. Les
récepteurs spécifiques spécialisés
mais surtout localisés chez l'homme déterminent
des sens assez bien définis: la vue, l'ouïe,
l'équilibration (kinesthésie
inconsciente voir plus bas), l'odorat, le goût.
Les autres sensations, moins bien localisées, et ne
correspondant pas toujours à des récepteurs connus,
sont qualifiés de somesthésiques. Elles
comprennent le sens tactile au sens large qui recouvre aussi
la thermosensibilité et la sensibilité
à la douleur (nociceptive) (pour laquelle
il n'a pas encore été trouvé de
récepteurs spécifiques mais qui semble être une
chémoréception) ainsi que la
kinesthésie (=cinesthésie) consciente
(sensibilité aux mouvements des
différentes parties de son corps).
La somesthésie dite "générale"
désigne donc l'ensemble des sensations venant de la peau, des
muscles, des articulations et des viscères.
Juste une remarque pour montrer la finesse de la
sensibilité tactile: la pulpe des doigts peut distinguer au
repos deux reliefs séparés de 2,5 mm; mais si le doigt
se déplace une simple différence de rugosité
peut être reconnue ce qui permet à des aveugles de lire
l'écriture Braille à près de 600 lettres par
minute, ce qui est plus rapide qu'une lecture à
vue.
L'encéphale correspond très
grossièrement à deux cylindres creux accolés.
Chez les Poissons et les Amphibiens il ne reçoit que peu
d'afférences sensitives (essentiellement olfactives; les
autres se terminant dans des centres inférieures
médullaires ou bulbaires) mais possède
déjà un rôle moteur incontestable. Chez les
Reptiles, Oiseaux et Mammifères, les relations entre les
récepteurs périphériques et les
hémisphères cérébraux se font de plus en
plus étroites. La partie la plus en avant
(télencéphale) se différencie en une
masse ventrale constituée des noyaux de la base et une
couche de plus en plus épaisse de cellules nerveuses qui
donnera le cortex, d'autant plus épais et riche en
cellules et en prolongements cellulaires que l'on est chez des
vertébrés au comportement complexe. Chez l'homme, le
cortex recouvre la totalité des deux
hémisphères. Les cellules nerveuses du cortex sont
organisées en six couches. Chez les
Mammifères on a pus observer que la densité de neurones
est d'autant plus faible que l'animal est de grande taille; ce qui
est à mettre en relation, non pas avec une diminution du
nombre de neurones mais avec l'augmentation du nombre de cellules
gliales, très marquée chez les animaux de grande
taille. Les zones du cortex en liaison avec les
récepteurs périphériques sont regroupés
en volumes occupant toute l'épaisseur corticale et coupant la
surface du cortex selon des aires assez bien
délimitées. L'ensemble des aires corticales, et
spécialement celles qui sont liées à la vision,
à la somesthésie et à la motricité,
s'organisent en une sorte de mosaïque formée de
colonnes juxtaposées orthogonales à la surface
du cortex.
Nathan p 226-227? Bordas p 220-225
On désigne par somatotopie (du grec "soma" = corps
et "topos" = lieu) la relation "topologique" c'est-à-dire dans
l'espace entre une structure périphérique du corps et
une structure corticale. Il existe une incontestable somatotopie au
niveau du cortex somatosensoriel qui reçoit les informations
tactiles: les zones sensibles du corps reportées sur le cortex
dessinant la forme du corps ("l'homoncule" ou homunculus en latin)
avec des proportions caractéristiques de l'importance relative
des différentes surfaces corporelles: la tête et les
mains étant maximales.
4.14 Le comportement de l'organisme résulte de
l'activité intégrée du système
nerveux
a - Les corps cellulaires des motoneurones médullaires
intègrent (somment) les afférences sensitives
excitatrices et/ou inhibitrices et les afférences centrales
volontaires
TP EXAO 1 et Bordas B3 p 209
Lors d'une commande de contraction volontaire le cerveau transmet aux
motoneurones stimulés un message excitateur. Si une
stimulation d'intensité efficace est portée sur le
tendon d'Achille, alors que le muscle antagoniste (jambier
antérieur) est contracté volontairement, le
réflexe myotatique est inhibé. Les
afférences centrales volontaires sont donc à la fois
excitatrices sur le motoneurone commandant le jambier
antérieur mais aussi inhibitrices sur le motoneurone
commandant le muscle antagoniste. Ainsi le corps cellulaire du
motoneurone commandant la contraction du soléaire a
reçu simultanément une afférence inhibitrice
centrale volontaire et une afférence sensitive réflexe
excitatrice. La résultante a été une inhibition
du réflexe.
b - Chaque synapse chimique transmet un message soit excitateur
soit inhibiteur à la cellule postsynaptique selon le type de
neurotransmetteur qu'elle libère dans la fente
synaptique
La transmission synaptique chimique est orientée: il
y a une dissymétrie entre les deux zones synaptiques. Dans une
synapse chimique le message nerveux, électrique, est
transmis chimiquement d'une zone synaptique à
l'autre.
Une synapse fait intervenir au moins 3 cellules:
* une cellule présynaptique, qui est toujours un neurone dont
une zone axonale ou dendritique (plus rarement) présynaptique
se renfle;
* une cellule postsynaptique, qui peut être un neurone, une
cellule musculaire ou une cellule glandulaire
* une ou des cellules gliales.
Une synapse comprend 3 parties:
* la zone présynaptique dont l'axoplasme renferme des
vésicules synaptiques dans lequel est stocké le
(ou les) neurotransmetteur(s) spécifique(s) de la synapse
(on y trouve également des mitochondries, de
nombreux microtubules et des vésicules denses qui se
différencient des vésicules synaptiques, petites de
claires); la membrane présynaptique, au point d'exocytose des
vésicules synaptiques, est souvent plus épaisse et plus
sombre au MET;
* la fente synaptique ou espace intersynaptique
(occupé dans le cas de la synapse
neuromusculaire par une membrane basale plus ou moins colorée
et visible au microscope électronique à
transmission);
* la zone postsynaptique dont le contenu cytoplasmique
dépend fortement du type cellulaire de la cellule
postsynaptique; habituellement la membrane
postsynaptique présente un épaississement encore plus
net que la membrane présynaptique, visible au MET; du
point de vue fonctionnel cette membrane contient les
récepteurs au neurotransmetteur.
Lors de l'arrivée d'un PA au niveau de la zone
présynaptique, le neurotransmetteur est libéré
dans la fente synaptique par exocytose des vésicules
synaptiques. Le neurotransmetteur se fixe sur les récepteurs
de la membrane postsynaptique et est simultanément
inactivé ou dégradé par voie enzymatique dans la
fente synaptique et/ou capturé par la cellule
présynaptique et/ou par les cellules gliales. Ainsi la synapse
peut de nouveau est activée après un temps très
bref typiquement de l'ordre du dixième de milliseconde. La
fixation du neurotransmetteur à la membrane de la cellule
postsynaptique modifie son activité.
La fixation d'un neurotransmetteur inhibiteur sur les
récepteurs de la membrane d'un neurone provoque une
hyperpolarisation qui empêche l'apparition d'un PA qui
constituerait un message postsynaptique qui pourrait être
propagé. A l'inverse, la fixation d'un neurotransmetteur
excitateur sur les récepteurs de la membrane d'un neurone
provoque une dépolarisation qui, si elle atteint le seuil
d'excitation du neurone, peut provoquer l'apparition d'un PA
postsynaptique qui est alors transmis par l'axone.
Dans le cas de la jonction neuromusculaire, un PA
présynaptique est toujours suivi d'un PA postsynaptique.
c - Dans les centres supérieurs les corps cellulaires
des neurones reçoivent de très nombreuses
afférences excitatrices et inhibitrices dont ils font la somme
spatiale (sur toutes les synapses) et temporelle (sur une
période de temps donnée)
À la suite de la libération simultanée des
neurotransmetteurs des nombreuses synapses excitatrices et
inhibitrices dans les fentes synaptiques entourant le corps
cellulaire d'un neurone central, ce dernier élabore un message
efférent qui résulterait de la somme spatiale et
temporelle des messages synaptiques inhibiteurs et excitateurs.
2ème
partie - Des cellules nerveuses vivantes formant un système en
permanente évolution
2.1 La vie sensitive (partie culturelle)
La physiologie est non seulement explicative (au
sens de détailler, donc descriptive) mais
compréhensive (au sens étymologique de
"prendre avec soi", d'assimiler par son intelligence), dans la mesure
où elle recherche la signification (signe visible du sens
profond) de tel ou tel mécanisme; ce que Knut Schmidt-Nielson
appelle les questions du pourquoi et du comment. Dans l'introduction
de Physiologie animale ; adaptation et milieux de vie (1998,
Dunod) il écrit: «en étudiant l'adaptation de
l'animal a son milieu on est conduit à voir ce qui est bon
pour lui... L'animal doit se maintenir en vie et il n'y a rien
d'inconvenant, ni de non scientifique, à découvrir
comment et pourquoi il y réussit».
La neurophysiologie progresse, comme toujours, de concert avec
l'évolution des techniques: d'une part la biophysique
qui permet de mesurer des activités électriques
très faibles, très rapides et très nombreuses et
de stimuler de plus en plus précisément des structures
cachées au plus profond des hémisphères
cérébraux; et d'autre part la biochimie, devenue
neurochimie, qui explore non seulement les neurotransmetteurs
synaptiques mais s'intéresse aux médiateurs,
récepteurs, enzymes et autres molécules dont la
neuropharmacologie étudie à son tour les applications
thérapeutiques. On peut dire que du point de vues des
données expérimentales les progrès ont
été considérables.
Mais en ce qui concerne la théorie un tel progrès est
plus difficilement soutenable.
- Sans faire une histoire des sciences qui sort de mon champ de
compétence (mais que j'appelle de tous me
vœux), on peut probablement considérer qu'il y
a deux étapes principales préparatoires à
l'étape actuelle, foisonnante comme toujours.
- Une étape que l'on pourrait résumer par
la vie sensitive comme réponse aux stimuli de
l'environnement. La compréhension de toute
activité comportementale mettant en jeu le
système nerveux était une
généralisation de ce qui avait été
historiquement mis en évidence au sujet des
réflexes médullaires: toute activité
résultait d'un stimulus déclenchant
associé à la notion de besoin physique ou
intellectuel (nourriture, boisson, connaissance, sexe...).
Cette étape peut trouver un repère historique
dans ce que certains appellent "la plus retentissante des
anciennes découvertes" par laquelle François
Magendie (1822) attribua aux racines dorsales des nerfs
rachidiens la fonction de conduire les messages de la
sensibilité et aux racines ventrales celle de conduire
ceux de la motricité.
- Une seconde étape que l'on pourrait aussi
résumer par la vie sensitive comme programme
déterminé de comportements sensibles.
L'activité d'un organisme résulterait d'abord
d'un programme central organisateur qui définit une
séquence déterminée d'étapes;
lors de l'action, les informations sensitives servent à
adapter, plus ou moins selon les types de mouvement, l'action
à l'environnement. Cette conception est
formalisée à l'aide d'outils issus de la
théorie des systèmes (servomécanisme,
boucles ouvertes, rétroactions, comparateurs
d'erreurs...). Cette théorie implique de rechercher le
lieu de la mémoire des comportements programmés.
Pour certains, cette mémoire repose sur le
"câblage neuronal", qui serait déterminé
génétiquement.
|
La
biocybernétique
|
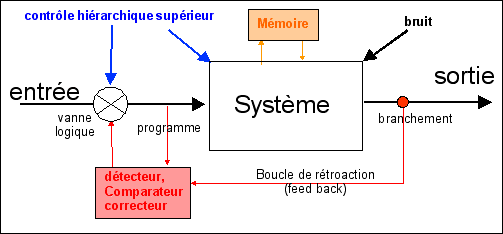
Un système formalisé à l'aide des
outils de la cybernétique
(d'après
EU)
|
La cybernétique désigne la science
des interactions entre les mécanismes; elle a
été développée depuis le
milieu du XXème siècle dans des
systèmes artificiels et naturels. Mais son
vocabulaire et ses concepts viennent bien de la
physique des systèmes artificiels. Plus
concrètement, appliquée à la
biologie, on pourrait dire que la
biocybernétique est la science des
échanges d'information (informations
entrantes et informations sortantes ou commandes ou
encore contrôles) entre systèmes vivants
ou composants de ces systèmes (à toutes
les échelles: du moléculaire au
social).
|
- L'étape actuelle voit poindre de vrais
paradigmes novateurs qui, bien évidemment, intègrent
les anciens. Un exemple qui me paraît être riche en
promesses est celui développé par René Thom
depuis les années 1960 et surtout par ceux qui utilisent
son outil qualifié par Zeeman de "théorie des
catastrophes" et repris depuis par ce que l'on pourrait appeler
une "école française de morphodynamique" dont Jean
Petitot est un des membres.
Quelques mots de René Thom dans Paraboles et
catastrophes (1983, Flammarion, col. Champs)
«… en biologie ce sont les structures
mathématiques qui ordonneront les phénomènes
les plus importants. Par exemple, les
phénomènes de régulation exigent
un grand nombre de paramètres et, par conséquent,
toute description un peu affinée de ces
phénomènes nécessitera l'utilisation
d'espaces pluridimensionnels. croire que l'on pourra donner une
théorie de la régulation tout simplement en
manipulant des diagrammes cybernétiques avec des sommets et
des flèches est illusoire, selon moi. L'importance de la
régulation consistera toujours dans le fait qu'il
s'agit d'un phénomène à caractère
fondamentalement continu ; il faudra donc associer des
figures multidimensionnelles à ces situations. Dans ce cas
la théorie des catastrophes pourra
être très utile justement parce qu'elle vise
à interpréter des nuages de points recueillis
expérimentalement, au moyen de constructions
mathématiques qui seraient à la fois les plus
simples et les plus robustes et, ainsi, qui satisferaient la
propriété de stabilité structurelle tout en
résistant à de petites perturbations dues au milieu
ou aux erreurs expérimentales. Toute la philosophie de
la théorie des catastrophes , son schéma
général, tient justement à ceci: il s'agit
d'une théorie herméneutique qui s'efforce,
face à n'importe quelle donnée expérimentale,
de construire l'objet mathématique le plus simple qui
puisse l'engendrer.» (...)
« Sur l'anatomie du cerveau et sur la physiologie du
neurone on a acquis d'énormes connaissances et pourtant
cela n'a pas beaucoup servi pour comprendre le fonctionnement du
cerveau. On ne parvient même pas à comprendre
très bien l'origine, pour ainsi dire, des variations
électriques de l'encéphalogramme : ce dernier
apparaît comme une espèce de phénomène
surimposé dont la signification est mal comprise. En ce
sens, la situation est typique : il ne suffit pas de savoir
comment est fait un système pour comprendre comment il
fonctionne surtout quand les éléments ont une
structure interne plutôt compliquée. (...) il faut
donc avoir recours à une théorie continuiste
».
Pour expliciter ce que renferme cette notion de théorie
continuiste, je voudrais signaler combien il est frappant de voir
le terme d'homéostase (du latin
"homœo" ? et du grec "homolos" = "semblable",
et du latin "statio" = immobilité, mais aussi
école publique et assemblée) employé par R.
Thom notamment mais aussi par les spécialistes des sciences
cognitives, dans le sens de maintien de la forme,
aussi bien corporelle que psychique. L'utilisation habituelle
de ce terme en physiologie étant associé à
une image de l'organisme comme système réglé
dont certains paramètres sont maintenus constants.
Une théorie continuiste de la vie sensitive pourrait
être de définir la relation de l'individu au milieu
comme une forme maintenue constante par des processus
d'homéostase qui lierait activité physiologique et
psychique. Forme issue de l'intégrité cellulaire
d'abord et des mots comme architecture corticale, somatotopie et
autres expressions contenant l'idée d'une morphologie
trouveraient ici une unité. Mais forme issue aussi des
images et concepts de la pensée. Il s'agit là sans
aucun doute d'une métaphysique que Jean Petitot appelle un
réalisme écologique (voir l'article "forme"
de l'Encyclopedia Universalis et la page sur
les modèles sur ce site ou la page personnelle de Jean
Petitot qui explicite les domaines actuels de recherche
mathématiques et épistémologiques: http://www.crea.polytechnique.fr/JeanPetitot/JPmodeles.html#I.7
).
Enfin, il est nécessaire de souligner que toute
compréhension du système nerveux doit reposer sur
l'évolution. A ce titre l'évolution du
système nerveux des animaux est probablement un des exemples
de phylogenèse les plus éclairants. Origine
embryologique commune, internalisation, différenciation,
complexification progressive, hiérarchisation, sont autant de
traits évolutifs qu'il faut voir non pas par comparaison
d'espèces actuelles bien sûr mais en considérant
les ancêtres dont ils sont issus (pour des
lecteurs avertis vous pouvez consulter par exemple l'article
"neurogénèse" de Paul Laget dans l'Encyclopedia
Universalis).
2.2 La neuroplasticité
La plasticité désigne depuis au moins le
XVIIIème siècle une propriété du solide
déformable et malléable. Elle a un sens très
précis en géologie (voir
page sur
les séismes). En biologie
certains auteurs, à la fin du XXème, ont parlé
de plasticité biologique de l'homme dans le cadre d'une
vision simpliste du vivant : la biologie résultant de
l'expression du patrimoine génétique (qui conduit
à ce qui est comparé à un solide) variant selon
les conditions du milieu (qui modèlent le solide). L'aspect
individuel étant désigné par le terme de
plasticité (les jumeaux étant l'exemple
type montrant les limites de cette plasticité), et l'aspect
collectif et évolutif étant désigné sous
le terme d'adaptation. Il est à craindre que la
neuroplasticité proposée dans le programme
dérive de cette vision bornée qu'il faut absolument
dépasser.
L'être vivant est un système dynamique,
une société de cellules VIVANTES, en
perpétuel remaniement.
Depuis Aristote, la partie stable de
l'individu est sa FORME alors que la partie
changeant est la matière. En biologie, la forme, c'est
l'espèce (du latin
species = la forme visible avec les yeux).
L'approche théorique de la forme est remise
à la classe de terminale dans le chapitre sur les
classifications et l'évolution. Il ne s'agit pas ici de
traiter de ses variations mais uniquement de s'intéresser
à l'évolution du système nerveux après sa
mise en place embryonnaire.
Nous nous bornerons à étudier quelques exemples de
plasticité à différents niveaux.
La plasticité
cérébrale désigne la capacité du
cerveau à modifier sa structure ou son fonctionnement
après sa mise en place au cours de
l'embryogenèse. On considère qu'elle diminue
avec l'âge du sujet. Elle a d'abord été admise
comme un élément essentiel des zones affectées
à la mémoire mais absent des autres zones
cérébrales. Depuis les années 1990 on a
suspecté puis mis en évidence que cette
plasticité touchait aussi le cortex sensitif et même
moteur.
Des expériences mettant en évidence la
plasticité cérébrale à partir d'imagerie
fonctionnelle cérébrale réalisées chez
:
* des violonistes (Une empreinte dans le cortex des violonistes: une
étonnante plasticité jusqu'aux confins du pathologique,
Thomas Elbert, Brigitte Rockstroh, La Recherche, Juillet-août
1996, 289, p 86-89)
* ou des personnes atteintes de surdité (L'extension des aires
visuelles chez les sourds, Helen Neville et Daphne Bavelier, La
Recherche, Juillet-août 1996, 289, p 90-93).
On pourrait dire en conclusion qu'au niveau
du cortex, la neuroplasticité est une modification de
l'organisation dynamique se traduisant par un remodelage des
connexions synaptiques à la suite de modifications de
l'activité sensitive et/ou motrice
périphérique.
On peut distinguer :
* une plasticité structurale qui résulterait de
changements au niveau cellulaire: dans le nombre de cellules :
divisions de cellules avec (dédifférenciation) ou sans
(cellules souches) différenciation,
dégénérescences; ou dans les connexions entre
cellules : augmentation ou diminution du nombre de dendrites et/ou de
synapses...
* et une plasticité fonctionnelle : une cellule
différenciée qui change de fonction sans modification
structurale profonde (et donc dédifférenciation) est
difficilement envisageable mais il peut y avoir une modification de
la nature des neurotransmetteurs et, d'une façon plus complexe
à représenter, une réorganisation des aires
corticales par exemple...
On notera qu'il est difficile d'envisager des changements uniquement
fonctionnels ou uniquement structuraux.
a - une plasticité fonctionnelle neurochimique des
neurones adrénergiques et catécholaminergiques
Un cas typique est représenté par les changements
de métabolisme des neurones en culture (donc in
vitro) et lors de greffes (in
vivo):
les neurones sympathiques (voir page sur le
système nerveux
végétatif) en culture
sont noradrénergiques (libèrent de la
Noradrénaline) s'ils sont cultivés seuls mais
deviennent cholinergiques (libèrent de
l'Acétylcholine) s'ils sont cultivés avec d'autres
types cellulaires comme des fibres myocardiques.
C'est une plasticité fonctionnelle
neurochimique.
Des expériences de chirurgie nerveuse réparatrice ont
alors été menées. Ainsi des greffes de cellules
catécholamininergiques de la médullo-surrénale
(et du mésencéphale d'un fœtus humain) ont
été réalisée dans le striatum de malades
atteints de maladie de Parkinson. Les résultats ont
été encourageants puisque les greffons n'ont pas
été rejetés et que les tissus greffés ont
adoptés le profil neurochimique des tissus au sein desquels
ils avaient été greffés.
Avec le formalisme adopté dans ces pages (voir
le chapitre 2 du
cours de 1èreS et surtout le
schéma de
synthèse) il est clair que
cette plasticité nécessite une modification des trois
types d'informations (génétique, cytoplasmique et
environnementale). Plutôt que de dire que de nouveaux
gènes doivent être exprimés il serait plus juste
de dire que le niveau d'expression des différents gènes
change. Le changement de neurotransmetteur, qui ne sont pas des
protéines, implique des changements dans la synthèse ou
l'activité de plusieurs enzymes et surtout de cofacteurs
intervenant dans de nombreuses autres réactions. Mais ce n'est
pas parce qu'une molécule est utilisée quelque part
dans la cellule qu'elle va pouvoir obligatoirement être
utilisée autre part: il ne faut pas oublier que la plupart des
cofacteurs et enzymes qui sont de grosses molécules doivent
être transportés entre le lieu de leur
synthèse et leur lieu d'activité
(voir page
sur la cellule). La
plasticité du métabolisme repose plus sur la
présence simultanée dans un neurone de plusieurs
métabolismes. La plasticité exprime alors un simple
changement de niveau d'expression de certains gènes sans qu'il
soit nécessaire d'imaginer que la cellule "deréprime"
des gènes.
Certains neurophysiologistes préfèrent parler de
neuroplasticité transcriptionnelle.
|
Compléments sur l'Adrénaline et
l'Acétylcholine
|
|
Le métabolisme des monoamines (hydrosoluble)
issues de l'acide aminé tyrosine est un
métabolisme qui ne conduit pas uniquement à la
Noradrénaline. La tyrosine est un des produit
du catabolisme de la phénylalanine, qui peut
être déficient dans certaines formes de
phénylcétonurie (voir cours
de 1èreS et page sur la phénylcétonurie).
Les catécholamines sont
l'adrénaline (épinéphrine), la
noradrénaline (norépinéphrine) et la
dopamine; elles dérivent du catéchol
(1,2-dihydroxybenzène: un cycle benzénique
avec deux OH en position 1 et 2). Le nom Dopa vient du nom
allemand de la 3,4-dioxyphénylalanine. les
catécholamines sont synthétisées dans
certaines cellules nerveuses et dans la
médullosurrénale qui est assimilée
à un ganglion orthosympathique (même origine
embryonnaire et même métabolisme).
|
|
Tyrosine
|
-------->
|
Dopa
|
-------->
|
Dopamine
|
-------->
|
Noradrénaline
|
-------->
|
Adrénaline
|
|
enzymes
|
tyrosine
hydroxylase
|
décarboxylase
des a.a.
aromatiques
|
dopamine
ß-hydroxylase
|
phényléthanolamine
N-méthyltransférase
|
|
cofacteurs,
substrats et produits
associés
|
Tétrahydrobioptérine,
O2 >> H2O,
Dihydrobioptérine
|
PLP >>
CO2
|
Ascorbate, O2
>> H2O,
Déhydroascorbate
|
adoMet >>
adoHcy
|
|
|
L'acétylcholine
H3C-CO-O-CH2-CH2-N+-(CH3)3
est l'ester acétique de la choline
(il peut être préparé
chimiquement par chauffage de la choline avec l'anhydride
acétique mais c'est un produit instable en milieu
alcalin). C'est un tout petit composé (PM =
149). On l'a trouvé dans des plantes, des
micro-organismes et bien sûr certaines neurones
animaux. Dans la cellule elle se trouve liée à
une grosse protéine qui empêche son hydrolyse.
Sa biosynthèse est liée au catabolisme des
glucides produisant l'acétyl-coenzymeA (voir cours de
terminale spécialité).
L'acétylcholinestérase a été
localisée dans de petites vésicules du corps
cellulaire de certains neurones et dans l'espace
intersynaptique des synapses "à ACh". Il y a encore
beaucoup à apprendre sur ses lieux de
synthèse. Je signale par exemple
l'article de Cécile Klingler, La Recherche, 347,
Novembre 2001, 20-21 qui présente les cellules
gliales participant à la recapture et à la
dégradation de l'acétylcholine grâce
à la sécrétion de la protéine de
liaison AChBP (ACh Binding Protein).. chez Lymnæa
stagnalis.
|
choline +
acétyl-CoA +
protéine de liaison
|
thiamine-pyrophosphate
, CoA
|
acétylcholine
(ACh) -
protéine de liaison
|
|
cholineacétylase
|
|
------------------>
|
|
choline + acide
acétique +
protéine de liaison
|
<-------------------
|
|
acétylcholinestérase
(AChE)
|
|
|
|
b - la compensation vestibulaire: une plasticité
cérébrale
Source: Un exemple vécu de
plasticité cérébrale : la compensation
vestibulaire, Pierre Clément,
Biologie-Géologie, n°4-1999, p 731-735.
Chacun de nos deux nerfs vestibulaires contient des axones de
neurones sensitifs (en T) dont le corps cellulaire se trouve au
voisinage des récepteurs de l'oreille interne (utricule,
saccule et ampoules de la base des canaux semi-circulaires; voir
cours général sur les
sens) innervant des neurones situés dans les noyaux
vestibulaires (dans le bulbe rachidien au voisinage du cervelet). A
la suite d'un section accidentelle du nerf vestibulaire, ou d'une
lésion infectieuse (virale ?) qui conduit à une
dégénérescence équivalente, ou encore des
altérations des noyaux vestibulaires on observe une perte
brutale de la perception de la position globale du corps dans
l'espace (associée à des vertiges très violents)
ainsi que des symptômes plus variés comme des
nausées digestives et des mouvements saccadés et
involontaires des yeux (nystagmus). Ces dérèglements
sont dus à des couplages sensoriels entre
l'équilibration et d'autres sensations : d'abord la vision
(détection des mouvements des yeux... par exemple), puis la
proprioception (récepteurs intramusculaires et contrôle
des motoneurones alpha et gamma - voir
page sur les
réflexes myotatiques) et enfin la
somesthésie (récepteurs de la plante des pieds par
exemple nous informant de la nature du substrat...).
La compensation vestibulaire consiste dans la
récupération progressive du sens de l'équilibre,
malgré la lésion parfois définitive. La
disparition des symptômes intervient au bout de 3 à 4
semaines SI LE MALADE S'EFFORCE ACTIVEMENT DE RÉCUPÉRER
CETTE SENSATION. La compensation fait clairement intervenir de
nombreuses zones motrices et sensorielles, même si un
réelle plasticité au niveau des noyaux vestibulaires
est probable. Dans certains cas, et plus tardivement (5 à 6
mois) on peut aussi observer des restaurations fonctionnelles
complètes que l'on teste à l'aide de stimulations
codifiées des récepteurs vestibulaires.
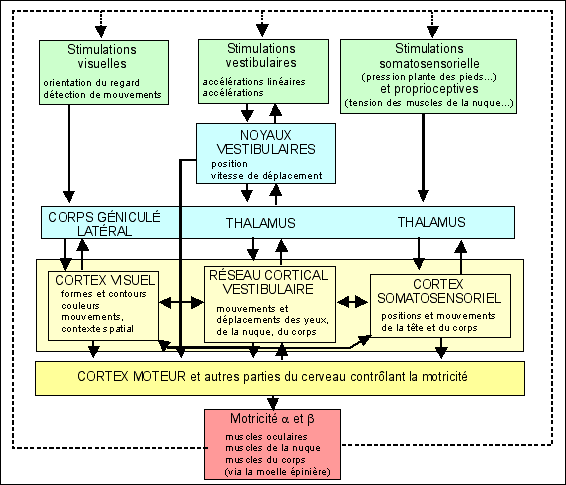
Schéma général très simplifié
de l'équilibration (in Clément,
Biologie-Géologie n°4-1999, p 734)
Dans le corps géniculé latéral,
situé dans le thalamus, les corps cellulaires des neurones
visuels qui envoient leurs axones vers le cortex visuel ne
reçoivent que 20% de leurs afférences de la
rétine (et donc des récepteurs visuels); 80% de leurs
afférences viennent d'autres zones du cerveau. Bien
évidemment les afférences et efférences
représentées, notamment au niveau des noyaux
vestibulaires et du thalamus, sont très partielles.
c - Autres exemples pris dans les manuels scolaires:
- La comparaison des comportements et des structures
cérébrales chez les jumeaux vrais (issus du
même zygote ou jumeaux monozygotes).
Je pense qu'il faut aussi bien se méfier
des ressemblances que des différences. Les
différences de sensibilités à des maladies
neurologiques observées chez des vrais jumeaux fait
ressortir non pas l'indispensable modulation du génotype
par l'environnement mais la modulation du milieu sur l'ensemble du
développement d'un individu. Les jumeaux vrais ont
peut-être le même génotype au niveau du zygote,
ce qui n'est pas évident et ce qui ne veut pas dire grand
chose car on parle bien d'allèles exprimés et non
pas de génome. Mais encore une fois, le génotype,
notion tout au plus cellulaire, n'est pas défini au niveau
de l'organisme entier et le déterminisme
génétique d'une anomalie ne doit pas être
écarté même si le jumeau n'est pas atteint. Il
faut cesser de voir le génotype comme la source d'un
déterminisme unique.
- des expériences réalisées chez le rat
notamment sur la sensibilité tactile par les vibrisses et
ses modulations à la suite d'amputations ou
d'apprentissages: Nathan p 228-229; Bordas p 234 (exercice 1) ou
chez le singe-hibou (Nathan p 238 exercice 5, Bordas p 228)
- l'interprétation de mutants chez la souris; Nathan p
225; Bordas p 226.
- la similitude des réseaux neuroniques entre individus
de même espèce...
Pourquoi deux individus de la même
espèce ou du même groupe de classification (les
réflexes médullaires myotatiques sont par exemple
mis en évidence chez de nombreux vertébrés)
ont-ils une organisation voisine de certains de leurs neurones ?
La réponse faisant intervenir une similitude de
gènes est une pétition de principe. Des
réseaux semblables demandent des tissus semblables, des
cellules semblables, des neuromédiateurs semblables, des
interactions cellulaires semblables au cours du
développement. Ce sont donc bien les mécanismes
généraux du développement et de la
différenciation cellulaire qui sont ici responsables de
cette organisation. L'information génétique n'est
jamais seule à intervenir. Elle est toujours sous le
contrôle de l'information cytoplasmique et environnementale.
Une théorie du développement qui soit aussi
évolutive est bien plus à même
d'éclairer la neurophysiologie comparative qu'une
théorie du programme génétique
dépassée.
- l'existence d'anomalies congénitales
d'insensibilité à la douleur dont une forme est
associée à une mutation du gène d'un
récepteur au facteur de croissance des cellules nerveuses
(NGF).
D'une part, seules quelques formes de ces
anomalies congénitales sont suspectées avoir un
déterminisme génétique direct et d'autre part
le NGF est bien connu pour avoir d'innombrables rôles et pas
seulement sur les cellules nerveuses...
Pour ce qui concerne les anomalies congénitales
d'insensibilité à la douleur je n'ai trouvé
que deux références, mais elles sont probablement
symptomatiques:
* la neuropathie sensitive et autonomique type 4 ou
Insensibilité à la douleur avec anhydrose (site
orphanet) (fichier de synthèse en anglais: http://www.orpha.net/data/patho/GB/uk-HSANIV.pdf)
dont voici le résumé: La neuropathie sensitive
autonomique de type 4 est une maladie excessivement rare.
Seulement une trentaine de cas ont été
rapportés. C'est une affection génétique
autosomique récessive, caractérisée par une
insensibilité à la douleur et une anhydrose
entraînant des accès d'hyperthermie
récurrents, des auto-mutilations, des infections
récurrentes, une ostéomyélite chronique, des
déformations des os et des articulations, et des
amputations des membres. Les études ultrastructurales et
morphométriques des nerfs périphériques
montrent une perte en fibres non myélinisées et peu
myélinisées. Le mécanisme physiopathologique
de cette anomalie du développement est toujours inconnu.
(Dr S. Aymé -septembre 2002)
* certains types d'insensibilité à la douleur
doivent être dues à un contrôle
morphinomimétique (qui met en jeu des
neuromédiateurs se fixant sur des récepteurs
morphiniques) endogène car le seuil du réflexe
nociceptif de flexion, normalement très élevé
chez les patients qui sont atteints de cette insensibilité,
prend en effet une valeur presque normale après injection
de naloxone (H. Dehen et al.) (EU douleur)
Comment a-t-il pu germer
l'idée dans la tête des concepteurs de ce programme
de 1èreS (puisque cet exemple est nommément
cité dans les activités proposées) de faire
reposer le déterminisme génétique du
développement neuronal sur cet exemple qui touche quelques
dizaines de personnes au monde et dont le déterminisme
physiologique est inconnu ?
4.2 La glycémie, une variable
homéostatique
Sources:
Physiologie animale; adaptation et milieux de vie, Knut
SCHMIDT-NIELSEN, Dunod, 1998
Précis de Physiologie, A. Calas, J-F. Perrin, C. Plas et P.
Vanneste; Doin, 1997
D'après le programme:
«Seule est étudiée la régulation de la
glycémie à court terme après un jeûne de
courte durée ou après un repas. L'intégration de
la glycémie dans des boucles de régulation plus
complexes, sous-tendant des processus de régulation à
long terme, ne fait pas partie du programme».
On notera aussi que les deux seules hormones au programme sont
l'insuline et le glucagon. Nous nous y tiendrons.
Dans le but d'étudier l'intégration (ou
coordination) des travaux du vivant, le programme de 1èreS,
dans la continuité de celui de la classe de 2nde, nous demande
de traiter le travail de nutrition (voir cours de
seconde, partie 2.
Il existe deux grands types trophiques: l'autotrophie (se nourrir
seul) et l'hétérotrophie (ou plutôt
l'allotrophie - se nourrir des autres)
).
La glycémie est
la concentration en glucose du sang. Sa valeur moyenne
(mesurée dans les veines du bras) oscille entre deux valeurs
extrêmes habituelles: 0,8 g.L-1 et 1,2 g.L-1
(soit 4,2
mmol.L-1 à 5,7
mmol.L-1). Localement, elle
peut atteindre des valeurs un peu plus faibles et nettement plus
élevées
(jusqu'à 50
mmol.L-1 soit 9,6
g.L-1).
rappel: TP-TD
: Les systèmes de communication de l'organisme
page
complémentaire:
éléments de biochimie pour les élèves de
1ère S
4.2.1 - Le glucose est la forme circulante
de l'énergie entre cellules
Le glucose est la forme circulante (de
cellule à cellule) de l'énergie chez les
pluricellulaires (comme l'ATP est la forme intracellulaire de
transfert de l'énergie chimique de
liaison). Le glucose est présent dans le
sang et la lymphe (interstitielle) à des taux variables mais
qui reflètent l'activité et l'état
physiologique de l'organisme.
La nourriture est formée de matière et
d'énergie.
* En ce qui concerne la source de matière, nous avons vu en
seconde (voir cours
de seconde, paragraphe 1.5) que les
animaux sont hétérotrophes car ils utilisent une
nourriture organique, ou mieux encore qu'ils sont allotrophes
car ils consomment d'autres êtres vivants (des proies vivantes
ou mortes). Les matières organiques et minérales qui
arrivent dans l'organisme (dans le milieu intérieur,
c'est-à-dire entre les cellules) sous forme de
nutriments sont variées (voir tableau
ci-dessus).
* De même nous avons vu que les animaux sont
chimiotrophes du point de vue de leur source d'énergie
car ils puisent leur énergie dans l'énergie chimique
des substances organiques qu'ils consomment. Nous allons voir que
c'est le glucose qui est la principale source d'énergie
chimique des cellules des animaux.
Les nutriments sont variées (glucides simples, aa,
glycérol et acides) mais peuvent tous être
transformés en glucose, principalement par le foie.
L'alimentation étant discontinue alors que l'utilisation du
glucose par les cellules étant continue, il existe des formes
de stockage du glucose.
Le glucose est consommé pour le catabolisme
énergétique par toutes les cellules. Cependant
certaines cellules peuvent utiliser d'autres nutriments
énergétiques.
Le glycogène est la forme de stockage la plus facilement et
rapidement mobilisable (même en absence d'O2) même s'il
prend plus de place que les lipides. Les lipides sont une forme de
stockage énergétiquement plus dense mais moins
facilement utilisable et surtout qui demande la présence de
dioxygène.
|
Masse par unité d'énergie
comparée entre 4 formes de stockage
énergétique dans le monde
vivant
(in Schmidt-Nielsen,
p173)
|
|
composés de stockage
énergétique
|
masse par unité d'énergie
(g.kJ-1)
|
|
graisse
|
0,026
|
|
protéines
|
0,055
|
|
amidon
|
0,057
|
|
glycogène + eau
|
0,24
|
Le glycogène (présent chez les animaux
(vertébrés et invertébrés) mais aussi
chez les champignons) présente une masse dix fois plus
importante que les lipides
(si l'on tient compte de la masse d'eau stockée avec le
glycogène estimée entre 3 et 5 g d'eau pour 1g de
glycogène stocké)
pour une quantité d'énergie stockée
identique.
Si l'amidon est une forme habituelle de stockage
énergétique chez les plantes, les protéines et
les graisses sont aussi mises à contribution dans les graines
par exemple.
Remarques importantes:
Si les cellules nerveuses et les hématies ne consomment que du
glucose, la plupart des cellules peuvent consommer des acides gras
circulants et certaines consomment aussi des acides aminés
circulants à des fins énergétiques dans
des conditions particulières.
Mais:
* les acides gras (A.G.) ont un rôle
énergétique principal de réserve. Leur
utilisation comme nutriment énergétique ordinaire est
secondaire (sauf chez certaines cellules notamment du foie et du
rein) ou tout au moins partagé avec des rôles essentiels
structuraux (constituants principaux des membranes, couches
protectrices thermiques...) et fonctionnels (l'acétyl coenzyme
A (produit de la dégradation des acides gras) est un carrefour
métabolique dans la cellule, synthèse
d'hormones...);
* le taux sanguin et surtout le taux de la lymphe en A.G. est
très variable selon les apports alimentaires et les particules
lipidiques sanguines sont captées rapidement par le tissu
adipeux, le foie, le cœur et les autres muscles
(voir cours
général sur la nutrition
humaine). Il n'y a pas de régulation de la
lipidémie comme on l'observe pour la glycémie,
notamment parce que les formes de transport des lipides sont
variées;
* les acides aminés issus des protéines
alimentaires digérées ne sont pas stockés dans
l'organisme mais utilisés par les cellules pour construire (et
renouveler) leurs propres protides; certains aa sont
synthétisés par les cellules. Ce n'est qu'en cas de
jeune prolongé (ou d'une alimentation
déséquilibrée beaucoup trop riche en protides)
que les aa sont consommés en grande quantité comme
substrat énergétique, notamment dans les muscles. Le
foie peut synthétiser du glucose à partir de certains
aa dits gluco-formateurs (les réactions font partie de
la néoglucogénèse).
* les corps cétoniques peuvent être
utilisés à des fins énergétiques à
la place du glucose par la majorité des cellules.
4.2.2 Analyse de courbes et
d'expériences: les faits expérimentaux
Les expériences s'insèrent bien sûr dans une
théorie (voir
méthode) mais nous nous
efforcerons principalement ici de faire des analyses de
résultats parfois très anciens et pour lesquelles les
théories sont méconnues, n'étant plus
accessibles autrement que par des recherches historiques.
Je renvoie aux méthodes d'analyse
de courbes et données acquises en seconde.
Courbes et
expériences:
- glycémie ordinaire
journalière mesurée toutes les 15 min - moyenne de 16
patients (Nathan, 148-1a) un seul patient (Bordas p139-B4)
- mesure du glycogène hépatique après 3 repas
sur 15 h (Nathan, 151-2a)
- hyperglycémie provoquée par voie orale - moyenne sur
10 sujets (Nathan, 148-1b) même courbe avec insulinémie
et glucagonémie (Nathan, 154-1a) - un seul patient (Bordas
p139-B6) et (Bordas p148-A2)
- hyperglycémie provoquée par voie orale et mesure dans
la veine porte hépatique, la v. sus hépatique et
l'artère hépatique ((Nathan, 149-2c)
- perfusions d'insuline et de glucagon chez le chien et mesure de la
glycémie (Nathan, 153-3)
- perfusion de glucose d'un pancréas isolé de chien,
mesure de l'insulinémie et de la glucagonémie (Nathan,
154-1b) (Bordas p149-B3) Ancien Bordas p 237 avec pic de
sécrétion de l'insuline et ultrastructure de la cellule
ß
- sécrétion d'insuline en fonction de la concentration
en glucose du milieu par des ilôts de Langerhans isolés
de rat (Nathan, 154-1c) (Bordas p149-B4)
- effet de l'injection d'insuline sur la glycémie, la
production hépatique du glucose et l'utilisation du glucose
chez l'homme (Nathan, 155-2a) (Bordas p146-A1) courbes de bilan
hépatique du glucose chez un chien normal à jeun et un
chien diabétique à jeun (bac)
- effet d'une perfusion de glucagon chez le porc (Nathan, 155-2b)
(Bordas p146-A1)
- effet de la concentration plasmatique d'insuline sur la production
hépatique de glucose et sur le prélèvement de
glucose par les autres organes (Nathan, 155-3)
- mesure de la glycémie
à la suite de l'injection de 20 mL de glucose à 5% dans
l'artère afférente au pancréas d'un chien
(bac)
- mesure de la glycémie à la suite de l'injection de 20
mL de glucose à 5% dans l'artère afférente au
pancréas greffé au cou d'un chien (bac)
- taux de réabsorption
rénale du glucose (BG1-2002 p 145 -3)
- couplage glycogénolyse-glycogénogénèse
dans le foie (BG1-2002 p 146 -5)
- insulinémie, glycémie et glucagonémie avant,
pendant et après un repas ((BG1-2002 p 147 -6)
- origine du glucose consommé lors d'un jeune de 10 jours chez
l'homme (BG1-2002 p 157 -17)
- stress de la tonte chez le mouton (BG1-2002 p 166 -26)
- adaptation du nouveau-né au stress hypoglycémique
à la naissance (BG1-2002 p 170 -28)
- différents
récepteurs au glucose dans les cellules humaines (BG4-2001 p
774 -2)
4.2.3 Une application du principe
d'homéostasie à la nutrition du tissu nerveux
L'homéostase désigne
l'état
d'équilibre intérieur d'un organisme face à des
modifications du milieu
extérieur.
La racine latine homœo orthographiée
homéo en français viendrait du grec
homolos (= semblable) et n'est donc pas différente de
la racine homo. C'est le physiologiste anglais
W. B. Cannon qui forga ce mot vers 1932 en
réunissant deux racines grecques: homœo et
stasie (= position).
On emploie indifféremment
homéostase (qui se rapporte à l'état
caractéristique: un système homéostatique est
dit "en homéostase") ou homéostasie (qui
désigne plus particulièrement la
propriété d'un
système).
Remarque :
Il est surprenant de voir utilisé le terme
d'homéostat pour le vivant (par les concepteurs
du programme !!!) alors que ce terme, utilisé en technologie,
vient de la physiologie mécaniciste héritée du
XIXème siècle (l'homéostat est, en technologie,
un appareil électrique inventé par Ashby en 1948 qui
simule l'homéostasie des organismes vivants). C'est comme si
l'on décrivait un sapin vivant à partir d'un sapin en
plastique. J'imagine bien sûr que ceux qui emploient
récemment ce terme veulent désigner le modèle et
non pas la fonction modélisée. L'usage tranchera. Je
préfère conserver les termes d'homéostase et
d'homéostasie.
La notion de régulation, empruntée à
la mécanique, est plus ancienne, et date d'au moins la fin du
XVIIIème. Actuellement la régulation est
le maintien du fonctionnement d'un système
(souvent avec le sens d'une conformité à une
norme, ce qui est nettement plus délicat
à employer en biologie - voir l'introduction
du cours sur la
pression artérielle). Je ne recommande donc pas son
emploi.
Remarque:
Il est à noter que Claude Bernard, probablement
persuadé de la profonde différence entre le vivant et
la machine (il était vitaliste), s'est contenté
dans ses théories du fonctionnement de l'organisme comme un
tout, d'utiliser les termes de "balance", "équilibre" et
"compensation", et non de "régulation", fort employé
déjà par des biologistes de son temps. En effet,
après avoir mis en évidence le rôle du milieu
intérieur dans la vie des animaux supérieurs, il a
opposé au mode de « vie oscillante»
directement soumise aux variations du milieu, le mode de
« vie constante ou libre », dans laquelle
les éléments cellulaires de l'organisme sont
protégés contre les changements dans le milieu
extérieur. Un tel animal n'est pas indifférent au
milieu ; il est en relation avec lui « de
façon telle que son équilibre résulte d'une
continuelle et délicate compensation établie comme par
la plus sensible des balances » (Leçons sur
les phénomènes de la vie communs aux animaux et aux
végétaux, 1878). (in EU article régulation
de Canguilhem).
Je rappelle le premier principe dynamique du vivant vu en
classe de seconde:
|
1er
principe de dynamique du vivant =
principe
d'homéostasie
«
un être vivant
est un système homéostatique ou en
homéostase »
ou
« les
fonctions du vivant sont STABLES
(résistantes
à de petites perturbations)
»
|
Un essai de formulation plus rigoureuse du terme
de fonction (voir aussi
ci-dessous)
La fonction f est représentée par une courbe
qui décrit les valeurs de la fonction en tout point
d'un espace à deux dimensions où le temps (x)
et la glycémie (y) sont les deux paramètres :
y = f(x)
|
|
fonction
|
axe des y
|
axe des x
|
commentaires
|
|
fonction = maintien au cours de la journée,
lors de repas et d'activité, au cours du sommeil, du
stock de glucose circulant dans le sang et la lymphe
à disposition des cellules
|
y = glycémie
enregistrée à tel ou tel endroit sur tel ou
tel organisme
|
temps
sur 24h
|
la glycémie est mesurée habituellement sur
une veine du bras.
Quelles informations peut-on
tirer de l'étude (et de la comparaison) d'une courbe
glycémique d'une journée chez un seul individu
(Bordas B4 p 139) et celle obtenue à partir de la
moyenne chez 16 individus (Nathan, 1a p 148) ayant eu (?)
les mêmes activités et prises alimentaires
?
On cherche à établir un lien entre les
variations du paramètre mesuré et un
mécanisme physiologique général. Si la
glycémie baisse c'est que les apports diminuent et/ou
les départs augmentent et inversement.
Un seul individu: chez un individu donné la
glycémie peut varier entre telle et telle valeur. au
repos elle est relativement stable, autour de 0,9
g.L-1; lors d'un et après un repas elle
augmente (plus ou moins selon le repas et les individus)
puis revient en quelques heures à la valeur de repos;
lors d'un effort, et après un effort, elle ne baisse
pas significativement.
Pour une moyenne de seize individus on perd des
informations en les superposant. La comparaison de 16
courbes apporte une information bien supérieure. Le
chiffre de 16 est probablement insuffisant pour
généraliser les limites et les sens de
variations.
La glycémie oscille
chez la plupart des individus en bonne santé,
indépendamment du sexe, entre 0,75 et 1,2
g.L-1. Elle augmente transitoirement lors des
repas mais ne diminue pas notablement lors
d'activités physiques.
La fonction correspondante de maintien de la
glycémie (veineuse au bras) est donc une fonction
de type homéostatique
(l'homéostasie
peut être définie provisoirement comme le
maintien d'un équilibre face aux perturbations
extérieures - voir
ci-dessous).
|
Le terme de
fonction est aussi très riche de sens. Il a
probablement une origine biologique et sociologique
(cette idée n'a été
soutenue que tardivement par René Thom; voir Analyse
sémantique d'un mot polysémique: la fonction, 1993,
Séminaires de la Société de Biologie
Théorique, année 1992-1993, Acta Biotheoretica, 42
), puis qui a été
formalisée en mathématique (dans
le plan, la fonction (numérique) d'une variable (x) est
représentée par un graphe y=f (x); en
mathématique la représentation d'une relation de
quantité (avec des variables numériques) ou de
qualité entre deux ensembles d'objets est défini par le
terme moderne d'application (Fréchet, 1909))
, et enfin est retournée dans le
domaine social et dans celui de la biologie.
La vie est un processus fonctionnel. Classiquement on parle des trois
grandes fonctions du vivant: se nourrir, communiquer et se
reproduire. Personnellement je préfère la notion de
travail, plus riche (voir
cours de
seconde) que je
formule ainsi: "la vie est un travail de relation, de nutrition et
de reproduction".
La notion de fonction est un tournant de l'analyse des
phénomènes vivants (voir
note en bas de
page à partir d'un texte de
René Thom).
La compréhension du monde vivant a
toujours été associé à celui de l'homme
d'abord et des sociétés humaines ensuite.
Fonctionnalisme et organicisme sont des
termes utilisés en sciences sociales pour désigner des
théories qui comparent les sociétés humaines
avec le fonctionnement d'un ou d'une partie d'un être vivant.
De nos jours on parle davantage de sociobiologie.
Claude Bernard lui-même, en proposant de prendre l'organisme
vivant comme modèle de système dont les
sociétés humaines doivent s'inspirer, n'est pas le
moins illustre de ces savants qui n'hésiteront pas à
prétendre unifier leur compréhension du monde dans une
philosophie.
Avec l'outil de la "théorie des catastrophes" ce serait
plutôt la notion de forme qui pourrait
prétendre à un tel avenir. Dire que la glycémie
est un paramètre du vivant est en quelque sorte
affirmer que le vivant est modélisable, ce que tous les
physiologistes font. A notre niveau de classe de 1ère S il est
essentiel de revenir dessus pour bien préciser quel est notre
outil.
Raisonner en terme de fonction c'est aussi raisonner en terme de
finalité, de sens (et donc répondre à la
question "pourquoi ?"), et pas uniquement en terme de
mécanisme (que l'on peut supposer répondre à une
question utilisant l'adverbe comment).
Pourquoi maintenir une
glycémie stable ? A quoi cela sert-il
? Dans quel but l'organisme
maintient-il ce paramètre stable ?
La glycémie ne constitue pas une fonction biologique
qui puisse être regardée comme dynamiquement stable.
La glycémie n'en est qu'un
paramètre participant d'un processus
d'homéostase ou fonction de type homéostasique. Quelle
est donc cette fonction ?
|
La fonction maintenue stable (donc
homéostatique), malgré la période
d'activité ou de repos (ce qui est
net), malgré l'effort
(ce qui est très net),
malgré les repas (ce qui est moins net si
l'on se contente de mesurer la glycémie à la
veine du bras mais beaucoup plus net si on mesure la
glycémie au niveau artériel céphalique
par exemple) est donc la
fonction de nutrition
des cellules.
|
La question qu'il faudrait se poser, et dont la réponse
dépasse bien sûr le cadre d'un cours de 1ère S,
est de savoir comment l'homéostase est
réalisée (Thom dirait "déployée") dans
l'espace de régulation qui contient tous les
états de tous les paramètres liés à la
fonction maintenue.
On remarquera que l'on peut ainsi parler d'homéostase
cellulaire, populationnelle, sociale...
Dans le cadre de ce cours, et pour faire simple, mais bien
sûr de façon non exhaustive, juste comme un
exemple, on pourrait dire que la
glycémie est la variable de l'homéostase
énergétique du tissu nerveux. Le glucose
sanguin assure en effet l'équilibre énergétique
nécessaire aux cellules nerveuses, puisqu'elles ne peuvent
faire de réserves de nutriment énergétique.
a - la glycémie est la variable
de l'homéostase énergétique du tissu
nerveux
L'homéostase étant basée sur une analogie
mécanique on peut présenter deux représentations
simples:
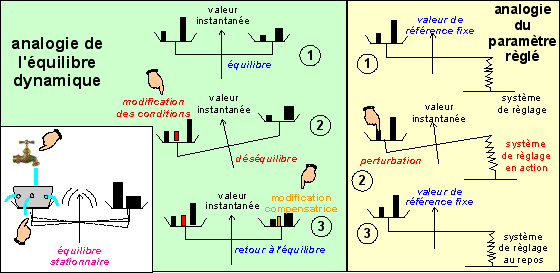
Selon le niveau d'observation où l'on se place, on peut
préférer l'une ou l'autre des représentations:
à petite échelle (donc d'une ou de plusieurs grandes
fonctions) l'équilibre dynamique est facilement
compréhensible comme expression de l'unité
physiologique (intégration des fonctions ou efficacité
du travail du vivant...) alors qu'à grande échelle (par
exemple celui d'un mécanisme moléculaire) l'analogie
avec un paramètre réglé (que l'on peut aussi
comparer à un "culbuto") est pertinente.
* modèle classique
Pour décrire le système de régulation le
formalisme habituellement proposé dans l'enseignement
secondaire et issu de la cybernétique (voir ci-dessus)
comporte deux rectangles (fonction réglée -
système réglant), où l'on place les capteurs,
régulateurs et effecteurs.
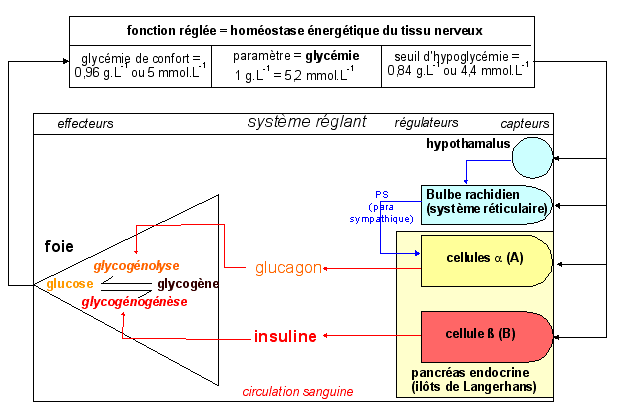
Dans cet exemple l'insuline et le glucagon sont clairement
antagonistes quand à leur fonction hypo et
hyperglycémiante. On notera que l'insuline possède,
à l'inverse du glucagon, de nombreuses autres cellules cibles
(et de nombreuses autres fonctions, que nous verrons ensuite) que les
cellules hépatiques. Les cellules alpha et ß sont des
capteurs sensibles à la glycémie du sang qui perfuse le
foie. On notera aussi que, même si elle n'est pas
représentée, la commande nerveuse existe aussi bien
pour les cellules alpha que ß. Globalement la stimulation du
système parasympathique active la libération de
glucagon et inhibe la sécrétion d'insuline alors que
celle de l'orsthosympathique a un effet antagoniste
(voir système
nerveux
végétatif).
Remarque:
le mécanisme neuro-hormonal présenté ici est le
plus habituel mais ce n'est pas le seul mécanisme de
régulation. En effet, un animal hypophysectomisé et
pancréatectomisé est capable de maintenir sa
glycémie voisine de la normale, dans certaines conditions
(repos et régime approprié) (in EU
article glycémie). Ce qui semble prouver que la
glycémie peut se régler d'elle-même, sans
l'intervention du système neuro-hormonal. Cette
autorégulation s'explique par l'intervention de facteurs
physico-chimiques : taux de glucose dans le sang (dans le cas
des cellules insulino-sécrétrices cultivées in
vitro, l'effet des dérivés métaboliques du
glucose est démontré en relation avec le taux de
calcium intracellulaire) ; équilibre osmotique entre le
glucose du sang et celui des espaces interstitiels ;
élimination du glucose en excès par le rein...(le seuil
de réabsorption du glucose par le rein est de 1,92
g.L-1 soit 10 mmol.L-1).
|
Complément
* modèle moderne
Ce qui est profondément frustrant avec le
schéma précédent c'est que le tissu
vivant, qui consomme le glucose, semble ici étranger
au système de régulation. Celui-ci est en
quelque sorte extérieur au système: des
organes contrôlent la fonction de nutrition d'autres
organes. Alors que je pense que l'organisme fait un tout
(la vie est une propriété non
locale et c'est tout le travail d'une biologie
théorique d'en montrer des propriétés
ou fonctions locales). Je pense que le système
vivant est à la fois celui qui consomme et celui qui
règle la consommation ou du moins qu'il fait partie
du système réglant. C'est pour cela que je
préfère une modélisation globale du
système sans se préoccuper de savoir qui
règle et qui consomme. Le système vivant est
alors une boîte noire qu'on renonce à ouvrir
(du moins ouvrir "totalement", mais on peut avoir
plusieurs niveaux d'approche) et dont on regarde le
fonctionnement de l'extérieur en faisant varier
quelques paramètres de contrôle
(voir aussi une
page en travaux pour une autre
présentation et davantage de
références).
Je tiens à souligner combien cette partie est encore
"prospective".
|
|
Des conditions expérimentales au
modèle:
- la glycémie
artérielle afférente au niveau du tissu
nerveux céphalique correspond à un
point stable dans le temps (qui
résiste à de petites perturbations venant de
l'activité (repos-effort), de la prise alimentaire
(repas, jeune court...), de l'état physiologique
(fièvre...), des phases veille-sommeil....).
- ce point est considéré
comme une singularité d'une
application définie dans
un espace de grande dimension qui représente le
métabolisme. Ce point est
apellé un point catastrophe.
Faute de pouvoir connaître de la
figure complète du métabolisme, l'idée
est de réduire le problème, par des
approximations simples, à un nombre de
paramètres qui permette de le solutionner. C'est
l'inestimable découverte de René Thom que
d'avoir montré que non seulement le problème
peut avoir des solutions mais qu'elles sont SIMPLES
(géométriquement exprimées), en PETIT
NOMBRE (7), TRÈS GÉNÉRALES (on peut
faire des parallèles avec d'innombrables domaines des
mathématiques ou de la physique). Tout
phénomène présentant une
singularité (un lieu où il se passe
quelquechose de singulier(de discontinu) sur un fond
continu), pour peu que l'on prenne les hypothèses
simplificatrices exposées ci-dessous, peut
s'expliquer, mathématiquement, à l'aide de ce
que l'on a apellé la Théorie des
catastrophes.
On considère que le phénomène
étudié est représenté par une
fonction de RnxRN : F(p1,
..., pn, x1, ..., xN); les
pi étant les paramètres
externes, accessibles à l'expérimentateur,
et les xj, les variables internes, non
acessibles (on peut observer leur valeur mais pas les fixer
expérimentalement: ce sont elles qui sont
associées au phénomène observable).
Dans le cas d'un espace avec n æ 4 et N æ 2 René Thom
a prouvé, par des calculs non accessibles à
des non mathématiciens (c'est la notion de
déploiement universel d'une singularité
différentiable), qu'il existe 7 catastrophes
élémentaires et seulement 7.
La première hypothèse consiste à
supposer que le phénomène que l'on
désire modéliser dérive d'un potentiel,
ce qui permet d'utiliser les équations
différentielles, déjà bien connues des
physiciens. Concrètement cela consiste à dire
que le phénomène que l'on désire
étudier possède des variables internes
(x1, ..., xN) qui présentent un
minima lorsque l'on fait varier les paramètres
externes (p1, ..., pn). Les
équations différentielles étant alors
dxi/dt = - d F (p1, ...,
pn, x1 ..., xN )/ dxi avec
1 æ i æ N (
(voir aussi une
page en travaux ). Je
précise que tous ces modèles correspondant
à des dynamiques, le temps est toujours un
paramètre présent mais qui n'est
représenté qu'à travers les autres
paramètres de contrôle (ce n'est pas le temps
qui agit, il n'est qu'une mesure de la vie... c'est une
durée très
bergsonienne).
Au point catastrophe il existe
un attracteur (au sens mathématique,
voir page sur
les modèles) du
métabolisme dont la structure et la topologie
réflètent la fonction biologique en ce
point.
Donc en résumé ce point
catastrophe est une singularité
d'une application
différentiable du type F (p1, ...,
pn, x1, ..., xN), avec
pi les paramètres externes, et
xj les variables internes et n æ 4 et N æ
2.
|
Représenter une
figure métabolique non
représentable....
|
la forme métabolique
imaginaire....

Le métabolisme d'un organisme (au niveau
de certaines fonctions locales qui le
décrivent) est stable par rapport à
de petites variations. Il peut donc être
représenté par une FORME dans une
ESPACE DE GRANDE DIMENSION (voire de dimension
infinie).
|
un détail...
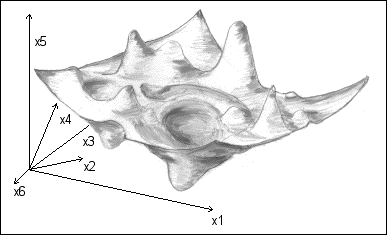
Une "représentation" du paysage
épigénétique de Waddington
repris par Thom comme figure de régulation
métabolique de l'organisme dans un espace de
grande dimension (non
représentable...
donc, évidemment, pour ce schéma le
nombre de dimensions est de 3 même si 6 axes
imaginaires sont indiqués) et
les formes sont "lisses" alors qu'on les imagine
très complexes.
|
|
Conrad Hall Waddington, dans les années
1960, avait introduit la notion de paysage
épigénétique «
epigenetic landscape » comme un
arbre de trajectoires descendantes du haut d'une
colline hémisphérique pour
décrire des évolutions divergentes
des tissus embryonnaires. Cette figure a
été reprise par Thom et voici sa
traduction en motif en creux et bosses, les points
les plus bas indiquant des points de
stabilité des fonctions locales (un
attracteur en mathématiques), les points
élevés des domaines
d'instabilité (bifurcation). La forme
générale en creux étant une
image de la fonction globale, par exemple ici la
nutrition. La stabilité du paysage dans le
temps et par rapport à de petites variations
des paramètres de contrôle est une
caractéristique importante de cette figure
métabolique.
|
Une image..... d'un
paysage stable malgré les petites
déformations.... 
|
|
La figure globale du métabolisme est
INACESSIBLE de par sa complexité (nombre de
variables) mais l'on peut dans chaque cas concret,
FAIRE DES APPROXIMATIONS et réduire les
variables à un nombre accessible à
une résolution géométrique (3
ou 4). L'approximation la plus importante
étant que la fonction du vivant
étudiée localement en un point
DÉRIVE D'UN POTENTIEL (noté F ou V
selon les pages) et que l'on peut donc utiliser
l'outil des équations
différentielles. (voir
page
annexe)
|
|
|
Un essai de représentation avec le
modèle de fronce :
Pour avoir un puits de potentiel présentant une
symétrie selon deux directions opposées il
faut envisager au moins deux paramètres externes
p1 et p2 qui pourraient être
(p1) le flux entrant de glucose dans la
circulation (absorption du glucose par apport alimentaire,
déstockage hépatique...) et (p2) le
flux sortant de glucose de l'appareil circulatoire
(par la consommation en glucose globale de l'organisme - qui
pourrait rendre compte de l'activité musculaire
principalement en s'efforçant de considérer
que tous les autres paramètres sont fixes).
La glycémie n'est plus alors un paramètre mais
bien une sortie (x) non contrôlable mais
observable. x est la morphologie du
système, stable face à de
petites perturbations ; on pourrait aussi dire que
c'est la réserve glucidique sanguine ou le
flux glucidique sanguin. Je voudrais ainsi modifier la
vision habituelle des physiologistes qui, quand ils
affirment que la glycémie est stable ou
contrôlée, y voient un système
cybernétique avec un système de contrôle
plus ou moins localisé dans le système nerveux
central et nécessitant des capteurs et des
régulateurs. Je voudrais donc y substituer
l'idée simple que la
glycémie, comme morphologie stable d'un
système dynamique dont la fonction peut être
approchée par un potentiel, se trouve au niveau d'un
minimum stable de ce potentiel. La stabilité
devient ainsi une propriété intrinsèque
de la dynamique et n'a plus rien de magique ou de
contrôlée extérieurement par un
système qui ne dit pas son nom.
ce qui est difficile à saisir est que, de
façon inhabituelle, F(x) ne désigne pas le
résultat observé mais
c'est x qui est le
résultat, la
fonction reste cachée et F n'en est qu'un
modèle. Pour "voir" le comportement du système
il ne faut pas "regarder" les F(x) mais les x seulement.
Les surfaces
(qui donnent leur nom à la catastrophe) ou les
courbes (projections ou ensemble de bifurcations)
représentant les points singuliers de F (points
catastrophiques) nous permettent de visualiser les
différentes valeurs critiques de x en fonction des
paramètres de contrôle (on approche ainsi ce
que l'on appelle la structure de l'attracteur (ou des
attracteurs): figure mathématique qui explique la
stabilité de la fonction). Il ne faut donc pas
confondre la forme du potentiel (qui approche la fonction
cachée) et la forme de l'attracteur (ou des
attracteurs en conflit) qui est représentée
par l'ensemble des catastrophes.
On considère alors que la fonction de nutrition
cachée dans la boîte noire du vivant est un
potentiel que le vivant stabilise (minimise) par
homéostasie. Ce potentiel à pour expression
Fp1,p2(x)= (x**4) + p1*x**2 +
p2*x (* représente
l'opérateur multiplication et ** l'opérateur
puissance). On ne peut pas représenter directement
(en dimension 4) la fonction Fp1,p2(x) donc on se
contente (en dimension 3) de la surface des points de
l'espace de contrôle pour lesquels sa
dérivée est nulle: c'est à dire
F'p1,p2(x) = 0 ; et donc 4*x**3 +
2*p1*x + p2 = 0. Cette surface est une
fronce (cusp en anglais)
en rouge ci-dessous.
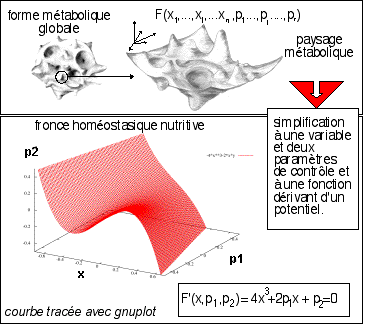
Pour des précisions sur
gnuplot voir la page
complémentaire sur la théorie des
catastrophes
|
Cette applet est empruntée à
Lucien Dujardin (http://perso.wanadoo.fr/l.d.v.dujardin/index.html)
qui en propose une pour chaque catastrophe
élémentaire (voir page
sur les modèles); elle a juste
été modifiée pour l'affichage
des paramètres de contrôle;
Reportez-vous à la page de M.
Dujardin pour des explications
complètes.
|
Entrées
(déplacez
la souris dans l'espace de
contrôle)
(cliquez
dans l'espace de contrôle pour
démarrer ; rechargez la page si
l'applet ne s'affiche pas correctement,
afin de réinitialiser
celle-ci)
|
la
courbe
représente un potentiel
F(x,a,b)=x4+a
x2+b x,
qui modélise le comportement de la
fonction inaccessible
(les valeurs des
paramètres a et b ne sont pas
exactement celles affichées, du
fait de contraintes de
représentation; la courbe est ici
un modèle qualitatif)
|
|
a = "normal
factor"
|
|
Le
système vivant est
considéré comme une
boîte
noire
(grise
ici) dont les
fonctions complexes peuvent être
approchées (grâce à
des simplifications) par des potentiels
qu'il minimise.
(convention
choise = règle du retard, voir
page
explicative
attention! Elle comporte des applets
à télécharger, un peu
lourdes (1Mo)...)
|
|
espace de
contrôle
|
b = "splitting factor"
(facteur d'écartement)
|
x
= Sortie
(c'est le minimum du
potentiel qui donne la valeur de
sortie de la fonction)
|
La même applet a été
modifiée afin de présenter un
potentiel qui donne les valeurs observées
pour l'homéostase nutritionnelle
glycémique:
|
Entrées
(déplacez
la souris dans l'espace de
contrôle)
(cliquez
dans l'espace de contrôle pour
démarrer ; rechargez la page si
l'applet ne s'affiche pas correctement,
afin de réinitialiser
celle-ci)
|
la
courbe
représente un potentiel
F(x,p1,p2)=
-
x4+p1x2+p2x,
qui modélise le comportement de la
fonction inaccessible
(les valeurs des
paramètres a et b ne sont pas
exactement celles affichées, du
fait de contraintes de
représentation; la courbe est ici
un modèle
qualitatif)
|
|
p1 =
"normal factor"
|
|
|
espace de contrôle
p2/p1
|
p2 =
"splitting factor" (facteur
d'écartement)
|
x
= Sortie
(c'est le minimum du potentiel
qui donne la valeur de sortie de la
fonction)
Du fait de la présence de
plusieurs minima (il y a toujours l'hypo
et l'hyperglycémie), le seul
minimum représenté (à
l'aide de la droite verticale) est celui
le plus facilement accessible du point
où l'on se trouve (chemin le plus
court, ce qui est une
caractéristique du
modèle).
|
Vous pouvez voir les programmes source de ces
applet: catapst.java et
catapstg.java
(ils ont été
compilés en pseudo-code à partie des
fichiers du site de M. Dujardin sans aucune
difficulté sur Mac avec les ressources Java
incluses dans le système : la commande de
compilation est javac catapstg.java
(elle doit se faire dans Terminal au même
niveau que le fichier source) et
génère un fichier
catapstg.class au même niveau que le
fichier source; je rapelle que les pseudo-codes
générés sous forme de fichiers
.class sont interprétables sur
pratiquement toutes les machines, ce qui fait leur
intérêt).
|
|
|
L'intérêt de tels modèles
réside dans leur efficacité
compréhensive même si
l'efficacité expérimentale est
encore limitée (plus par manque d'utilisation que par
défaut intrinsèque il me semble). On remplace
une vision mécaniciste et matérialiste
quasi magique du vivant par une vision pragmatique
ouverte mais formalisée mathématiquement. Au
lieu de dire que la physiologie de l'être vivant
constitue un équilibre dynamique (ce qui
n'explique rien et n'est en rien justifié si ce n'est
par l'efficacité expérimentale du
modèle, toute relative (que l'on
s'interroge sur la notion d'hormone, très
dépassée, qu'il serait possible
d'intégrer dans un paramètre plus large de
type informationnel, stimulant ou inhibiteur, d'un
système; la concentration de la substance
informationnelle (médiateur)
n'étant plus qu'un
paramètre - en relation avec beaucoup d'autres - de
l'état du système), on formalise
mathématiquement la fonction vitale en clarifiant les
approximations faites et les conditions de
validité (la fonction vivante
modélisée dérive d'un potentiel et la
vie consiste à minimiser ce potentiel). C'est
vraiment un travail scientifique et je crois que ce travail
de biologie théorique est promis à un grand
avenir.
|
b - la glycémie est une
variable de nombreuses fonctions
L'essentiel des données de cette partie
proviennent du Précis de Physiologie
publié chez Doin.
En plus des divers articles de l'EU, deux articles de
Biologie-Géologie me paraissent nécessaires à
citer:
Les réponses de l'organisme aux contraintes
énergétiques ou la régulation de la
glycémie revisitée, Jean Clos et Yves
Muller, Biologie-Géologie, n°1-2002, pp143-174; un bon
article de fond sur la compréhension du métabolisme
énergétique (ce qui n'est pas le sujet de ce cours ni
du programme de 1èreS) mais sans sortir du paradigme dominant
pour ce qui est des régulations.
Le diabète et le contrôle de la
glycémie, Roger Raynal, Biologie-Géologie
n°4-2001, 771-782; quelques données synthétiques
intéressantes notamment sur les récepteurs au glucose
et une revue des diabètes sucrés avec des informations
médicales et des liens pour une bibliographie plus
étoffée.
Lors d'un repas ou d'un effort la glycémie varie fortement
selon le point de mesure dans l'organisme. De nombreux
mécanismes sont mis en jeu pour stocker les nutriments dans le
premier cas et les mobiliser dans le second, et ils
interfèrent fortement avec la variable glycémique.
Présenter la physiologie de ces régulations conduit
à des schémas trop complexes qui n'apportent à
mon avis pas grand chose. Dans le cas d'un repas, d'un effort, d'un
stress,..., la glycémie n'est qu'une variable parmi tant
d'autres qui représente des fonctions très diverses aux
très nombreux paramètres. Pour ces fonctions la
glycémie n'est pas une variable stabilisée d'une
façon globale (partout dans l'organisme) mais peut
l'être localement comme c'était le cas pour la fonction
énergétique nutritive du tissu nerveux.
b1. l'insuline est à la fois
l'hormone du stockage du glucose et l'hormone de l'utilisation du
glucose
Nature chimique:
L'insuline est une hormone peptidique de 51 aa (deux
chaînes (A et B) de 21
(n°66 à 86-COOH) et
30 (n°1-NH2 à 30) aa
réunies par deux ponts disulfure (entre les aa
n°7-72 et 19-85)) de poids moléculaire voisin de
6000 daltons (5733 daltons pour l'insuline bovine; un
dalton (Da) est la masse de l'atome d'hydrogène: 1,7.
10-23 g).
Synthèse:
L'insuline est synthétisée par les cellules ß des
îlots de Langerhans pancréatiques.
La chaîne traduite à partir de l'ARN
messager comporte 110 aa (et est appelée
pré-proinsuline). L'ARN messager est transcrit à
partir d'un gène morcelé (comportant des parties
traduites et non traduites) situé sur le bras court du
chromosome 11. La préproinsuline comporte une
séquence signal qui permet l'entrée de la chaîne
dans la cavité du réticulum à la suite de sa
synthèse. Cette séquence signal est hydrolysée
et la molécule résultante de proinsuline est la seule a
subir un transit dans le Golgi.
La molécule de proinsuline (86 aa) est
scindée dans l'appareil de Golgi (et
libère un peptide C (de 31 aa associé à deux
dipeptides de liaison) qui est sécrété en
même temps que l'insuline qui est associée à des
ions Zn2+). L'insuline est stockée
dans des vésicules golgiennes et libérée sous
contrôle endogène (des propres cellules ß) et
nerveux (contrôle bulbaire et hypothalamique). Elle est
transportée par le sang avec une demi-vie circulante courte (6
à 10 min) sous une forme libre et sous une forme liée,
qui joue le rôle de réservoir.
Modes d'action :
Comme toutes les hormones protéiques elle se fixe à un
récepteur membranaire au niveau de ses cellules cibles. Deux
mécanismes d'activation sont évoqués :
*Les complexes récepteurs membranaires-hormone se rassemblent
dans une même région de la membrane qui s'invagine puis
forme une vésicule (endocytose) qui pénètre dans
la cellule. La vésicule est désagrégée
par les lysosomes et l'hormone est libérée à
l'intérieur de la cellule et active des systèmes
enzymatiques cytoplasmiques. Ce mécanisme est notamment
invoqué pour l'augmentation du nombre de récepteurs au
glucose (GLUT 4) médiée par
l'insuline chez certaines cellules (voir plus bas).
* La liaison hormone-récepteur active sur la face
cytoplasmique du complexe hormone-récepteur un système
métabolique (dans le cas de l'insuline il
s'agirait d'une activité enzymatique de type tyrosine kinase
(commune chez les facteurs de croissance), c'est-à-dire que
des molécules de substrats cytoplasmiques pourraient
être phosphorylées au niveau de l'aa tyrosine, ce qui
modifierait leur activité) que l'on peut qualifier de
message hormonal ou message endocrine (message
transporté par un médiateur endocrine ou hormone, en
provenance des cellules endocrines, et dirigé vers la cellule
cible). En fait, comme la cellule
cible ne peut être considérée comme demandeuse
d'information, le terme même d'information est probablement
inadéquat, bien que consacré par l'usage (voir
remarque
du cours de Spécialité de
TS). Les termes de
médiateur et message sont peut-être plus exacts mais non
moins porteurs d'idéologie.
Fonctions (rôles):
L'insuline possède principalement trois fonctions,
c'est-à-dire trois rôles qui diffèrent selon les
cellules cibles, leurs récepteurs et leur métabolisme.
On pourrait dire que l'insuline est un message hormonal qui a
plusieurs sens (non incompatibles) et une valeur (toujours
hypoglycémiante) :
* sur les cellules hépatiques, musculaires et adipeuses
, particulièrement sensibles à l'insuline, l'insuline a
une fonction de stockage (du glucose circulant mais
aussi d'autres nutriments comme les aa ou les lipides).
L'insuline augmente la glycogénogénèse
musculaire et hépatique, ainsi que la lipogénèse
adipeuse et hépatique. L'insuline inhibe par contre la
glycogénolyse hépatique et musculaire ainsi que la
lipolyse adipeuse.
* sur les cellules musculaires et adipeuses l'insuline a une
fonction de pénétration
facilitée du glucose (mais
aussi des AG pour les adipocytes). En effet, certaines
cellules, comme les cellules nerveuses, mais aussi les cellules
hépatiques, sanguines et les cellules du pancréas
endocrine, sont naturellement très "ouvertes" au glucose
(elles possèdent de nombreux récepteurs au glucose,
de type GLUT 1, GLUT2 et GLUT 3,
voir par exemple Roger Raynal,
Biologie-Géologie n°4-2001 p 774 , fig 2). Mais
les cellules musculaires et adipeuses sont normalement peu "ouvertes"
au glucose c'est-à-dire que sans insuline, le glucose
pénètre peu (les récepteurs au glucose
(de type GLUT 4) sont peu nombreux) et elles
ne consomment que peu de glucose. Par contre, en présence
d'insuline (on les qualifient alors
d'insulino-dépendantes), le glucose
pénètre en grande quantité dans ces cellules
(par augmentation du nombre de transporteurs
membranaires de type GLUT 4 suite à l'activation de la
transcription traduction des gènes de ce récepteur au
glucose mais aussi à l'exocytose transitoire (suivie d'une
endocytose dès que l'action de l'insuline cesse) de
vésicules dont les membranes portent ces récepteurs
- voir "Transport du glucose
dans la cellule musculaire" dans l'EU, article "histologie" ou sur
internet http://hometown.aol.com/_ht_a/drfatalis/Images/recrute.gif
) et l'utilisation du glucose y est
fortement stimulée (glycolyse). Le glucose
pénétrant dans une cellule y est immédiatement
phosphorylé (transformé en glucose-6P). C'est le
glucose-6P qui est le métabolite de départ des
réactions de respiration ou fermentation cellulaire
(par la glycolyse commune à ces
mécanismes). La déphosphorylation ne peut
être réalisée que dans le foie car les
hépatocytes sont les seules cellules à posséder
une glucose-6 phosphatase qui transforme le glucose-6P en glucose
(les cellules rénales, parmi d'autres rares
cellules, la possèdent aussi) et la membrane est
imperméable aux composés phophorylés. L'insuline
favorise l'entrée des AG circulants dans les adipocytes.
* sur de très nombreuses cellules l'insuline à une
fonction d'augmentation de l'utilisation du glucose.
Elle stimule la glycolyse et la voie des
pentoses-phosphate.
Remarque:
L'insuline peut aussi être considérée comme un
facteur de croissance. L'insuline est une hormone
dont on n'a pas fini de découvrir les rôles. Elle active
notamment la prolifération et la croissance cellulaires in
vitro et une famille de facteurs de croissance lui est
rattachée (IGF: insulin-like growth factors) avec une nature
protéique, une structure et un mode d'action
communs.
b2. le glucagon est l'hormone des besoins en
glucose (hyperglycémiante)
Le glucagon est un petit peptide de 29 aa (3500 Da)
sécrété (à partir d'un
précurseur de 9000 Da) par les cellules alpha (A)
situées à la périphérie des ilôts
de langerhans (à partir d'un gène
situé sur le bras long du chromosome 2) sous commande
endogène (des propres cellules alpha) ou nerveuse
(hypothalamique et bulbaire). Les cellules cibles sont les cellules
hépatiques pourvues de récepteurs membranaires au
glucagon. La fixation du glucagon à son récepteur
active un système métabolique assez
général (notamment par la
synthèse d'AMP cyclique à partir de l'ATP) et
conduit à une stimulation de la glycogénolyse et
donc à la libération du glucose dans le sang
(puisque les cellules hépatiques
possèdent une glucose 6 phosphatase... voir plus haut).
Le glucagon stimule aussi la sécrétion d'insuline par
les cellules ß voisines: c'est ce que l'on appelle un effet
paracrine (médiateur chimique agissant sur de
courtes distances sans transport par le sang: voir TP).
L'insuline inhibe la synthèse et la
sécrétion de glucagon par effet paracrine
opposé. L'insuline, sécrétée en
même temps que le glucagon favorise surtout l'utilisation du
glucose (voir ci-dessus et ci-dessous).
b3. lors d'un repas l'insuline est libérée pour
favoriser le stockage du glucose
Lors d'un repas riche principalement en glucides (et surtout de
sucres lents, c'est-à-dire complexes, comme l'amidon),
l'insuline est sécrétée avant tout pour
favoriser le stockage du glucose. Si le repas est même
composé uniquement de glucides (et surtout de sucres rapides,
c'est-à-dire simples, comme le glucose ou le fructose...) il
peut y avoir une hypoglycémie transitoire due à
l'action hypoglycémiante de l'insuline. C'est aussi ce que
l'on observe lors de l'injection de glucose expérimentale.
Lors d'un repas équilibré en glucides, acides gras
(lipides) et protides, insuline et glucagon sont
sécrétées simultanément et la
glycémie reste équilibrée: il n'y a pas
d'hyperglycémie postprandiale. Cela ne signifie cependant pas
que la glycémie est "régulée". C'est vraiment un
exemple d'équilibre dynamique (ou
d'homéostase) sans avoir besoin de faire intervenir un
mécanisme de régulation autour d'une valeur fixe.
Lors d'un repas riche pris alors que les réserves
hépatiques ne sont pas épuisées la
glycémie on observera par contre une hyperglycémie
transitoire. du fait du temps de latence de sécrétion
et d'action de l'insuline
Nous avons vu (TD analyses de courbes) que les réserves
hépatiques en glucose sont de l'ordre de 100 à 120 g,
ce qui constitue une réserve suffisante pour 10 à 12
heures de sommeil ou de repos (5 g.h-1 de glucose
consommé pour les cellules nerveuses et la même
quantité pour toutes les autres cellules des tissus
périphériques). Au réveil, si les
réserves hépatiques sont épuisées il est
important de les reconstituer par un "petit déjeuner" sinon
l'organisme consommera des AG pour les tissus
périphériques mais les cellules nerveuses ne consommant
que du glucose, le foie sera obligé de fournir du glucose par
néoglucogénèse (à partir des AG ou
des aa). Lors d'une prise alimentaire intervenant alors que la
néoglucogénèse fonctionne, on observe une assez
forte hyperglycémie étant donné que l'insuline
met près de 2h à inhiber la
néoglucogénèse.
La vue et l'odorat sont déclencheurs d'une faible
sécrétion d'insuline qui prépare le foie au
stockage du glucose. Des stimuli mécaniques buccaux et
gastriques provoquent ensuite une sécrétion d'insuline
plus importante. Enfin, par voie hormonale, le transit intestinal
stimule aussi les sécrétions pancréatiques.
b4. lors d'un effort insuline et glucagon sont
libérés simultanément pour permettre
l'approvisionnement énergétique des cellules
musculaires et nerveuses
On a vu en classe de seconde
que lors de l'effort l'organisme permet le travail musculaire
grâce à une augmentation des débits ventilatoire
et cardiocirculatoire. Le maintien d'un apport
énergétique suffisant aux organes en fonctionnement
n'est pas le seul fait des deux hormones étudiées ici.
Lors d'un exercice bref c'est l'adrénaline qui est l'hormone
principalement sécrétée. Les commandes
sécrétoires d'insuline et de glucagon sont
principalement nerveuses.

Un schéma des acteurs principaux (au programme de
1èreS) de la fonction d'homéostase
nutritionnelle ou énergétique liée au
glucose.
|
Annexe
Pour ceux qui souhaiteraient aller un peu
plus loin et établir une relation entre connaissances
scolaires et ce que l'on peut trouver sur internet où
dans des ouvrages de nutrition ou même de
vulgarisation...
http://www.ladocfrancaise.gouv.fr/brp/notices/044000493.shtml
(à
télécharger: le rapport Glucides et
santé : État des lieux, évaluation et
recommandations, AFSSA (Agence Française de
Sécurité Sanitaire des Aliments, octobre
2004); notamment ch 8, p 48 et annexe 4 : "index
glycémique", p 136).
Le glucose est absorbé sélectivement
et activement (son absorption par les entérocytes
consomme de l'énergie et peut atteindre une limite
maximale) alors que le fructose est absorbé
moins vite et à peu près proportionnellement
à sa concentration dans la lumière
intestinale. Pour de faibles quantités, le fructose
est converti en glucose par les entérocytes mais pour
de grandes quantités le fructose passe dans le sang
et c'est dans le foie qu'il est transformé rapidement
en glucose. Cependant la totalité du fructose peut ne
pas être absorbée, et il peut donc être
rejeté avec les excréments, ce qui n'arrive
jamais pour le glucose. Le saccharose est
hydrolysé en fructose et en glucose dans la
lumière intestinale avant son absorption. Le glucose
qui en résulte est absorbé encore plus
rapidement que du glucose ingéré seul.
On utilise maintenant un indice appelé index
glycémique pour évaluer la vitesse
d'absorption d'un sucre (ou d'un aliment sucré) et la
réponse glycémique de l'organisme.
|
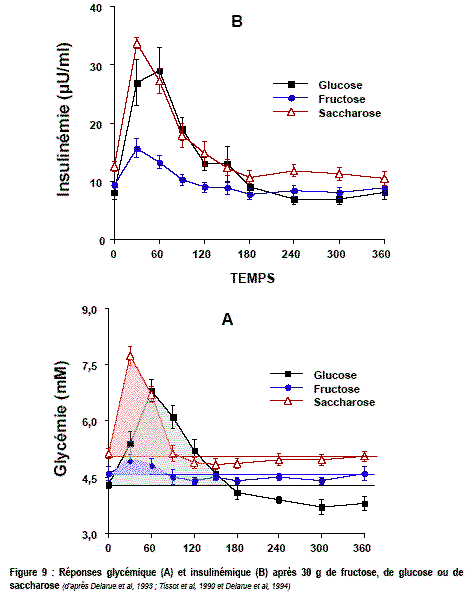
(in rapport cité ci-dessus,
modifié)
|
L'index glycémique le plus utilisé est
IGglucose qui est le rapport
entre les aires d'hyperglycémie (fig.9 A)
observées pour un sucre, à la suite de
l'ingestion d'une quantité fixe de ce sucre (50g
habituellement), et celle du glucose
(en grisé ici),
multiplié par 100. On utilise aussi
la référence au pain de mie blanc soit
IGpain. (Voir l'annexe de la
référence de l'AFSSA pour les protocoles
expérimentaux : quantité, durée et lieu
des prélèvements sanguins (toutes les 30
min...), nombre de sujets...).
|
glucides ou aliments glucidiques
|
IGglucose
(glucose = 100)
|
|
fructose
|
19 ± 2
|
|
saccharose (glucose + fructose)
|
68 ± 5
|
|
baguette
|
95 ± 15
|
|
purée de pomme de terre
instantanée
|
85 ± 3
|
|
Cornflakes, Kellogg's
|
81 ± 3
|
|
pain de mie blanc
|
70 ± 0
|
|
riz blanc
|
64 ±7
|
|
Coca-Cola
|
58 ± 5
|
|
spaghetti
|
44 ± 3
|
|
pomme
|
38 ± 2
|
Le fructose ne provoque qu'une faible augmentation de la
glycémie car sa présence dans la sang
résulte principalement de sa transformation par le
foie (la "fructosémie" maximale au niveau de
la veine porte lors des tests (50g d'absorption de fructose
ou de saccharose) ne dépasse pas non plus 2,2 mM, ce
qui est une valeur faible). Il est en plus très
facilement utilisé par les cellules du foie, du rein
et de l'intestin.
Le saccharose provoque une rapide mais fugace
hyperglycémie du fait de l'absorption très
rapide du glucose produit par hydrolyse du saccharose dans
l'intestin.
Le métabolisme du fructose est quasiment
indépendant de l'insuline dont la
sécrétion suit la glycémie. L'insuline
joue un rôle plus important dans le cas du saccharose
étant donné l'élévation rapide
de la glycémie.
|
4.2.4 Les diabètes: des
hyperglycémies chroniques aux sources diverses
Une source bien utile qui
complète et met à jour l'article paru dans l'APBG :
dont voici l'adresse sans les frames, tellement gênantes:
http://hometown.aol.com/_ht_a/drfatalis/Pages/diabetes.html
pour laquelle certaines images ne sont pas accessibles (n'existent
pas dans les répertoires spécifiés)
Les diabètes (sucrés) sont des
maladies multifactorielles avec une forte composante
héréditaire dont le trait commun est une
hyperglycémie chronique avec des symptômes
pas toujours bien nets (et même parfois inexistants): soif
intense, diurèse (quantité d'urine produite et
rejetée) importante, perte de poids et trouble de la
conscience aboutissant à un coma mortel (définition de
l'OMS de 1985 citée approximativement).
Étant donné l'unicité du système
hypoglycémiant on peut dire que les diabètes, en tant
qu'hyperglycémie, résultent d'abord d'un
dérèglement du système hypoglycémiant et
donc de la synthèse, de la libération par les cellules
endocrines, du transport, du mode d'action, ou de la
sensibilité des cellules cibles .... à
l'insuline. Ainsi on distingue deux types principaux
(sur 5) de diabètes selon la
quantité d'insuline sécrétée:
* les diabètes insulino-dépendants (DID)
ou de type I pour lesquels la sécrétion
d'insuline est très faible ou nulle mais dont le
symptôme principal (hyperglycémie) peut être
corrigé par des injections d'insuline;
* les diabètes non insulino-dépendants
(DNID) ou de type II qui représentent 90% des
diabètes diagnostiqués en France et pour lesquels la
sécrétion d'insuline est faible et l'injection
d'insuline inefficace à faire baisser la glycémie.
L'hyperglycémie a des conséquences graves:
- elle accroît la viscosité sanguine et endommage les
vaisseaux (angiopathie touchant d'une part les petits vaisseaux
pancréatiques, rénaux ou cardiaques et pouvant conduire
à la cécité et d'autre part les gros vaisseaux
conduisant à une athérosclérose (3/5 des
diabétiques meurent de maladies cardio-vasculaires)
- elle perturbe les sécrétions pancréatiques
puisque les cellules endocrines pancréatiques (alpha et
ß) sont directement sensibles à la glycémie
- elle conduit à des modifications chimiques de certaines
molécules circulantes comme l'hémoglobine qui fixe le
glucose et perd une partie de son activité (elle est
glycosylée).
Le diabète de type I est assez bien compris. On le
considère comme une maladie auto-immune dans
laquelle le système immunitaire du malade fabrique des
anticorps dirigés contre ses propres cellules ß
productrices d'insuline et les détruit totalement en absence
de traitement par injection d'insuline (qui peut préserver
ainsi une bonne partie des cellules ß). Les
mécanismes d'action des anticorps contre les cellules sont
assez complexes et variés: certains anticorps sont
dirigés contre l'insuline, d'autres contre des
éléments membranaires (récepteurs notamment),
d'autres encore activent des systèmes lytiques du
complément, enfin, les plus toxiques activent des cellules
cytotoxiques (mécanisme dit ADCC)... De nombreux
gènes, notamment du complexe majeur
d'histocompatibilité (CMH), présentent une
liaison statistique avec la maladie (la
fréquence allèlique (probabilité qu'un individu
d'une population présente un allèle; cette
fréquence est estimée à partir du % d'individus
possédant tel allèle dans une population
testée... voir cours de
spécialité de TS) est plus forte dans la
population diabétique que dans la population standard); on les
qualifie souvent de gènes de
prédisposition. Aucun cas de causalité directe,
avec un déterminisme précis, démontré
expérimentalement, n'a été mis en
évidence, à ma connaissance.
Le diabète de type II est mal compris. Trois
éléments principaux semblent caractériser ce
type de diabète:
- une insulinorésistance des tissus
périphériques, particulièrement des tissus
musculaires squelettiques (la glycémie reste
élevée même lorsque l'on élève
l'insulinémie)
- une perturbation de la sécrétion d'insuline qui est
faible (en absence de traitement)
- une synthèse de glucose exagérée.
Deux grandes interprétations sont actuellement
proposées: l'une privilégiant le rôle des
cellules ß et l'autre privilégiant
l'insulinorésistance en accord avec les résultats
obtenus à partir de modèles animaux (animaux (rats,
hamster, souris, lapins) chez qui on cherche à provoquer ou
que l'on sélectionne comme présentant des
symptômes voisins de la maladie humaine
étudiée).
On distingue trois phases d'installation d'un
diabète de type II: une intolérance au glucose (une
glycémie comprise entre 1,10 et 1,26 g.L-1
après 8 heures de jeune), le diabète de type II (si la
glycémie à jeun est supérieure à 1,26
g.L-1, ce qui correspond à 25% des cas
précédents), et enfin le stade des complications
dégénératives avec les atteintes aux vaisseaux
(on peut alors être amené à traiter le malade par
des injections d'insuline).
De nombreux gènes de prédisposition sont
étudiés.
Annexes
Paraboles et catastrophes,
René THOM, 1983, Flammarion (col. Champs)p 64
« Le monde extérieur, ne l'oublions pas, se
présente à nos yeux comme un mélange de
déterminisme et d'indéterminisme. En toute
circonstance, il convient de distinguer, comme le dit Epictète
dans son Manuel (note 5), ce qui « dépend de nous »
( ta eph hemin) et « ce qui ne dépend pas de nous
» ( ta ouk eph hemin). Importante d'un point de vue
éthique, cette distinction ne l'est pas moins pour la science.
Eh bien, la pensée mathématique a, pour ainsi dire,
poussé à l'extrême cette distinction: la variable
est ce qui dépend de nous, l'argument de la fonction... Ce qui
ne dépend pas de nous, c'est le déterminisme rigide
qui, après avoir assigné une fois pour toutes une
valeur donnée à la variable, détermine la valeur
correspondante de la fonction...
C'est une idée qui a eu beaucoup de poids dans le
développement de la tradition scientifique.
Je crois qu'en fait, à l'origine de la
révolution galiléenne, il y a simplement le fait que
l'esprit scientifique a été en mesure de
modéliser, justement à l'aide de la notion de
fonction, un certain nombre de phénomènes qui,
jusqu'alors, n'étaient pas modélisables d'une
manière suffisamment fidèle. De ce point de vue,
selon moi, deux facteurs ont agi conjointement : d'un
côté, une série de nécessités
pratiques, je pense principalement à l'artillerie amenant
à l'étude de la trajectoire des boulets de canon, des
projectiles et donc du mouvement des corps graves; de l'autre, la
notion de fonction qui commençait à poindre dans
l'esprit des chercheurs, leur permettant ainsi de décrire avec
exactitude et fidélité cette même trajectoire
d'un corps lourd. Je pense donc que la formation de cette image de
fonction - et il convient de dire image car fonction est ici
plus une image qu'un concept - est à l'origine de la grande
révolution scientifique galiléenne.
C'est grâce à la notion - même vague - de
fonction que l'on devient capable de modéliser la chute des
corps et la réfraction des rayons lumineux. Une fois les lois
connues, on peut construire les instruments exploités par ces
lois. Galilée a donc construit sa «lunette» et
quelque temps après un premier microscope...
Ces instruments réalisés, on a bien sûr
commencé à s'en servir. Galilée a observé
les astres, Malpighi les tissus de l'être vivant... Ainsi
naquit la science expérimentale. Mais l'importance
attribuée à l'expérience n'a pas
été la cause du progrès scientifique, elle en a
été l'effet. Elle a été l'effet de la
maturation dans l'esprit de la communauté scientifique de
cette structure théorique qu'est la notion de fonction.
La notion de fonction est apparue assez tard sur la scène
de la science, tout au moins sous une forme achevée. C'est une
notion pratiquement inconnue des mathématiques anciennes et
qui a fait une timide apparition uniquement avec l'algèbre
arabe qui, traitant des équations linéaires, a
introduit, dans une certaine mesure, la notion de fonction
linéaire. Au XVIe siècle, lorsque les
algébristes italiens ont commencé à
étudier les polynômes et les équations
algébriques du degré supérieur, on a
effectivement ressenti qu'il fallait une théorie de ces
fonctions particulières. Newton lui-même, en
décrivant le mouvement des corps, ne connaissait pas la
fonction, si ce n'est dans des cas particuliers où la variable
était le temps. Elle n'apparaît qu'avec Leibniz,
à qui l'on doit en fait les définitions
générales des notions de variable, d'argument d'une
fonction et également de paramètre (note 6).
Cela démontre clairement que l'on a tort de sous-estimer le
rôle de l'imagination dans le développement des
sciences. A l'inverse, j'estime que tous les progrès de la
science, au moins les progrès décisifs, sont toujours
liés à de meilleures possibilités de
modélisation, à une plus grande capacité de
simulation interne des phénomènes.
Donc, encore une fois, nous sommes en compagnie de Platon : les
idées ( les structures mathématiques)
précèdent les choses...
Bien sûr, et dans ce sens on peut reprendre tout ce qui a
déjà été dit plus haut pour la physique :
en général, les structures mathématiques ont
précédé leur utilisation en physique, et non
l'inverse. De la même manière, je crois que même
en biologie ce sont les structures mathématiques qui
ordonneront les phénomènes les plus importants. Par
exemple, les phénomènes de régulation exigent un
grand nombre de paramètres et, par conséquent, toute
description un peu affinée de ces phénomènes
nécessitera l'utilisation d'espaces pluridimensionnels. Croire
que l'on pourra donner une théorie de la régulation
tout simplement en manipulant des diagrammes cybernétiques
avec des sommets et des flèches est illusoire, selon moi.
L'importance de la régulation consistera toujours dans le fait
qu'il s'agit d'un phénomène à caractère
fondamentalement continu ; il faudra donc associer des figures
multidimensionnelles à ces situations. Dans ce cas, la
théorie des catastrophes pourra être très utile
justement parce qu'elle vise à interpréter les nuages
de points recueillis expérimentalement, au moyen de
constructions mathématiques qui seraient à la fois les
plus simples et les plus robustes et, ainsi, qui satisferaient la
propriété de stabilité structurelle tout en
résistant à de petites perturbations dues au milieu ou
aux erreurs expérimentales.
Toute la « philosophie » de la théorie des
catastrophes, son schéma général, tient
justement à ceci : il s'agit d'une théorie
herméneutique qui s'efforce, face à n'importe quelle
donnée expérimentale, de construire l'objet
mathématique le plus simple qui puisse l'engendrer. De ce
point de vue, il est clair que la théorie des catastrophes ne
coïncide pas, comme on a tendance à le penser, avec la
liste des sept catastrophes élémentaires; ce faisant,
on réduit en fait la théorie des catastrophes tout
entière à ce que moi j'appelle la théorie des
catastrophes élémentaires.»
note 5. Epictéte, philosophe stoïcien,
né à Hiérapolis de Phrygie vers l'an 50. Esclave
à Rome, il fut affranchi par Néron. Mal vu par
Domitien, il fut frappé par le décret d'exil
promulgué par le Sénat en 94 après J.-C.
S'étant établi à Nicopolis en Epire, il y
mourut, probablement au début du règne d'Hadrien. Ses
doctrines nous sont parvenues grâce à son disciple
Arrien, auteur de : Vie et mort d'Epictéte, de huit
livres d'Entretiens sur Epictéte et sa philosophie, et
également de l'Enrichidion ( ou Manuel) qui
résument ces livres.
note 6. Le mot « fonction » fut
employé par Leibniz dans un manuscrit de 1684 pour indiquer
toute quantité qui varierait d'un point à un autre
d'une courbe: par exemple, la longueur de la tangente, etc. C'est
encore Leibniz qui introduisit les termes
«constante», « variable» et enfin
«paramètre», ce dernier ayant
été employé dans le développement d'une
famille de courbes. (Cf. M. Kline, Mathematical Thought from
Ancient to Modern Times, New York, Oxford University Press, 1972,
p. 339-340.)
retour texte
Remarques sur la partie 1
* Ce cours s'inscrit dans la même veine
didactique que l'ancien chapitre de spécialité de TS
sur la pression
artérielle mais étant
donné le changement de niveau (passage de terminale à
1ère), des ajustements nécessaires devront être
repris petit à petit. Des éléments concernant
les systèmes de communication de l'organisme sont aussi repris
de l'ancien cours de seconde (communication
et organisation chez les animaux)
et de TS: physiologie
animale et humaine et
neurophysiologie.
Le système nerveux et son fonctionnement formant un ensemble
homogène il me paraît judicieux de le traiter avant
l'étude de la glycémie qui est un paramètre
physiologique qui fait intervenir de nombreuses populations
cellulaires dans un système complexe de contrôle.
De plus cette partie nous permettra de revoir des populations
cellulaires, animales cette fois, au cours du développement,
et de les comparer avec les populations de cellules des plantes
abordées dans le chapitre
précédent.
*
Le programme nous
demande de traiter un exemple de fonctionnement
intégré: les circuits neuroniques impliqués dans
un réflexe myotatique simple. C'est un bon exemple d'un
sensibilité intéroceptive, d'un contrôle rapide
(involontaire) de la contraction musculaire, qui met en jeu des
populations de neurones bien identifiées et un message nerveux
ionique et chimique spécifique de ces
populations.
Une seconde partie, plus
originale mais difficile à définir (surtout du fait de
la maladresse de la formulation qui nous parle de phénotype
à tout bout de champ), nous demande de nous intéresser
aux centres nerveux (cortex sensoriel) et au fonctionnement de
populations plus variées avec un nombre de messagers
très important, notamment du fait de la fonction endocrine du
cerveau. Si j'ai bien compris cette partie, le programme souhaite en
fait nous voir aborder la question de la
neuroplasticité et non de
l'hérédité ou de l'évolution des
comportements. Selon les termes du document d'accompagnement: la
neuroplasticité est un "concept indispensable pour
comprendre la part de l'expérience individuelle
complétant la part du génotype dans le fonctionnement
du système nerveux". Or la neuroplasticité
désigne habituellement la facilité d'un organisme
à modeler l'organisation de son système nerveux,
à l'état adulte ou au cours de sa maturation. En plus
des facultés de régénération cellulaire,
limitées, la neuroplasticité serait due à la
présence de cellules souches. Cependant,
des progrès récents de la neurochimie tendent à
définir une neuroplasticité
moléculaire (qualifiée de
transcriptionnelle), qui nous rapproche de la
liaison génotype-phénotype, que l'on voudrait à
nouveau nous voir traiter en caricaturant l'inné au
génotype et l'acquis au phénotype
(voir à ce sujet
l'intéressant travail de Philippe Mathy: Modélisation
génétique et influence du milieu: quelques outils
didactiques pour les cours de génétique du secondaire,
Philippe Mathy et al., Compte rendu du séminaire EMSTES
2000-2001(Courrier du Cethes, n° 48-49, sept. 2001, disponible
sur internet à l'adresse: http://www.fundp.ac.be/cethes/CourrierduCethes/sept2001.pdf).
Je pense que derrière cette maladresse se cache le souhait
de faire comprendre aux élèves que, malgré le
fait que le système nerveux soit un système
"câblé", histologiquement
rigide, il est bien un
système vivant, en
perpétuel remaniement. En tout cas c'est comme cela que je
le présenterai.
* une source
hétérogène pour la partie sur la
neuroplasticité: www.inrp.fr/Acces/biotic/neuro/plasticite/html/points.htm;
des éléments de formation continue (synthèse
d'articles) sans les bases qu'il faudra trouver ailleurs
(bibliographie du site et encyclopedia universalis par
exemple); je me permets
d'ajouter que lorsque les notions qu'un programme scolaire souhaite
voir enseignées sont tellement inadaptées au niveau des
élèves (et des enseignants) - et à leurs
interrogations- qu'il faut joindre un pseudo-cours sur un site du
ministère, il est légitime de se poser des questions
sur sa pertinence. La formulation du programme est une
honte ; je précise bien que ce n'est pas le
thème de la neuroplasticité qui est en soi
inadapté car tout thème biologique est passionnant,
mais bien le bagage qu'il demande pour être traité
convenablement, ce qui n'est peut-être pas le problème
des concepteurs du programme. Le système nerveux central reste
une des parties les plus complexes de la physiologie et des moins
enseignées pour les concours de l'enseignement.
retour début de page











