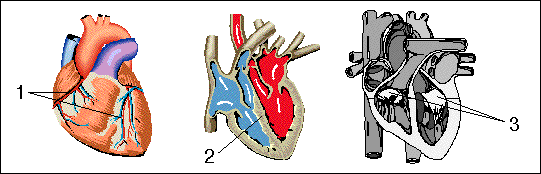
Chaque représentation met l'accent sur un point : lequel ?
(1. l'irrigation coronaire - 2. le cloisonnement cœur droit-coeur gauche - 3. les valvules anti-retour, essentielles pour une pompe volumétrique...)
Les trois principaux ouvrages utilisés pour cette partie
sont :
1 - L'organisme dans son milieu (précis
de zoologie fonctionnelle), Yves TURQUIER, Doin, Tome 2: l'organisme
en équilibre avec son milieu, 1994,
2 - Physiologie animale; adaptation et milieux de
vie, Knut SCHMIDT-NIELSEN, Dunod, 1998
3 - Précis de physiologie, de A. Calas,
J.-F. Perrin, C. Plas et P. Vanneste, publié en 1997 chez
Doin .
Contrairement à ce qui est exprimé dans le programme, la notion de régulation ne pouvant, à mon sens, être vue à partir de l'étude des sécrétions des hormones sexuelles, du fait de la complexité des mécanismes (voir cours), cette partie forme un ensemble relativement à part, même si on y retrouve des notions parfois déjà abordées dans d'autres parties.
Quelle ne fut pas ma surprise de découvrir que le verbe "réguler" n'est pas dans l'édition 1985 du Petit Robert (il se trouve dans d'autres dictionnaires) : on trouve régulation (contrôle, ajustement), régler (maintenir l'équilibre physiologique, en fait ajuster par rapport à une règle, ou mieux par rapport à un état de bon fonctionnement). En anglais le verbe to regulate existe et signifie "contrôler, ajuster".
* Que signifie la régulation d'une fonction ?
Dans un système non vivant, on règle, on
contrôle, on ajuste un paramètre.
Dans un système vivant on règle, on
contrôle, on ajuste, on adapte une fonction.
Dans ce sens la pression artérielle
n'est pas une fonction, ce n'est qu'un paramètre, il n'y a
donc pas de contrôle du paramètre en tant que tel mais
bien un contrôle de la fonction qui peut être la
locomotion (effort) par exemple ou la défense de l'organisme
(lors d'une hémorragie...). Si l'on va plus loin il est
important de souligner combien le fait d'imaginer que l'organisme a
besoin de connaître la valeur de tel ou tel paramètre et
de l'ajuster à une valeur de référence, fait
partie d'une vision mécaniciste du vivant. La demande
en oxygène d'un tissu par exemple à la suite de la
commande volontaire d'un effort physique, CAUSE un déficit
local qui est comblé par toute une série de
mécanismes. Il n'y a là-dedans aucun
présupposé de paramètre stable modifié
pendant l'effort. C'est la vie qui cause les modifications et
l'organisme qui contrôle dans le sens où il participe
lui aussi à la vie...
Le terme ne peut donc être employé en biologie que par
analogie avec un système physico-chimique (on est donc dans le
domaine des modèles) . Régler c'est ajuster un
paramètre variable de façon à le maintenir au
niveau souhaité. Le niveau souhaité est un
équilibre, une harmonie de fonctionnement, au sein de
l'organisme et entre l'organisme et son milieu. On retrouve les deux
aspects de toute étude physiologique : équilibre
interne d'une part, une sorte d'auto-fonctionnement, sous la
dépendance de déterminismes plus ou moins souples, et
adaptation de l'organisme à son milieu d'autre part, qui est
équilibre externe, déterminé par sa
capacité de réponse aux conditions de l'environnement,
aux événements parfois brusques...
Le terme d'équilibre est assez riche, analogiquement,
car il suppose implicitement que toute variation dans un sens est
compensée par une variation dans le sens opposé. On
peut donc utiliser équilibre dynamique. Mais bien
sûr, c'est une manière de voir l'être vivant et ce
n'est pas la seule. On parle souvent d'homéostasie : ce
qui suppe que l'on maintient les paramètres du milieu
intérieur autour d'une valeur fixe, constante (le point de
consigne). Ce terme masque les variations physiologiques normales
(liées à l'activité, à un état
métabolique particulier...). Peut-être serait-il donc
souhaitable de lui préférer un terme moins statique
comme le terme d'équilibre dynamique. (Le terme d'ajuster fait
lui aussi référence à une valeur constante. Par
contre le terme de contrôle est à mon avis un peu
trop vague même s'il convient à la fois pour
désigner des mécanismes de commande centralisés
et des systèmes de contrôle entièrement
automatiques : on pourrait donc cependant l'employer pour
désigner les mécanismes alors que le terme
d'équilibre ferait référence à la
théorie).
On progresse : la régulation de la pression
artérielle est donc l'ajustement de ce paramètre
physiologique afin de le maintenir dans un état
d'équilibre dynamique interne et externe.
* Mais pourquoi régler ? Au nom de quelle règle ? Y
a-t-il une règle ?, une norme ?
On suppose habituellement que la vie nécessite des conditions
physico-chimiques propices dont les limites sont connues par
l'organisme qui s'efforce de s'y maintenir. Il y a donc une
finalité (que l'on nomme aussi instinct : l'instinct de
survie). La vie s'efforce de survivre (cette formulation n'est
pas très heureuse et je lui préfère "la vie se
donne" qui a aussi de nombreux autres sens). Cette orientation
à la vie (encore une formule pas vraiment extraordinaire) est
une des caractéristiques essentielles du vivant qui repose sur
les trois aspects du travail du vivant : travail de nutrition,
travail de reproduction et travail de relation. Il est évident
que cette finalité reste vague dans sa définition alors
qu'elle est très concrète dans ses expressions. Il me
paraît juste nécessaire pour le biologiste d'y faire
référence comme une donnée
d'évidence.
*Qui règle ?
La réponse à cette question est contenue dans celle
à la question précédente. La vie contient en
elle ses propres règles, c'est l'organisme vivant qui vit,
qui s'adapte, qui survit.
On débouche sur la question de l'adaptation de l'organisme
à son milieu.
- Premier point incontournable : l'organisme fait partie du milieu,
il y a donc un équilibre dynamique entre l'organisme et son
milieu. Considérer uniquement le milieu en termes de
contraintes (la contrainte pourrait être définie
par exemple comme une règle obligatoire) est inadéquat,
tout comme supposer que le milieu n'est qu'un ensemble
extérieur de conditions physico-chimiques qui n'influencent
pas l'organisme (l'organisme modifie le milieu et le milieu
modèle l'individu...). Les termes d'équilibre dynamique
me semblent encore une fois appropriés alors que l'idée
de sélection naturelle masque à mon avis tout un
aspect des relations entre les organismes entre eux et entre le
milieu et l'organisme qui sont loin d'être toujours des
contraintes mais bien souvent des stimulations. Comme souvent, il
s'agit d'une question de point de vue : un individu qui
réussit profite-il de conditions favorables ou bien est-ce lui
qui modifie ces conditions pour qu'elles lui soient favorables, ou
est-ce lui qui s'adapte... ? L'adaptation des organismes au milieu
est un fait, le décrire en termes d'équilibre dynamique
me semble être le choix le plus judicieux.
- Deuxième aspect : si l'on considère l'adaptation dans
le temps, l'évolution du vivant est le résultat du
travail du vivant. L'actuelle diversité est l'état
de l'équilibre global à un instant donné :
l'instant présent. Et si l'on accepte l'actualisme comme un
principe utilisable, les mécanismes actuellement en jeu dans
l'équilibre du vivant sont les mêmes que par le
passé : les mécanismes de l'évolution sont les
mécanismes du vivant (voir cours d'enseignement commun :
évolution). Dire que l'actuel
équilibre résulte d'un déséquilibre par
le passé est pure supposition qui bien évidemment ne
peut pas être prouvée. L'actualisme propose au contraire
une "stabilité" (au sens dynamique), une continuité des
mécanismes.
* Qu'étudie donc le physiologiste ?
Le physiologiste, après avoir clairement défini son
véritable domaine d'investigation : celui du travail du
vivant, décrit par des équilibres dynamiques, s'efforce
d'élaborer des modèles à partir de ses
observations, modèles qu'il teste ensuite par des
expériences : on s'inscrit ici directement dans une
démarche expérimentale. Le physiologiste en arrive
ainsi à présenter une théorie du
contrôle ou plutôt une théorie de
l'équilibre. De tels modèles sont analogiques mais
fort utiles, ils permettent de cerner les problèmes. Si je
reprends ce que j'ai proposé dans la page sur la méthode
on peut dire que l'on distingue alors les modèles
internes (qualifiés de "réels" car ils s'efforcent
de décrire le comportement des systèmes réels
c'est-à-dire naturels pour ce qui nous intéresse) et
les modèles externes (qui s'efforcent de décrire
le "comportement" des observations, c'est-à-dire de notre
connaissance, ce sont des modèles logiques). Cette
idée vient de l'article de Jacques OKSMAN : Mesures et
information, Pour la Science, 258, avril 1999, 90-95, et je la trouve
tout à fait applicable à notre problème (voir
aussi une petite page sur les modèles).
C'est donc ainsi que je vais présenter ce cours en proposant
un modèle logique (classique) et un modèle interne (un
peu plus original).
|
L'unité de pression internationale (adoptée par la 1ème conférence générale des poids et mesures en 1971) est le pascal (Pa). Une unité tolérée est le millimètre de mercure (mm d'Hg) ou Torr avec 1 Torr = 1 mm d'Hg = 133,3 Pa. Les atmosphères et le bars ne sont plus acceptées. La pression atmosphérique de nos laboratoires (1 atmosphère) à de faibles altitudes est d'environ 101,3 kPa. |
Le cœur est une pompe volumétrique automatique
à fibres musculaires striées mais dont le
fonctionnement est complexe et n'entre pas dans le cadre de ce cours
: on peut juste préciser que la contraction des fibres
striées cardiaques fait intervenir le tissu nodal (à
l'origine des contractions autonomes à un rythme plus
élevé que le rythme du cœur en place : de l'ordre
de 100 battements par minute), des jonctions serrées
très étroites entre les cellules de forme très
particulière (en Y) qui permettent une contraction
homogène et rapide du muscle, la présence de lames de
collagène et d'autres éléments conjonctifs qui
compartimentent le muscle cardiaque et assurent une contraction
légèrement décalée entre les deux
oreillettes et d'un bloc et de façon "vrillée" pour les
ventricules (expulsion de la quasi totalité du sang emplissant
les ventricules). On notera aussi le mécanisme de remplissage
dont on peut avoir une bonne idée à partir d'une courbe
de pression intracardiaque (voir par exemple Précis de
physiologie, doin, p 14 et s). L'irrigation du cœur (le
cœur est un muscle qui consomme beaucoup de dioxygène)
par les artères coronaires a lieu essentiellement pendant la
phase de diastole et est sous l'étroite dépendance de
la vasodilatation des artères coronaires.
Etant donné le programme, on peut résumer (de
façon simpliste) le cœur à son aspect de pompe
(muscle strié irrigué et innervé)
présentant deux états : un état de
relâchement (la diastole), pendant lequel
le cœur se remplit par retour veineux, et un état de
contraction (la systole) ou d'éjection
systolique pendant lequel un certain volume de sang (ondée
systolique) est projeté dans les artères.

La pompe cardiaque n'est pas la seule pompe présente sur le
réseau circulatoire.
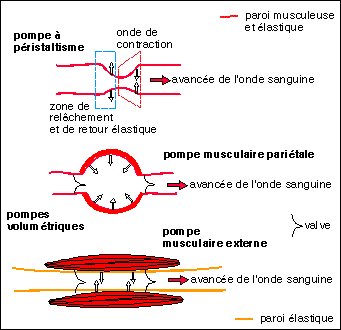
D'une part, la présence de valves (clapets anti-retour) sur tout le trajet veineux montre l'importance de l'exercice physique chez l'homme pour assurer un bon retour du sang veineux au cœur (mouvements respiratoires notamment du fait de la dépression intrathoracique à l'inspiration qui abaisse la pression de retour veineux et donc augmente le volume d'éjection systolique.... les profondes inspirations-expiratoins recommandées avant la plongée en sont une illustration ; ou encore la marche pendant laquelle les contractions des muscles striés squelettiques fournissent une énergie non négligeable à la pompe musculaire veineuse). (Le raisonnement est aussi valable pour les vaisseaux lymphatiques dont le drainage se fait par le même principe). D'autre part la musculation des artérioles mais aussi des artères, même s'il elle est proportionnellement moindre, montre la part que peut prendre le péristaltisme dans la dynamique circulatoire, même si elle est difficile à évaluer.
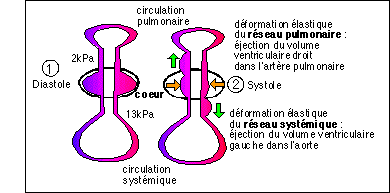
La circulation pulmonaire a une résistance faible ,
la pression sanguine y est peu élevée (2kPa au niveau
de la sortie du cœur) et la paroi des artères assez
mince. Le volume sanguin de la circulation pulmonaire
représente 10 à 12% du volume sanguin total et semble
peu sujet à variation. En section transversale les
artères pulmonaires apparaissent ovales et ne deviennent
circulaires que lors du passage de l'ondée sanguine. La
déformation élastique de la paroi expliquerait pour une
bonne part l'amortissement de l'écoulement par saccades du
sang venant du cœur, ce qui permettrait une perfusion continue
des capillaires pulmonaires (en fait il semble que la pulsation de
pression soit très amortie mais pas la pulsation de
débit). Ne pas oublier que le poumon est une surface
d'échange. Le sang est filtré au niveau des capillaires
pulmonaires. L'excédent de liquide interstitiel
représente environ 0,5 L par jour et est repris par les
vaisseaux lymphatiques.
La circulation systémique comprend 4 parties :
* le réseau artériel (de l'aorte aux
artérioles) : réseau ramifié où, du point
de vue histologique, c'est la composante élastique qui
domine (faible innervation et faible musculation). La pression
moyenne y est maintenue étroitement autour de 12,5 kPa. Le
débit y est pulsatif (variations dans l'aorte : 9-15 kPa, dans
l'artère radiale : 8-18 kPa pour des vitesses oscillant
respectivement entre -10-120 cm/s et -2-30 cm/s, les valeurs
négatives correspondant au reflux de l'ondée sanguine).
La résistance à l'écoulement y est faible et la
vitesse élevée). Le volume sanguin contenu dans le
réseau artériel est très faible par rapport au
volume sanguin veineux. Le pouls est une onde de pression qui
se propage très rapidement (10 à 40 m/s et donc
beaucoup plus vite que l'ondée sanguine...) depuis le
cœur vers la périphérie.
* le réseau artériolaire (diamètre
compris entre 10 et 100 µm) dit "résistif" car il est
caractérisé par une capacité à modifier
son diamètre (et donc la résistance à
l'écoulement) d'une part par la contraction des fibres lisses
de la paroi des artérioles, richement innervées
(vasomotricité = vasoconstriction/vasodilatation), et
d'autre part par la présence de très nombreux
sphincters (petits muscles lisses circulaires à
commande nerveuse individualisée) situés juste avant
les capillaires. Il semble que ce soit réellement le
système de contrôle de l'irrigation des organes : on
pourrait donc plutôt le qualifier d'adaptatif et non de
résistif.
* le réseau capillaire, extrêmement
ramifié, très résistif mais peu
contrôlable (peu adaptable), la paroi des capillaires
étant quasiment limitée à l'endothélium
vasculaire, son rôle essentiel semble bien être d'assurer
les échanges entre le sang et le liquide interstitiel,
véritable milieu intérieur où vivent les
cellules. La vitesse d'écoulement du sang y est très
faible (de l'ordre de quelques mm/s) et la pression minimale.
* le réseau veineux, considéré comme
passif dans le sens où la paroi veineuse n'est
quasiment pas musclée (par contre sa composante
élastique est essentielle) mais étant donné la
présence de valvules et le principe des pompes externes (voir
plus haut), le retour veineux au cœur se fait de façon
active, même si la pression y est minimale. La
résistance à l'écoulement y est
considérée comme faible, les variations du volume
veineux, importantes, se suivies par des modifications
élastiques du volume des veines sans augmentation de pression
(qui reste voisine de 1,4 à 0,7 kPa par exemple à
l'extrémité veineuse des capillaires pour un homme
allongé). Le sang veineux représente la très
grande majorité du volume sanguin total estimé à
environ 70% (dans un cadavre, tout le sang se retrouve dans les
veines, les artères sont vides).

|
dans les différentes parties du système vasculaire de l'homme (1 mm d'Hg = 0,13 kPa) in Schmidt-Nielsen, fig 3.11 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Deux remarques essentielles doivent être faites si l'on considère l'appareil circulatoire clos des vertébrés à double circulation présentant un cœur cloisonné (séparé en deux moitiés), comme c'est le cas de l'homme et de la plupart des vertébrés :
2.1 Paramètres liquidiens :volume, composition (liquides, solutés, gaz, cellules...), température...
Le sang n'est qu'un des liquides circulants de l'homme et représente entre 5 et 10 % de la masse du corps, selon les estimations. Le volume sanguin (volémie) de l'homme est de l'ordre de 5 L mais peut varier de quelques dizaines de % de cette valeur en fonction de l'état physiologique, soit par augmentation de la masse totale (par exemple pendant une grossesse), soit par augmentation de la masse des cellules sanguines (par exemple hématies stockées par la rate), soit par augmentation des liquides (par exemple réabsorption rénale ou au niveau du colon augmentée). La teneur en eau d'un vertébré est de l'ordre des deux tiers de la masse totale mais il y a de grandes variations, notamment en fonction de la teneur en graisses (le tissu adipeux ne contient que peu d'eau : 10% en masse ; et donc, plus un individu est gras, moins il possède d'eau); si on se réfère au pourcentage "hors graisse" on trouve des chiffres plus homogènes, approximativement:
|
|
|
|
|
|
||
|
eau intracellulaire : 45% |
||
|
|
||
Les variations de la volémie sont difficilement
séparables des variations de composition chimique ou
cellulaire du sang étant donné le lien entre tous ces
paramètres. On peut tout de même considérer trois
facteurs qui jouent directement sur la volémie:
* la teneur en eau du sang (équilibre hydrique) qui
dépend de la quantité d'eau filtrée et
réabsorbée aux niveaux des capillaires (ce n'est pas
toujours évident et il me semble nécessaire de rappeler
que c'est bien au niveau de capillaires que vont se faire les
échanges d'eau, d'ions ou d'autres solutés)
* l'équilibre minéral (Na+ et K+ qui
interviennent de par exemple dans les phénomènes
d'excitabilité cellulaire...mais aussi le Ca2+, essentiel pour
le squelette minéralisé de l'homme)
* l'équilibre acido-basique (acidose, alcalose) car le
sang présente un pH compris entre 7,35 et 7,45...
Comme il est impossible dans le temps qui nous est imparti de traiter
ces questions, nous ne ferons que les effleurer...
|
|
|
|
glandes salivaires |
la salive représente 0,8 à 1,5 L/jour (98% d'eau) et comprend des produits toxiques comme des métaux lourds, de l'acide urique ou des alcaloïdes... |
|
estomac |
le suc gastrique représente 1 à 1,5 L par repas |
|
foie |
la bile représente 0,7 L par jour |
|
intestin |
les selles contiennent environ 75% d'eau pour une masse
de 100 à 250g par jour pour un adulte |
|
poumons |
les poumons excrétent une quantité d'eau très variable en fonction de la ventilation, l'humidité de l'air et surtout la température de l'air (les poumons de certains mammifères désertiques absorbent de l'eau par cette voie) |
|
glandes sudoripares |
la sueur permet essentiellement l'excrétion de chlore et surtout la thermorégulation mais les pertes d'eau ne sont pas négligeables au niveau de la peau en mlieu aérien. De la même façon il existe des animaux qui absorbent de l'eau par cette voie. |
|
reins |
le débit rénal calculé est de 1,2
L/min soit 20% du débit cardique. Le sang filtre au
niveau des glomérules (sorte de pelotes de
capillaires) et passe dans les tubules rénaux
(l'unité anatomique et fonctionnelle est le
néphron). L'ultrafiltration résulte
semble-t-il de la différence entre la pression dans
le capillaire glomérulaire (6kPa) et la pression dans
la capsule du néphron (estimée à 2 kPa
de pression osmotique et 2,7 à 4 kPa de pression
oncotique). En effet, on en est arrivé
dans cette partie à traiter de la fonction
rénale, de l'équilibre hydro-minéral,
on est dans un tout autre domaine que le contôle de la
pression artérielle. Ces facteurs interviennent sur
la volémie sans aucun doute mais on ne peut traiter
de façon détaillée chaque
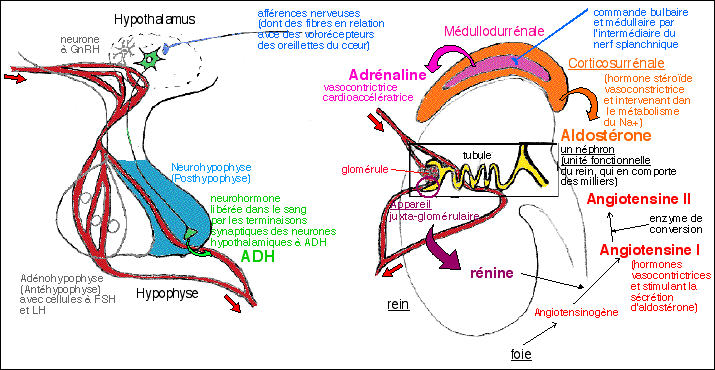
système. Le système rénine-angiotensine
est un mécanisme plutôt de type immunitaire et
je ne vois pas comment l'expliquer en quelques lignes...
tout comme les méacnismes liés directement au
sang comme la coagulation en cas d'hémorragie... La sécrétion de rénine est sous la dépendance de stimuli nerveux centraux, de la pression artériolaire au niveaude l'appareil juxta-glomérulaire et de la concentration en chlorures du tube contourné distal...La rénine scinde l'angiotensinogène en un peptide sanguin qui semble inefficace et l'angiotensine I qui est à son tour scindée en un autre peptide inefficace et l'angiotensine II par une enzyme de convesion que l'on trouve notamment en grande quantité dans les cellules endothéliales des artères pulmonaires. C'est l'angiotensine II qui est la forme la plus active qui agit directement comme puissant vasoconstricteur (contraction des fibres musculaires lisses, surtout au niveau mésentérique et cutané) et stimule la sécrétion d'aldostérone par la zone glomérulée des cortico-surrénales (cortex des glandes surrénales). L'aldostérone est une hormone stéroïde qui agit sur les cellules des tubes contournés distaux rénaux, les cellules de la muqueuse intestinale, des glandes salivaires et des glandes sudoripares. On la qualifie d'hormone minéralocorticoïde car elle semble diminuer les pertes de Na+ en échange d'une sortie de K+ et d'H+. |
|
tous les organes |
l'eau métabolique est produite notamment lors de la respiration (voir cours de première S : le dioxygène est l'accepteur final d'électrons de la chaîne respiratoire) |
Un paramètre sanguin, assez difficile à mesurer mais qui est important si l'on désire chiffrer l'adaptation d'un organisme à l'effort par exemple, est le taux d'extraction du dioxygène sanguin. Le sang artériel est saturé en dioxygène mais dans des conditions normales le sang veineux en contient encore entre 50% et 25% du volume extractible. Par simple effet de demande accrue (baisse de la pression partielle au niveau des tissus), les cellules peuvent donc augmenter le taux d'extraction du dioxygène.
Les paramètres physiques comme la viscosité sont difficiles à évaluer du fait de la présence de cellules (le sang est considéré comme un TISSU). Le sang est TRES visqueux : le plasma a une viscosité relative de 1,8 (par rapport à celle de l'eau égale à 1 à 37°C et 2,6 à 0°C) essentiellement à cause de sa composition en protéines dont la teneur est voisine de 7%. Les cellules, essentiellement les hématies (stockées notamment par la rate), augmentant encore la viscosité et étant susceptibles de provoquer des bouchons dans les capillaires très fins, où elles doivent se déformer pour pouvoir circuler ; il n'en reste pas moins que du fait de l'élasticité des vaisseaux et de la déformation des hématies, la viscosité réelle (apparente) est bien plus faible (le sang s'écoule bien plus facilement) que la viscosité théorique (calculée) ; on parle de comportement "non newtonien" du sang mais cela ne surprend pas du tout les physiologistes qui savent très bien que le sang est un tissu vivant....
2.2 Paramètres cardiaques : débit, fréquence et volume d'éjection systolique
Les paramètres cardiaques sont classiquement
exprimés dans la formule : D = F
x VES
, avec:
* le débit cardiaque (D) : exprimé en litres par
unité de temps
* la fréquence cardiaque (F) : exprimé en nombre
de battements par unité de temps
* le volume d'éjection systolique (VES; exprimé
en litres) dépend essentiellement de la valeur de la pression
de retour veineux (et donc du volume ventriculaire
télédiastolique, c'est-à-dire de la
quantité de sang qui reste dans le ventricule après
l'éjection systolique) mais la valeur moyenne de la pression
artérielle peut aussi s'opposer à ou favoriser
l'éjection et intervient donc dans le VES.
Pour un homme adulte au repos, F = 72 battements par minute, VES =
0,07L, soit D = 5 L/min, la totalité du sang de l'organisme
(estimée à environ 5L) est donc pompée par le
cœur chaque minute. Lors d'un effort la fréquence peut
être multipliée par trois et le volume d'éjection
systolique par presque deux, ce qui permet d'atteindre des
débits cardiaques de 30 L/min chez des athlètes, alors
que l'on considère qu'une valeur de 10 L/min correspond
à celle d'un exercice modéré avec F = 120
battements /min et VES = 0,085 L.
Contrôle de la fréquence cardiaque :
Le rythme autonome de décharge du tissu nodal
(nœud sinusal, zone musculaire à
caractéristiques embryonnaires (appelé aussi le
pace-maker cardiaque), relayé par un amas de cellules
semblables situé dans la cloison entre les oreillettes et les
ventricules : le nœud auriculo-ventriculaire) est de l'ordre de
100 battements par minute. On peut donc penser qu'un cœur humain
isolé du reste de l'organisme battrait avec un rythme
spontané de 100 battements par minute (mais il est
évident que cette expérience ne peut être
réalisée comme pour la grenouille ou pour la tortue
pour lesquelles le cœur isolé continue à battre
pendant plusieurs heures, et que d'autre part, le cœur des
Mammifères bat beaucoup moins longtemps et semble être
très sensible à la température et à
l'apport en dioxygène). Une preuve du rythme cardiaque
autonome est aussi l'observation des premiers battements cardiaques
embryonnaires, par exemple chez le poulet, bien avant la mise en
place de l'innervation.
Le contrôle nerveux direct a été mis en
évidence par d'innombrables expériences (cf manuels).
L'innervation efférente est double : orthosympathique
(OS ou sympathique) et parasympathique (PS). Elle
aboutit essentiellement au tissu nodal (nœud sinusal,
majoritairement, et nœud auriculo-ventriculaire pour une moindre
part) pour le PS, mais les neurones de l'OS innervent aussi
directement les fibres cardiaques. Le contrôle du rythme
cardiaque est donc principalement le contrôle nerveux du rythme
du tissu nodal mais certainement pas uniquement : il y a un
contrôle nerveux direct du muscle cardiaque.
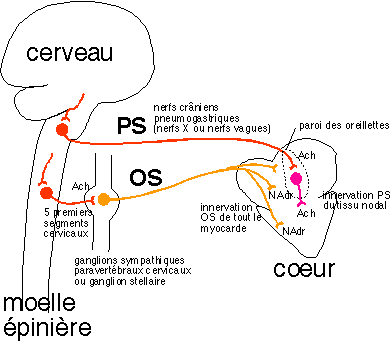
Des expériences classiques de section chez de nombreux
mammifères ont montré qu'il existe à la fois
un tonus cardiomodérateur (OS) et un tonus
cardioaccélérateur (PS), mais le rôle de
chaque système n'est pas forcément identique pour tous
les types d'effort et espèces de mammifères
considérés.
La noradrénaline (NAdr) est le neurotransmetteur
libéré par les fibres OS innervant le cœur, en se
fixant à des récepteurs ß1
adrénergiques, elle induit une augmentation de la
perméabilité au Ca2+ des cellules myocardiques et
nodales. Elle augmente la vitesse de dépolarisation
spontanée des cellules nodales et donc la fréquence du
rythme sinusal. Elle accélère aussi la vitesse de
conduction du tissu nodal. On note que lors de la stimulation de l'OS
et donc de l'accélération du rythme cardiaque, la
vitesse de contraction est augmentée mais la durée de
la diastole est diminuée de façon moindre et assure en
quelquesorte un remplissage ventriculaire convenable. Les
mécanismes ne sont pas donc aussi simples qu'une augmentation
de la fréquence des contractions cardiaques.
L'adrénaline (Adr) circulante libérée par
les médullosurrénales (par exemple en cas de stress ou
de peur) se fixe sur les mêmes récepteurs ß1
adrénergiques et a le même effet sur le rythme
cardiaque.
L'acétylcholine (Ach) est le neuromédiateur
libéré par les terminaisons synaptiques des neurones
postganglionnaires courts PS innervant essentiellement le tissu
nodal. Elle se fixe aux récepteurs muscariniques (M2)
des cellules nodales et provoquent une augmentation de la
perméabilité cellulaire au K+. De façon
symétrique à l'action de la noradrénaline,
l'acétylcholine diminue la vitesse de dépolarisation
des cellules nodales et augmente l'amplitude de leur
hyperpolarisation spontanée. Globalement l'Ach provoque donc
une diminution du rythme autonome du tissu nodal. L'Ach ralentit
aussi la conduction auriculo-ventriculaire et donc diminue la vitesse
de contraction cardiaque globale. Cependant l'Ach ne peut circuler
dans le sang comme l'adrénaline, car celui-ci contient une
enzyme qui hydrolyse l'Ach rapidement.
Contrôle du volume d'éjection systolique :
C'est essentiellement le volume de remplissage ventriculaire
qui semble être le paramètre principal qui modifie
à son your le volume d'éjection systolique. C'est ce
qu'on appelle la loi du cœur de Starling (voir par exemple fig.
5.16 dans Précis de physiologie, doin). Si on
réalise une préparation coeur-poumon, on constate qu'en
faisant varier artificiellement la pression assurant le remplissage
ventriculaire que l'on appelle pression de retour veineux (on
élève ou abaisse un réservoir connecté
à l'oreillette gauche par une des veines caves, l'autre veine
cave étant relié à un manomètre ; cette
pression représente, dans l'organisme, la pression veineuse
centrale), que plus la pression de remplissage ventriculaire augmente
(mesurée à l'aide d'un manomètre relié
à la cuve dans laquelle est immergée le cœur, ce
qui permet de voir les variations de volume cardiaque externe, que
l'on relie de façon indirecte au paramètre du volume
ventriculaire télédiastolique (volume de sang dans les
ventricules en fin de diastole, c'est-à-dire le volume maximal
de sang intraventriculaire) dans l'organisme), plus le volume
d'éjection systolique augmente (celui-ci est
évalué à partir du liquide éjecté
au niveau de la crosse aortique par un débitmètre
couplé à un mécanisme permettant de faire varier
la résistance à l'écoulement et d'un
manomètre...). Ainsi il semblerait que la pression de
remplissage ventriculaire joue directement sur le myocarde, les
fibres musculaires étirées ont tendance à se
contracter plus fortement. La noradrénaline,
libérée par les fibres OS innervant le myocarde,
augmente aussi la contractilité des cellules du myocarde et
donc aussi le volume d'éjection systolique.
L'adrénaline a les mêmes effets que la
noradrénaline sur les fibres du myocarde.
Des remarques plus générales:
Si l'on fait un peu d'anatomie comparée du cœur dans les
différentes classes de vertébrés, on note tout
d'abord que la taille du cœur (masse cardiaque)
croît proportionnellement à la taille de l'animal (masse
du corps). De même, à l'intérieur de chacun des
groupes considérés, des différences importantes
de métabolisme ne se traduisent pas par des différences
de volume cardiaque. Si l'on relie le volume cardiaque au volume
d'éjection systolique (plus le cœur est gros plus le
volume d'éjection systolique est élevé), on en
déduit que les variations de métabolisme
(quantité de dioxygène transporté car
utilisé par unité de temps par exemple)
résultent de variations du débit cardiaque plutôt
que du volume d'éjection systolique.
La fréquence cardiaque varie en sens inverse de la
masse du corps (25 battements par minute chez un
éléphant de 3000 kg au repos et 600 battements par
minute chez une musaraigne de 3g, le plus petit mammifère
existant ; on atteint 1200 battements par minute chez le colibri ou
de petites chauves-souris en vol...). On note aussi qu'il y a une
quasi proportionnalité entre la consommation de
dioxygène par unité de masse et la fréquence
cardiaque, par unité de masse (plus l'animal est petit, plus
il consomme d'oxygène et plus il a une fréquence
cardiaque élevée : ce que l'on peut formuler aussi en
disant que la consommation spécifique de
dioxygène est directement proportionnelle au rythme
cardiaque spécifique). On peut mesurer
expérimentalement le débit cardiaque, notamment avec la
méthode dite du "principe de Fick": en considérant que
la différence entre la quantité de dioxygène
à l'entrée du cœur et à la sortie du
cœur correspond bien à la quantité de
dioxygène consommé par l'organisme (Vo2), on mesure les
teneurs systémiques artérielle (CaO2) et veineuse(CvO2)
le plus près possible du cœur ; le débit cardiaque
(D) est alors donné par la formule : D = Vo2/(CaO2-CvO2). Bien
évidemment cette méthode ne fonctionne pas s'il y a
mélange des sangs artériels et veineux (amphibiens et
certains reptiles) et surtout si une part importante de la
respiration se fait par voie cutanée...
2.3 Paramètres systémiques : volume sanguin, pression, vitesse d'écoulement, résistance à l'écoulement, distribution...
Le sang circule dans des vaisseaux élastiques et contractiles mais un peu de mécanique des fluides circulant dans des tubes va nous aider à y voir un peu plus clair (voir Schmidt-Nielsen, ch 3). Un fluide ne se déplace pas selon des gradients de pression (il ne va pas d'une pression haute à une pression basse) mais dans le sens des potentiels croissants et donc on doit considérer à la fois l'énergie cinétique (vitesse et frottements) et l'énergie de gravité.
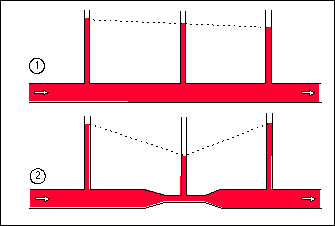
Remarque :
On parle ainsi souvent de résistance à
l'écoulement. Ce terme est défini à partir
de la loi de Darcy (la différence de pression (êp) entre deux
points voisins d'un même tube horizontal est
égale au débit (D) multiplié par la
résistance à l'écoulement (R) soit êp = D . R)
et n'est valable que dans un tube de diamètre constant
et ne pouvant s'allonger (à diamètre constant)...ce
qui n'est pas le cas des vaisseaux sanguins. On extrapole cette
notion à toutes les variations de diamètre des
vaisseaux qui s'opposent à l'écoulement, que l'on nomme
d'une façon générale "résistance
périphérique". Ces forces résultent d'une
contraction volontaire des muscles lisses de la paroi des
artérioles. Mais il est important de voir que l'augmentation
de la résistance périphérique par
vasoconstriction artériolaire provoque une diminution de
débit à pression constante (ce qui est souvent le cas)
ou une augmentation de pression, à débit constant (ce
qui intuitivement nous paraît le plus fréquent mais qui
est en fait assez rare....).
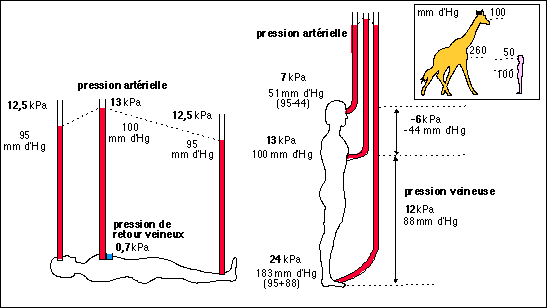
Le terme d'énergie de gravité est identique
quasiment en tout point du corps en position allongée.
Mais la gravité s'exerce sur la colonne sanguine en position
debout de façon très différente selon les
parties du corps :
la pression artérielle au niveau de la tête n'atteint
que 7kPa (50 mm d'Hg) pour l'homme
(chiffres à comparer avec la girafe avec son cou de 2 m de
long, ces chiffres sont issus de mesures...)
(in Schmidt-Nielsen, fig 3.15 et 3.16 et
Précis de physiologie, fig.5.19)
Le diamètre des vaisseaux est en relation directe avec la
pression qu'ils doivent supporter (relation de Bernouilli ou loi de
Laplace : la tension exercée sur une paroi est
égale au produit de la pression par le rayon du tube). Les
artères de gros diamètre ont effectivement une paroi
plus épaisse qui leur permet de résister
à cette augmentation de la tension. Par contre les capillaires
peuvent avoir et ont une paroi extrêmement fine.
Mais il y a aussi les forces de cisaillement qui s'exercent
d'abord dans le liquide sanguin, visqueux, mais aussi au niveau des
cellules endothéliales notamment.
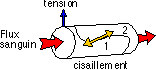
Les forces de cisaillement exercent une contrainte (traction) sur la paroi des vaisseaux parallèlement à leur surface : ici par exemple sur deux cellules endothéliales adjacentes (1 et 2). On a noté notamment des proliférations de cellules endothéliales dans les vaisseaux soumis de fortes contraintes (la multiplication des cellules permet une diminution de la surface de chaque cellule et donc de la contrainte de cisaillement, sans compter l'augmentation du diamètre du vaisseau qui joue aussi dans le même sens). On notera s'une vasoconstriction d'un vaisseau se traduit par une augmentation des contraintes de cisaillement.
Au niveau des capillaires la théorie proposée par Starling en 1896 est toujours considérée comme valable: le sang est filtré (on parle d'ultrafiltration) et passe dans les espaces interstitiels lorsque la pression hydraulique (résultant de l'énergie cinétique et de gravité) est supérieure à la pression oncotique (pression osmotique résultant de la présence de protéines dans le sang et qui sont trop grosses pour filtrer à travers l'endothélium, considérée comme fixe et égale à 25 mm d'Hg). L'ultrafiltration du liquide interstitiel se fait dans le sens inverse au niveau des capillaires lorsque la pression hydraulique devient plus faible que la pression oncotique.
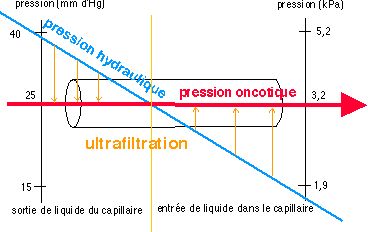
Ce modèle est assez utilisé cependant est permet de prévoir que sur l'ensemble de l'organisme il y a un excédant de filtration, ce qui justifie que le liquide interstitiel excédentaire est drainé et canalisé (lymphe circulante) et rejoint le cœur au niveau de la veine cave. On admet ainsi qu'à l'échelle de l'organisme 20 L sont filtrés et 16-18 L réabsorbés par jour, ce qui représente un débit lymphatique de 2-4 L par jour. Le modèle permet aussi de prévoir qu'en cas d'hémorragie il y a une chute de pression hydraulique et donc de pression de filtration ce qui fait que le sang se dilue (hémodilution) ; ce phénomène est connue en médecine en cas d'hémorragie importante sous le nom d'hémodilution hémorragique lorsque du liquide interstitiel passe vers le sang.
|
(in Schmidt-Nielson, fig 3.6) |
||||||||||||
|
homme |
vache |
mouton |
chien |
chat |
poulet |
pigeon |
alligator |
tortue |
grenouille |
crapaud |
morue |
carrelet |
|
3,2 |
2,8 |
2,9 |
2,7 |
3,2 |
1,5 |
1,1 |
1,3 |
0,9 |
0,7 |
1,3 |
1,1 |
1,1 |
On ne sait pas interpréter ces variations. On notera notamment qu'elle est plus élevée chez les mammifères alors qu'elle est plutôt basse chez les oiseaux alors que leur pression artérielle est élevée (mais on ne connaît pas bien leur pression capillaire). On connaît aussi des cas pathologiques de baisse de la pression oncotique (par exemple par des fuites urinaires d'albumine) qui se traduisent alors parfois par des œdèmes.
D'une façon plus générale il est particulièrement intéressant de développer l'étude des microcirculations au niveau des capillaires. On distingue habituellement trois types de capillaires :
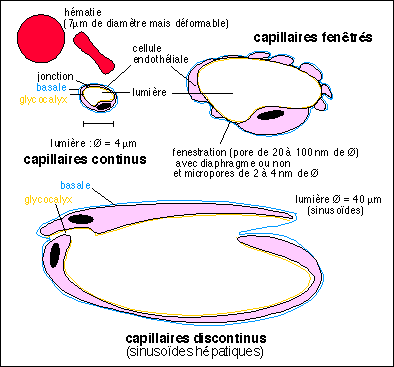
Le passage de la barrière capillaire (ce mot est assez mal venu étant donné le rôle principal de surface d'échange) ou du filtre capillaire se fait soit à travers la cellule (voie transcellulaire notamment par pinocytose : petites vésicules), soit par les jonctions intercellulaires (serrées, étanches ou fenêtres ou pores ou simple lame basale à traverser...). C'est à ce niveau qu'interviennent de nombreux contrôles et la physiologie des microcirculation est certainement encore riche de découvertes.
La vitesse d'écoulement dépend bien sûr des paramètres liquidiens comme la viscosité mais aussi de la distribution dans le réseau :
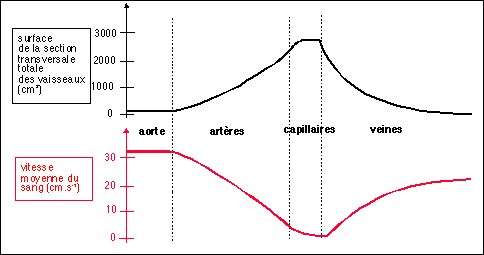
La répartition ou plutôt la distribution du sang au sein du réseau est un paramètre qui peut être évalué par la mesure des débits sanguins.
|
(in Schmidt-Nielsen, fig 3.4) |
|||||
|
|
|
|
|
||
|
|
0,3 |
3,5 |
|
3,6 |
|
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
66,5 |
|
2,0 |
|
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|||
L'élasticité des vaisseaux est très difficile à évaluer in vivo. Un expérience simple : examiner ses propres veines au niveau du bras et de l'avant-bras en fonction de la position de ceux-ci. Si l'on se tient assis les bras ballants, on constate que les veines situées au-dessus du niveau du cœur sont collabées (signifie de section ovale : vient du latin collabor, eris, apsus = tomber avec, s'affaisser (collapsus), s'écrouler) ; alors que les veines sont d'autant plus gonflées que l'on s'abaisse en dessous du niveau du cœur. Si l'on relève le bras à l'horizontale, les veines sont toutes collabées.
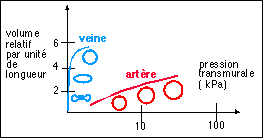
Le contôle local de la vasodilatation artériolaire est sous la dépendance d'abord des produits du métabolisme : pCO2, H+, pO2, température sont autant de stimuli pour la vasodilatation des fibres lisses de la paroi artériolaire. Dans le cadre de lésions cellulaires ou à la suite de réactions inflammatoires, de nombreuses substances vasodilatatrices peuvent être libérées : histamine et surtout les kinines (bradykinine) ou encore l'angiotensine II (octapeptide circulant à demie-vie plasmatique très brève mais donc l'activité vasodilatatrice est près de 5 fois plus élevée que celle de l'adrénaline, à demie-vie plasmatique plus longue) ; une nouvelle famille de peptides d'origine cardiaque a aussi été découverte dont le facteur atrial natriurétique, secrété par l'oreillette en réponse à une distension de sa paroi : son action est diurétique (augmentation du voolume urinaire par baisse de la réabsorption de l'eau), natriurétique (augmentation de l'excrétion rénale de Na+) et vasorelaxante (il inhibe la sécrétion d'aldostérone par les surrénales et la libération de rénine par l'appareil juxta glomérulaire) ; on connaît aussi des substances vasoconstrictrices comme la sérotonine (libérée notamment par les plaquettes sanguines).
2.4 Notion de récepteur interne... la sensibilité interne : proprioceptive ou viscéroceptive
Pour tous les modèles de contrôle il semble important que les paramètres contrôlés soient mesurés. Comment cela est-il possible ? Comment concevons-nous cette mesure ? Nous utilisons tous le terme de récepteur interne mais que recouvre cette notion ?
Les classifications ne me semblent pas utiles car elles se recouvrent. Voir par exemple les généralités sur la perception dans le cours d'enseignement général (Stimuli et organes des sens). Que l'on appelle cette sensibilité proprioceptive ou viscéroceptive ne change pas grand chose : les organes sont-ils sensibles à certains paramètres et comment le manifestent-ils ? La sensibilité interne est-elle toujours nerveuse ? Y a-t-il une différence entre un barorécepteur et un volorécepteur ? Mais, plus insidieusement, existent-ils tout simplement ?
Je pense que je ne suis pas le seul enseignant à être
très étonné de l'absence de données
facilement accessibles, dans les ouvrages que j'ai utilisé et
que j'apprécie donc beaucoup par ailleurs.
|
(Bordas, spécialité, 1994, p 74 ; Bordas, TD, 1989, p 246 et p 258 ; Physiologie humaine, A.J. Vander, J.H. Sherman et D.S. Luciano, 1977, McGraw Hill) |
|
On présente comme une donnée anatomique
(chez le chien ou chez l'homme) l'innervation de la paroi
musculaire lisse des sinus carotidiens (renflements à
la base des carotides) par les nerfs de Hering, pairs,
reliés au bulbe rachidien (on notera qu'une bonne
part du trajet est commun aux nerfs X
parasympathiques...). En ce qui concerne la sensibilité à des
substances chimiques, on rapporte la présence de
chimiorécepteurs ou
chémorécepteurs au niveau des corps
carotidiens et aortiques, situés très
près mais distincts des récepteurs à
l'étirement précédents. On pense que ce
seraient des cellules épithéliales
associées à des terminaisons nerveuses
sensitives (?). Là encore les ouvrages dont je
dispose sont peu complets : il semblerait que ce soit la pO2
du sang artériel qui soit le stimulus
déclencheur des PA sensitifs... (???) Mais le
rôle de la pCO2 n'est pas non plus négligeable
et notamment par l'intermédiaire du pH qui semble
être un paramètre essentiel au niveau du
liquide céphalo-rachidien, notamment. |
Pour pouvoir comprendre la régulation de la fonction est
est nécessaire de déterminer précisément
la fonction de l'appareil circulatoire (je précise que
l'appareil circulatoire doit à mon sens être
élargi à l'appareil lymphatique qui permet le retour au
sang du liquide intersticiel). Il est évident que ses
fonctions sont multiples. On essaiera de les classer par ordre
d'importance, mais je sais bien tout ce que ce classement à de
provisoire et subjectif :
* travail de nutrition : distribution de l'oxygène
et des nutriments aux organes (si l'on étudie la
distribution au niveau artériel et artériolaire) et aux
cellules (si l'on étudie les mécanismes au niveau des
capillaires). On peut aussi envisager le rôle de l'appareil
circulatoire dans la prise en charge des nutriments et de
l'eau au niveau de l'appareil digestif ou du dioxygène au
niveau de l'appariel pulmonaire. De la même façon,
l'élimination des déchets gazeux au niveau des
poumons ou en solution au niveau des reins, fait partie des fonctions
auxquelles participe l'appareil circulatoire.
* travail de relation : l'appareil circulatoire
transporte non seulement des molécules chimiques
informatives (médiateurs) mais aussi des cellules
spécialisées dans les communications entre
populations cellulaires (les cellules immunitaires). Il
participe aussi au maintien de la forme (hydrosquelette) des
organes (et pour des organismes plus simples que l'homme, au
squelette principal : chez les annélides par exemple...).
L'appareil circulatoire est aussi l'élément principal
du milieu intérieur : on pourrait dire que c'est le milieu
intérieur dynamique. Mais je ne pense pas que dans la
conception du vivant que je m'efforce de présenter il soit
nécessaire de considérer qu'il existe une fonction
homéostasique: il ne me semble pas pertinent de voir le milieu
intérieur comme un milieu aux paramètres
régulés... laissons cette vision aux modèles
logiques... je préfère pour ma part un modèle
interne : ce sont les fonctions qui sont réglées et non
d'hypothétiques paramètres : ce n'est pas
l'équilibre hydro-minéral qui est réglé
c'est l'absorption par exemple de Ca2+ au niveau de l'intestin en vue
d'approvisionner le squelette ou le foetus en cours de grosesse...).
Par contre la locomotion (qui met bien sûr en jeu la
nutrition des muscles) est une fonction qui fait intervenir en
premier chef la circulation sanguine. De même, dans le cadre de
la défense de l'organisme, les mécanismes de lutte
contre une hémorragie par exemple font partie de ce
travail de relation avec le milieu.
Je voudrais illustrer ici encore cette conception en prenant
l'exemple de la température qui est habituellement vue comme
un éléments stable (on parle
d'homéothermie/poïkilothermie ou plutôt
d'endothermie/ectothermie, comme on préfère le faire
maintenant) alors que l'on peut très bien voir la
température comme une conséquence du
métabolisme. Dans ce cas, le fonctionnement de chaque organe
étant reglé, la constance (ou la variation) de la
température n'est alors que la conséquence du type de
fonctionnement des organes chez tel ou tel organisme. Quand on voit
un reptile se chauffer au soleil on est bien d'accord pour dire qu'il
ne thermorégule pas mais qu'il augmente sa température
interne pour pouvoir démarrer une activité
métabolique suffisante pour lui permettre par exemple la
locomotion active en vue de la recherche de nourriture. De la
même manière, voir une thermorégulation dans le
mécanisme sudatif peut être remplacé par la
considération que ce qui est observé est une
élimination de l'énergie calorifique
excédentaire (dans le sens non pas de "par rapport à
une norme" mais bien comme la conséquence d'une
activité du vivant) produite par exemple par l'activité
musculaire : la finalité (causalité) étant bien
l'activité musculaire et non la régulation de la
température.
* travail de reproduction : on retrouve le travail de
nutrition mais cette fois dirigé vers le foetus en cours de
grossesse, des mécanismes aussi variés que l'ovulation
(dont nous avons déjà dit qu'elle était
considérée comme un processus inflammatoire) ou
l'érection...
On en arrive à un point très
intéresssant mais qui rend très difficile
l'exploitation des sujets de bacalauréat qui sont souvent
articiels (ce sont de faux problèmes avec des solutions
attendues, et pour lesquelles trouver une autre réponse serait
sanctionné).
Dans notre conception du vivant, toute modification artificielle
de l'équilibre dynamique , comme par exemple l'injection
de rénine, d'angiotensine II ou encore d'adrénaline,
chez des sujets malades ou non, ou chez des animaux de laboratoire,
est suivie d'un retour à l'équilibre initial. Il
n'y a pas là, à mon sens, une preuve d'une
régulation d'un paramètre mais bien de
l'équilibre dynamique du vivant au repos, c'est à dire
de l'ensemble des mécanismes du vivant : en absence de toute
activité particulière (métabolisme au repos), il
y a un équilibre dynamique, mais la stabilité des
paramètres n'est qu'une conséquence de l'état de
repos. La seule chose que l'on puisse déduire d'une injection
au repos est au mieux le lieu ou mode d'action de telle ou telle
substance. Ces expériences nous renseignent bien peu sur les
fonctions. Les dosages lors d'efforts physiques ou
d'hémorragies sont bien plus riches en enseignements.
Quand on montre à un élève
une courbe de pression artérielle sur 24 h (avec des
périodes de sommeil, d'activité physique, de repas, de
repos... Bordas p 68, Nathan p 54) et qu'on attend de lui qu'il en
déduise la notion de régulation de la pression
artérielle...je crains que l'on ne soit assez peu
crédible (ce que fait il me semble le Nathan mais pas le
Bordas, plus prudent): la courbe montre à l'évidence
des variations en fonction des différents types de travail du
vivant, dans des limites particulières (minima-maxima) qui
sont les limites physiques, structurales, de l'appareil circulatoire
et qui varient selon le sexe et les individus (mais justement ce sont
des concepts qu'une seule courbe ne peut pas montrer, sauf si l'on
sous-entend que toutes les courbes sont identiques chez tous les
individus, ce qui est bien évidemment faux). La conclusion
proposée à la suite de la présentation d'une
telle courbe est donc bien : la pression artérielle est un
paramètre très variable (mais pas
contrôlé). La nécessité du contrôle,
intuitive certes, demanderait à être établie
à partir de courbes de pathologies pour montrer les limites
connues chez les êtres vivants (ce que fait le Nathan en
montrant la table de Master mais pas vraiment le Bordas...mais
personnellement, je ne vois pas très bien l'usage que l'on
peut faire de telles tables étant donné que l'on ne
sait pas comment elles sont établies, on ne connaît pas
les écarts, les échantillons de population, le pays
d'étude... bref on est pas du tout dans une démarche
biologique), ou mieux d'expériences sur la résistance
des vaisseaux et des surfaces d'échange à des
variations importantes de la pression... A partir de cette courbe on
peut aussi montrer que les valeurs des pressions systoliques et
diastoliques sont étroitement corrélées
(à l'échelle de l'observation, c'est à dire sur
24h, mais pas comme nous le verrons plus loin à une
échelle plus grande). Il y a là une indication sur la
mécanique cardiaque ou plutôt sur les
propriétés physiques des artères où l'on
mesure cette pression..
Il est donc clair qu'il est hors de question de traiter l'ensemble des aspects et des régulations telles qu'on les comprend dans chaque cas. Je vais donc essayer d'en traiter deux, qui semblent être les exemples qui sont choisis pour les sujets du baccalauréat : l'effort physique et l'hémorragie.
Lors d'un effort musculaire (muscle strié squelettique) on peut penser que les deux paramètres essentiels sont d'une part l'apport de l'oxygène et des nutriments au muscle et d'autre part l'élimination des déchets (dioxyde de carbone et acide lactique).
Les principales modifications cardiovasculaires sont résumées dans le tableau ci-dessous mais les chiffres ne sont pas homogènes selon les sources : il s'agit plutôt de donner ici des limites de variations et des tendances générales :
|
(Vander, 1977 ; Précis de Physiologie, doin, 1997) |
||||
|
(debout) |
|
|
||
|
|
|
|||
|
débit musculaire |
1,2 L/min |
12,5 L/min |
+175% |
|
|
débit rénal |
1,1 L/min |
0,6 L/min |
-30% |
|
|
débit cardiaque |
5,5 L/min |
20-30 L/min |
+120% |
augmentation proportionnelle à l'intensité de l'effort si celui-ci est modéré. Débit maximal possible amélioré par l'entraînement |
|
fréquence cardiaque |
72 battements par min |
180-200 battements par min |
+100% |
* la fréquence au repos diminue chez le sujet
entraîné |
|
volume d'éjection systolique |
75 mL |
de 100 à 160 mL |
+20% |
le volume au repos et le volume maximal lors de l'effort
sont augmentés par l'entraÎnement |
|
volume ventriculaire télédiastolique |
= |
|||
|
pression artérielle moyenne |
13 kPa |
+15% |
augmentation très modérée en effort dynamique aérobie, plus forte en effort statique |
|
|
pression artérielle systolique |
+50% |
|||
|
pression artérielle diastolique |
= |
|||
|
pression de retour veineux central |
0,7 kPa |
0,8 kPa |
+10% |
augmentation due essentiellement à la pompe musculaire veineuse et à une vasoconstriction veineuse (nerf splanchnique orthosympathique) |
|
résistance périphérique totale |
-50% |
|||
Un point essentiel lors de l'exercice est l'augmentation du retour
veineux qui est certainement facilité par les pompes
musculaires externes et les mouvements respiratoires (voir plus haut)
ainsi que par la vasodilatation artériolaire au travers des
muscles en cours d'activité. On rapporte qu'un lévrier
dont le coeur a été dénnervé est capable,
après récupération de l'intervention, de courir
presque aussi vite qu'avant la dénnervation. On note alors
surtout une augmentation du volume d'éjection systolique.
Ces questions sont notamment importantes dans le cas de greffes
cardiques pour lesquelles le coeur greffé n'est bien sûr
plus innervé, même s'il est stimulé
artificiellement.
En ce qui concerne l'apport du dioxygène, on a quelques
résultats (in Schmidt-Nielsen et Turquier):
Les mesures de débit cardiaque réalisées
selon le principe de Fick (voir plus haut) montrent notamment
que lors d'un exercice, chez tous les animaux chez qui l'on a fait la
mesure (peu nombreux il est vrai), il n'y a pas d'augmentation du
débit cardiaque proportionnelle à la consommation de
dioxygène : une plus grande utilisation d'oxygène a
pour conséquence une baisse de la concentration de
dioxygène dans le sang veineux : le débit cardiaque
n'est pas un paramètre réglé autour d'une valeur
constante.
Ainsi, lors d'un effort, l'utilisation accrue d'oxygène est assurée par trois mécanismes simultanés (que l'on compare ici chez la Truite entraînée à nager à contre-courant, chez un oiseau et chez l'homme):
En ce qui concerne les paramètres circulatoires généraux (permettant d'évaluer la distribution sanguine), voici quelques données (d'après Vander, 1977 et Turquier, 1994, modifiés):
|
|
|||||||||
|
cerveau |
cœur |
muscles |
peau |
reins |
abdomen |
autre |
total |
||
|
débits |
au repos |
750 |
250 |
1200 |
500 |
1100 |
1400 |
600 |
5800 |
|
lors d'un exercice intense |
750 |
750 |
12500 |
1900 |
600 |
600 |
400 |
17500 |
|
|
masse (kg) |
1,4 |
0,3 |
29 |
2,5 |
0,3 |
35 |
70 |
||
|
débits relatifs |
au repos |
536 |
833 |
41 |
200 |
3667 |
29 |
||
|
lors de l'exercice intense |
536 |
2500 |
431 |
760 |
2000 |
14 |
|||
Il est important de souligner que ces chiffres concernent des débits et non par exemple la concentration en dioxygène dont la teneur peut varier énormément d'une zone à l'autre (mais la consommation de dioxygène de chaque organe est bien sûr corrélée étroitement à son activité métabolique : on peut même affirmer sans grande crainte de se tromper que l'augmentation du débit cardique est sans aucun doute causée par l'augmentation de la consommation de dioxygène par le muscle cardiaque lui-même grâce à son irriguation coronarienne... par contre l'augmentation de débit au niveau de la peau pourrait être corrélée plutôt à l'évacuation de l'excédent de chaleur produit lors de la contraction musculaire) ou encore la pression qui peut chuter fortement sans qu'il y ait forcément une variation de débit ou inversement augmenter sans que le débit soit changé...
L'élévation de la fréquence cardiaque
apparaît même lorsqu'un effort est prévu puis
finalement non exécuté, elle apparaît en moins
d'une demi-seconde et est sous l'étroite dépendance du
cortex par l'intermédiaire de décharges sympathiques.
Pendant l'effort physique, les rétrocontrôles
supposés si l'on considère que la pression
artérielle est un paramètre régulé sont
supprimés, il est par contre certain que c'est avant tout une
augmentation de l'apport de dioxygène (et son extraction voir
plus haut) aux muscles en activité dont le coeur, qui est
observée. Il est donc plus exact de parler de l'adaptation de
l'organisme à l'effort, dont l'augmentation de pression
artérielle n'est ni vraiment un symptôme, ni vraiment
une nécessité.
Du point de vue du contrôle nerveux on a une augmentation de
l'activité sympathique et donc libération de
noradrénaline qui agit sur les récepteurs ß1 des
cellules cardiaques et participe ainsi à l'augmentation du
débit cardiaque. Selon les zones de distribution sanguine et
selon le type de récepteurs, l'effet de la
noradrénaline libérée par les terminaisons
sympathiques innervant les fibres lisses vasculaires est variable :
la fixation de la noradrénaline sur les récepteurs
alpha provoque une constriction, alors que pour les récepteurs
ß1 et ß2 il y a relaxation. Les récepteurs alpha
se trouvant surtout au niveau du rein et des réseaux veineux,
les récepteurs ß2 plutôt au niveau des vaisseaux
irriguant les muscles squelettiques striés (mais
l'adrénaline est alors plus efficace que la
noradrénaline). Les coronaires portent des récepteurs
ß1.
A l'arrêt de l'effort, il n'est pas rare d'observer une
hypotension passagère que l'on interprète comme une
brusque chute du débit cardiaque alors que la
résistance périphérique reste encore faible
pendant plusieurs minutes.
|
(adrénaline, noradrénaline) agoniste (substance efficace avec transduction du signal) antagoniste (substance se liant spécifiquement au récepteur mais ne provoquant pas d'effet) remarques : la demi-vie de l'adrénaline dans le sang est très bève, de l'ordre de 10 à 20 secondes, la plupart des tissus sont sensibles à l'adrénaline, les effets étant modulés en fonction des différentes affinités et des proportions entre les différents récepteurs au niveau d'un tissu donné (pour ce que l'on pense...) : on peut ainsi avoir des effets opposés selon le dosage et donc selon le type de récepteurs (à faible dose par exemple la grande affinité des récepteurs ß est dominante et provoque une vasodilatation, alors qu'à forte dose ce sont les récepteurs alpha 1 plus nombreux mais de plus faible affinité qui déterminent une vasoconstriction...) |
||
|
|
agoniste spécifique = méthoxamine , antagoniste spécifique = prazosine récepteurs pour lesquels l'affinité de l'adrénaline est la plus faible |
* se trouvent notamment sur les artères irriguant les reins et les territoires splanchniques et la peau , la fixation des catécholamines provoque une vasoconstriction et donc une diminution du débit sanguin local * on en trouve aussi au niveau du foie, les catécholamines provoquant alors une activation de la glycogénolyse et de la néoglucogénèse (conduisant à une libération de glucose dans le sang et donc à une élévation de la glycémie) * au niveau de la vessie, les muscles du sphincter et le trigone sont sensibles aux catécholamines, se contractent et inhibent la miction (action d'uriner) |
|
agoniste spécifique = clonidine , antagoniste spécifique = yohimbine |
ce sont les récepteurs de la membrane postsynaptique des synapses adrénergiques situés essentiellement au niveau des veines, la fixation des catécholamines provoque une constriction |
|
|
indéterminés |
au niveau des muscles arrecteurs des poils , les catécholamines provoquant une piloérection |
|
|
|
agoniste spécifique = xamotérol , antagoniste spécifique = practolol l'affinité de l'adrénaline et de la noradrénaline sont équivalentes pour ces récepteurs |
se trouvent surtout au niveau du coeur et des artères coronaires : la fixation des catécholamines provoquant une augmentation de la contractibilité et de la vitesse de contraction pour le coeur (effet dit inotrope) et une dilatation des artères coronaires (augmentation du débit sanguin coronarien) |
|
agoniste spécifique = salbutamol , antagoniste spécifique = butoxamine l'affinité de l'adrénaline est supérieure à celle de la noradrénaline pour ces récepteurs |
* situés au niveau des artères des muscles squelettiques, la fixation des catécholamines provoque une vasodilatation et donc une élévation du débit sanguin local * au niveau de l'appareil juxtaglomérulaire, les catécholamines activent la sécrétion de rénine, qui agit sur la transformation de l'angiotensinogène en angiotensine II et donc provoque une augmentation de la pression artérielle * au niveau du foie ils sont présents avec les récepteurs alpha 1 provoquant alors une activation de la glycogénloyse et de la néoglucogénèse (conduisant à une libération de glucose dans le sang et donc à une élévation de la glycémie) * au niveau des muscles, la fixation des catécholamines provoque une activation de la glycogénolyse et donc une augmentation de métabolisme anaérobie musculaire (fermentation lactique avec production de lactate) * au niveau des bronches, les catécholamines provoquent une relaxation et donc une bronchodilatation |
|
Je n'ai pas trouvé de documents originaux, je me
réfère donc à ceux du manuel (Nathan p 63) qui
ont été repris dans un sujet de bac et à ceux
d'une vieille édition "du Vander" que j'ai ajouté en
rouge plus foncé sur le tableau ainsi qu'un tableau de
données liquidiennes (Physiologie humaine, A.J. Vander,
J.H.Sherman, D.S. Luciano, McGraw-Hill, 1977): j'espère qu'il
s'agit bien ici d'une véritable hémorragie et non d'un
prélèvement de sang qui n'a aucun sens du point de vue
physiologique (voir plus haut) et que l'on est bien chez
l'homme...j'imagine aussi que l'hémorragie a été
stoppée dans la première minute... l'individu est-il
couché ? où a-t-on mesuré la pression
artérielle ? Y a-t-il eu un stress (choc) : s'agit-il d'un
accident ou d'une hémorragie volontaire, expérimentale
? ... bref des tas de questions indispensables si l'on veut
comprendre quelque chose à la physiologie,
quand cessera-t-on de nous proposer des
modèles à analyser..? il faut donner des
expériences (complétes) aux élèves et non
des modèles....
.
|
|
||||
|
|
|
|||
|
|
|
|||
|
pression artérielle (mm d'Hg) |
max |
|
|
|
|
min |
|
|
|
|
|
pression auriculaire (mm d'Hg) |
|
|
|
|
|
volume d'éjection systolique (mL) |
|
|
|
|
|
volume télédiastolique (mL) |
|
|
|
|
|
fréquence cardiaque (battements/min) |
|
|
|
|
|
débit cardiaque (mL/min) |
|
|
|
|
|
débit rénal (mL/min) |
|
|
|
|
|
débit encéphalique (mL/min) |
|
|
|
|
Que peut-on déduire de l'analyse de ces résultats
très incomplets ? Beaucoup d'hypothèses et très
peu de certitudes...
* la pression artérielle diastolique est revenue
à sa valeur initiale en 5 minutes, après avoir
chuté fortement ; par contre la pression artérielle
systolique reste plus faible... on est donc dans le cas où
pression artérielle systolique et diastolique sont
"découplées" alors que l'on pensait qu'elles
étaient toujours corrélées : le mécanisme
est-il lié au coeur ou aux vaisseaux ou aux deux ?
* la pression auriculaire chute immédiatement, c'est
donc bien un paramètre qui est lié directement à
l'hémorrragie, et elle est toujours très faible 5
minutes plus tard, elle n'est donc pas contrôlée de
façon très efficace
* le volume d'éjection systolique baisse
immédiatement (de 47% et il n'est plus qu'à -30%
après 5 minutes soit une chute moins rapide et un
rétablissemnt plus rapide que le volume
télédiastolique ce qui indique qu'il y a un
mécanisme compensateur d'augmentation de la contraction
cardiaque (voir plus haut))
*le volume télédiastolique est relié au
remplissage ventriculaire en fin de diastole : il chute de 50% juste
après l'hémorragie mais remonte à 40% en 5
minutes
* la fréquence cardiaque augmente mais pas
immédiatement (il n'y a donc pas une relation directe,
immédiate, entre la pression artérielle et le rythme
cardiaque), elle est donc bien contrôlée mais n'est pas
un paramètre sanguin...: le cœur est un effecteur de la
réponse à une hémorragie...
* le débit cardiaque est modifié directement par
l'hémorragie et n'est pas rétabli, c'est bien ce que
l'on avait vu pour l'effort physique: le débit cardiaque n'est
pas un paramètre maintenu constant
* le débit rénal chute lors de
l'hémorragie (il est vraiment dommage que l'on ne connaissae
pas le lieu de l'hémorragie car il est impossible de savoir si
cette baisse et locale ou générale... le fait qu'elle
soit aussi répercutée au niveau de l'encéphale,
nous fait penser plutôt à une variation globale), et il
ne semble pas revenir à sa valeur rapidement et donc ne pas
être contrôlé... est-ce à la suite d'une
modification de la pression systémique ou est-ce une
régulation locale ?
* le débit encéphalique est modifié
immédiatement, ce qui fait penser que l'hémorragie soit
se trouver bien près de la tête..., mais 5 minutes plus
tard, la valeur initiale est quasiment rétablie. En absence
d'autre paramètres on peut penser que que débit
encéphalique est contrôlé dans le sens où
le fonctionnement cérébral est prioritaire par rapport
à l'irriguation d'organes moins essentiels...
|
(Vander, 1977) |
|||||
|
|
|
||||
|
|
|
||||
|
|
|
|
variation (% de la valeur initiale) |
||
|
volume sanguin total (mL) |
|
|
|
|
|
|
volume érythrocytaire (mL) |
|
|
|
|
|
|
volume plasmatique (mL) |
|
|
|
|
|
|
albumines plasmatiques (masse en g) |
|
|
|
|
|
Ce tableau permet de préciser que 3h après l'hémorragie si le volume sanguin total est quasiment rétabli (-2% de la valeur initiale), c'est essentiellement à cause de l'augmentation du volume plasmatique (+13% trois heures plus tard soit 33% du volume total si l'on tient compte du volume à rétablir à la suite de la perte) et de la sécrétion d'albumines et non par la libération de globules rouges.
Il semblerait que l'organisme tolère assez bien des hémorragies avec une perte inférieure à 20% du volume sanguin total. Au delà on observe un état de choc qui peut brusquement empirer au bout de quelques heures et l'hypotension s'accentue alors de façon irréversible et conduit à la mort. On peut aussi assimiler à des hémorragies les pertes de liquide extracellulaire dues par exemple à des diarrhées sévères ou à des brûlures, des vomissements ou encore des pertes urinaires, mais plus rarement. On observe alors les mêmes symptômes que lors de la perte sanguine hémorragique. On peut aussi souligner du point de vue pratique qu'en cas d'hypotension il est formellement déconseillé de donner de l'alcool (vasodilatateur) ou de réchauffer le blessé par exemple à l'aide de couvertures (vasodilatation périphérique) ou pire encore, de le mettre en position debout (on diminue alors le débit encéphalique du fait de la position de la tête en hauteur par rapport au coeur)
Le terme pression artérielle fait en fait référence à la pression moyenne (au-delà de la pression atmosphérique) qui règne dans les grosses artères et MESUREE à l'aide d'un sphygmomanomètre (ou brassard gonflable associé à un manomètre et un stéthoscope : vois technique dans le livre de TS : Bordas p 62, Nathan p 53). On mesure bien évidemment soit la pression au bras en position couchée, soit la pression au bras en position debout ou assis, à hauteur du cœur, de façon à s'affranchir de l'énergie gravitaire.
a. un modèle logique : la pression artérielle est un paramètre réglé autour d'une valeur moyenne.
C'est le formalisme habituel qui s'inspire des systèmes
artificiels.
D'une part on extrapole de façon indue la loi de Darcy
à l'ensemble de la circulation systémique et l'on
considère que la mesure de la pression
artérielle réalisée avec le brassard donne
une estimation du êp au niveau du cœur (à peu près
égale à la pression mesurée si l'on
néglige la pression de retour veineux). Ce êp est donc
considéré comme une estimation du produit du
débit cardiaque (lui-même fonction de la
fréquence cardiaque et du volume d'éjection systolique)
par la résistance périphérique totale
(grandeur totalement imaginaire qui assimile le réseau
systémique à UN tube de diamètre UNIQUE (mais
adaptable) donc indéformable pour une valeur donnée de
la résistance périphérique). On est loin d'un
modèle du vivant.
Une analogie très parlante que l'on peut faire est celle de la
distribution d'électricité par l'EDF qui maintient
à tout instant une différence de potentiel entre le
phase et le neutre de votre prise de courant de 210-200 V quel que
soit le nombre d'appareils branchés sur le réseau. Dans
cette vision mécaniciste, l'organisme maintient toujours une
valeur fixe de la pression artérielle pour approvisionner
correctement les organes en dioxygène par exemple. Il est
évident qu'en cas de demande excessive, il n'est plus possible
de servir tout le monde et certains consommateurs sont
prioritaires... Cette analogie est peut-être valable pour
expliquer la constance de débit encéphalique mais elle
échoue pour tous les autres paramètres....
Nous représenterons le modèle en utilisant le formalisme qui me semble avoir été proposé par M. Hervé, IPR, notamment dans les ouvrages de l'éditeur Hatier.
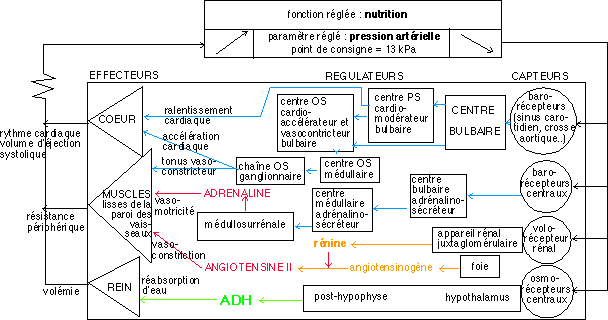
Un modèle que je perçois comme de plus en plus faux.....il cache le fonctionnement coordonné du vivant.
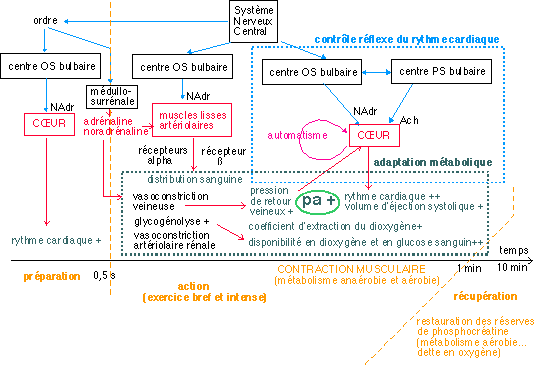
b. un modèle interne : la pression artérielle est une des composantes du travail du vivant
Selon ce formalisme, la pression artérielle est un
paramètre soumis aux deux systèmes principaux de
contrôle mais ce n'est pas le paramètre qui est
contrôlé mais bien les fonctions: on peut cependant
garder le formalisme des flèches qui indiquent non plus une
information mais une réelle CAUSALITE : une relation de cause
à effet.
Comme dans tout modèle il faut simplifier : je pense donc que
dans les deux exemples ci-dessous, plutôt que de vouloir
représenter tous les paramètres, il est plus judicieux
de ne présenter que ceux qui sont essentiels :
c'est-à-dire ceux qui suffisent pour prédire les
variations physiologiques...
la pression artérielle comme variable de l'adaptation au
milieu : exemple : régulation lors d'un effort physique bref
et intense (type course ou bicyclette).
Déjà, à l'échauffement (ou même
sans mouvement), le cœeur se prépare à l'effort en
augmentant le rythme cardiaque (un contrôle du système
nerveux central) , de même de l'adrénaline est
secrétée par la médullosurrénale et elle
commande une vasomotricité différente selon les
territoires... Lors de l'effort, la pression artérielle
augmente peu par contre le débit sanguin intramusculaire, le
rythme cardiaque et le volume d'éjection systolique ainsi que
l'extraction du dioxygène, sont les facteurs les plus
augmentés. Après l'effort, la pression
artérielle tend à chuter, le rythme cardiaque n'est
abaissé que progressivement, ainsi que le débit au
niveau des muscles (nécessaire notamment à
l'évacuation de l'acide lactique et des autres déchets
du métabolisme...) et le débit au niveau de la peau
(nécessaire à l'évacuation de la chaleur de
contraction)...
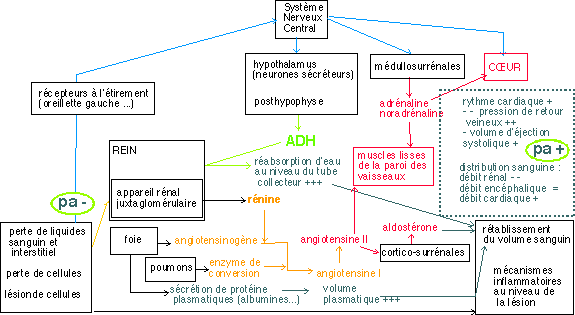
la pression artérielle comme variable de interactions entre populations cellulaires : exemple : régulation lors d'une hémorragie
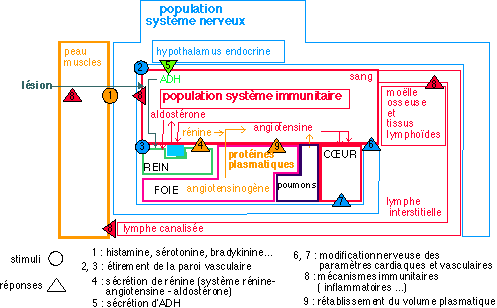
On considère que les hypertensions interviennent dans (causent directement ou indirectement) 170.000 décès par an en France en favorisant les maladies cardiovasculaires, les accidents vasculaires cérébraux et les insuffisances rénales. Je vous renvoie à la double page du Nathan qui est bien assez documentée pour moi (p 66-67 du livre de spécialité SVT).
On sort sans aucun doute ici du domaine de la science
expérimentale pour à nouveau entrer dans le domaine de
la médecine.
Je profite donc de cette occasion pour rapeller quelques points :
la science expérimentale (ici la physiologie humaine
pour ce chapitre) essaye de s'affranchir des variations
individuelles pour trouver des mécanismes
généraux (modèles internes et externes...)
l'éthiologie cherche au contraire à
étudier les variations individuelles pour établir
une norme (limites dans lesquelles peuvent varier
les paramètres étudiés sans que les individus
soient malades) puis rechercher les causes de
ces variations individuelles. Des normes sont établies
ainsi en fonctions de populations selon différents
critères d'âge, de sexe, de localisation
géographique, de patrimoine culturel, de catégorie
socio-professionnelle, d'origine géographique, voir de
critères génétiques...
On peut prendre comme exemple un article récent :
L'hypertension chez les noirs d'amérique, Richard Cooper,
Charles Rotimi et Ryk Ward, 1999, Pour le Science, n°258, avril
1999... dans lequel on a semble-t-il un mélange de tous ces
critères. Je ne sais trop comment formuler ce que je ressens
en face d'un tel amalgame de bons sentiments , de méthodes
inadaptées à mon sens (aller recherche un allèle
de l'angiotensinogène dans certaines populations noires et
blanches d'afrique et d'amérique sur des échantillons
forcément extrêmement limités.... je vous renvoie
à nos discussions sur la liaison entre le génotype et
le phénotype)... ce qui me gêne le plus est que l'on
essaye de nous faire croire qu'il s'agit de science
expérimentale, alors qu'à mon avis on est dans un tout
autre domaine, à la fois médical, sociologique et
surtout économique.