|
D'après le
programme: «Seule est étudiée la
régulation de la glycémie à court terme
après un jeûne de courte durée ou
après un repas. L'intégration de la
glycémie dans des boucles de régulation plus
complexes, sous-tendant des processus de régulation
à long terme, ne fait pas partie du
programme». |
Sources: |
||||||||||||||||||||||||||||
|
Plan |
|||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Dans le but d'étudier l'intégration (ou coordination) des travaux du vivant, le programme de 1èreS, dans la continuité de celui de la classe de 2nde, nous demande de traiter le travail de nutrition. |
(voir cours de seconde, partie 2. Il existe deux grands types trophiques: l'autotrophie (se nourrir seul) et l'hétérotrophie (ou plutôt l'allotrophie - se nourrir des autres) ) |
||||||||||||||||||||||||||||
|
La glycémie est la concentration en glucose du sang. |
Sa valeur moyenne (mesurée dans les veines du bras) oscille entre deux valeurs extrêmes habituelles: 0,8 g.L-1 et 1,2 g.L-1 (soit 4,2 mmol.L-1 à 5,7 mmol.L-1). |
Localement, elle peut atteindre des valeurs un peu plus faibles et nettement plus élevées (jusqu'à 50 mmol.L-1 soit 9,6 g.L-1). |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
page complémentaire: |
Éléments de biochimie pour les élèves de 1ère S avec Jmol - applet java - pour simualiser les molécules) |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
C1 - Le glucose est
la forme circulante de l'énergie entre
cellules
|
|||||||||||||||||||||||||||||
|
Le glucose est la forme circulante (de cellule à cellule) de l'énergie chez les pluricellulaires (comme l'ATP est la forme intracellulaire de transfert de l'énergie chimique de liaison). |
Le glucose est présent dans le sang et la lymphe (interstitielle) à des taux variables mais qui reflètent l'activité et l'état physiologique de l'organisme. |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
La nourriture est formée de matière et d'énergie. |
* En ce qui concerne la source de matière, nous avons vu en seconde (voir cours de seconde, paragraphe 1.5) que les animaux sont hétérotrophes car ils utilisent une nourriture "organique", ou mieux encore qu'ils sont allotrophes car ils consomment d'autres êtres vivants (des proies vivantes ou mortes). Les matières organiques et minérales (voir cours de seconde pour une discussion sur ces termes impropres) qui arrivent dans l'organisme (dans le milieu intérieur, c'est-à-dire entre les cellules) sous forme de nutriments sont variées (voir page complémentaire). |
* De même nous avons vu que les animaux sont chimiotrophes du point de vue de leur source d'énergie car ils puisent leur énergie dans l'énergie chimique des substances organiques qu'ils consomment. Nous allons voir que c'est le glucose qui est la principale source d'énergie chimique des cellules des animaux. |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Les nutriments sont variés (glucides simples, aa, glycérol et acides) mais peuvent tous être transformés en glucose, principalement par le foie (néoglucogénèse). |
L'alimentation étant discontinue
alors que l'utilisation du glucose par les cellules est
continue, il existe des formes de stockage du glucose. |
Le glycogène est la forme de stockage la plus facilement et rapidement mobilisable (même en absence d'O2) même s'il prend plus de place que les lipides. Les lipides sont une forme de stockage énergétiquement plus dense mais moins facilement utilisable et surtout qui demande la présence de dioxygène. |
|||||||||||||||||||||||||||
|
(in
Schmidt-Nielsen, p173) |
Le glycogène
(présent chez les animaux
(vertébrés et invertébrés) mais
aussi chez les champignons)
présente une masse dix fois plus importante que les
lipides |
Si l'amidon est une forme habituelle de stockage énergétique chez les plantes, les protéines et les graisses sont aussi mises à contribution dans les graines par exemple. |
|||||||||||||||||||||||||||
|
Remarques importantes: |
Si les cellules nerveuses et les hématies ne consomment que du glucose, la plupart des cellules peuvent consommer des acides gras circulants et certaines consomment aussi des acides aminés circulants à des fins énergétiques dans des conditions particulières. |
||||||||||||||||||||||||||||
|
Mais: |
* les acides gras (A.G.) ont un rôle énergétique principal de réserve. Leur utilisation comme nutriment énergétique ordinaire est secondaire (sauf chez certaines cellules notamment du foie et du rein) ou tout au moins partagé avec des rôles essentiels structuraux (constituants principaux des membranes, couches protectrices thermiques...) et fonctionnels (l'acétyl coenzyme A (produit de la dégradation des acides gras) est un carrefour métabolique dans la cellule, synthèse d'hormones...); |
* le taux sanguin et surtout le taux de la lymphe en A.G. est très variable selon les apports alimentaires et les particules lipidiques sanguines sont captées rapidement par le tissu adipeux, le foie, le cœur et les autres muscles (voir cours général sur la nutrition humaine). Il n'y a pas de régulation de la lipidémie comme on l'observe pour la glycémie, notamment parce que les formes de transport des lipides sont variées; |
* les acides aminés issus
des protéines alimentaires digérées ne
sont pas stockés dans l'organisme mais
utilisés par les cellules pour construire (et
renouveler) leurs propres protides; certains aa sont
synthétisés par les cellules. Ce n'est qu'en
cas de jeune prolongé (ou d'une alimentation
déséquilibrée beaucoup trop riche en
protides) que les aa sont consommés en grande
quantité comme substrat énergétique,
notamment dans les muscles. Le foie peut synthétiser
du glucose à partir de certains aa dits
gluco-formateurs (les réactions font partie de
la néoglucogénèse). |
||||||||||||||||||||||||||
|
C2 - Analyse de courbes et d'expériences: les faits expérimentaux |
|||||||||||||||||||||||||||||
|
Les expériences s'insèrent bien sûr dans une théorie (voir méthode) mais il n'est pas rare que lorsque les théories changent les résultats expérimentaux soient réinvestis d'une nouvelle explication dans le cadre de la nouvelle théorie. Parfois les résultats sont si anciens que les théories sont méconnues, n'étant plus accessibles autrement que par des recherches historiques. |
Je renvoie aux méthodes d'analyse de courbes et données acquises en seconde et à la page sur les mathématiques en SVT vue en classe de seconde. |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
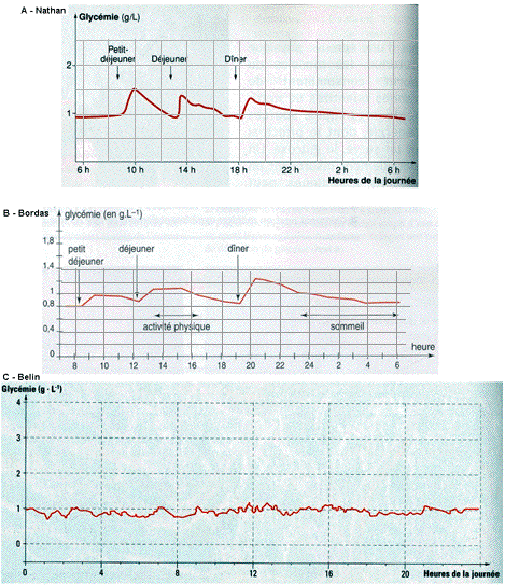
Courbes de
références: glycémie ordinaire
journalière mesurée toutes les 15 min |
Les différences dans ces trois courbes scolaires sont difficiles à comprendre (et je n'en ai pas toutes les clés... quand aurons-nous de véritables documents physiologiques et non des courbes redessinées ?) Elles ne peuvent se comprendre que si le message choisi est différent et que les conditions de mesures sont différentes. A et B cherchent peut-être à mettre en évidence une régulation (c'est-à-dire un retour à la normale après des activités impliquant une variation dans un sens ou dans l'autre); C insiste peut-être davantage sur le côté permanent de cette régulation. Il est indispensable de connaître les conditions physiologiques dans lesquelles les mesures ont été faites: nombre de patients, état nutritionnel, âge, sexe, activités, lieu et méthode de mesure, incertitude... Sans de nombreuses mesures chez de très nombreux individus et dans des conditions physiologiques très différentes, il est FAUX de chercher à déduire de ces courbes que la glycémie est un paramètre maintenu stable (autour d'une valeur moyenne dite valeur physiologique) par l'organisme, en dépit des causes de variation . En ce sens une courbe moyenne sur de très nombreux individus est la seule pertinente; ou encore mieux de très nombreuses valeurs dans un tableau permettant une véritable analyse. |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Il est FAUX de dire que ces courbes prouvent la régulation. Seuls les repas font sensiblement augmenter la glycémie et le retour à la valeur physiologique est très lent (plusieurs heures). L'exercice, même si les courbes ne le présentent pas ici comme un paramètre séparé, ne provoque pas de baisse de la glycémie. Ces courbes justifient l'emploi du terme stabilité. |
|||||||||||||||||||||||||||||
|
Comment donc formuler de façon rigoureuse - sans tomber dans la "caricature mécanique" (les philosophes parlent de mécanicisme) - que l'organisme présente une valeur physiologique stable (et non pas constante) ? Le meilleur moyen est de revenir à la notion de fonction. |
|||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Il n'y a donc pas de "fonction glycémique" mais bien une "fonction nutritive". |
Il n'y a pas de "régulation de la glycémie" mais "une fonction nutritive de type homéostatique" dont la glycémie est un paramètre. |
C'est ce que nous allons expliquer. |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Le terme de fonction est aussi très riche de sens. Il a probablement une origine biologique et sociologique (cette idée n'a été soutenue que tardivement par René Thom; voir Analyse sémantique d'un mot polysémique: la fonction, 1993, Séminaires de la Société de Biologie Théorique, année 1992-1993, Acta Biotheoretica, 42 ), puis qui a été formalisée en mathématique (dans le plan, la fonction (numérique) d'une variable (x) est représentée par un graphe y=f (x); en mathématique la représentation d'une relation de quantité (avec des variables numériques) ou de qualité entre deux ensembles d'objets est défini par le terme moderne d'application (Fréchet, 1909)) , et enfin est retournée dans le domaine social et dans celui de la biologie. |
La vie est un processus fonctionnel.
Classiquement on parle des trois grandes fonctions du
vivant: se nourrir, communiquer et se reproduire.
Personnellement je préfère la notion de
travail, plus riche (voir cours
de seconde) que je formule ainsi:
"la vie est un travail de relation, de nutrition et de
reproduction". |
La compréhension du monde vivant a
toujours été associé à celui de
l'homme d'abord et des sociétés humaines
ensuite. Fonctionnalisme et
organicisme sont des termes utilisés en
sciences sociales pour désigner des théories
qui comparent les sociétés humaines avec le
fonctionnement d'un ou d'une partie d'un être vivant.
De nos jours on parle davantage de
sociobiologie. Claude Bernard lui-même,
en proposant de prendre l'organisme vivant comme
modèle de système dont les
sociétés humaines doivent s'inspirer, n'est
pas le moins illustre de ces savants qui n'hésiteront
pas à prétendre unifier leur
compréhension du monde dans une philosophie. |
|||||||||||||||||||||||||||
|
L'homéostase désigne l'état d'équilibre intérieur d'un organisme face à des modifications du milieu extérieur. |
|||||||||||||||||||||||||||||
|
La racine latine homœo orthographiée homéo en français viendrait du grec homolos (= semblable) et n'est donc pas différente de la racine homo. C'est le physiologiste anglais W. B. Cannon qui forga ce mot vers 1932 en réunissant deux racines grecques: homœo et stasie (= position). |
On emploie indifféremment homéostase (qui se rapporte à l'état caractéristique: un système homéostatique est dit "en homéostase") ou homéostasie (qui désigne plus particulièrement la propriété d'un système). |
Remarque : |
|||||||||||||||||||||||||||
|
La notion de régulation, empruntée à la mécanique, est plus ancienne, et date d'au moins la fin du XVIIIème. Actuellement la régulation est le maintien du fonctionnement d'un système (souvent avec le sens d'une conformité à une norme, ce qui est nettement plus délicat à employer en biologie - voir l'introduction du cours sur la pression artérielle). Je ne recommande donc pas son emploi. |
|||||||||||||||||||||||||||||
|
Je rappelle le premier principe dynamique du vivant vu en classe de seconde: |
Remarque: |
||||||||||||||||||||||||||||
|
« un être
vivant est un système homéostatique ou en
homéostase » |
|||||||||||||||||||||||||||||
|
Raisonner en terme de fonction c'est aussi raisonner en terme de finalité, de sens (et donc répondre à la question "pourquoi ?"), et pas uniquement en terme de mécanisme (que l'on peut supposer répondre à une question utilisant l'adverbe comment). |
Pourquoi
maintenir une glycémie stable ?
A quoi cela
sert-il ?
Dans quel but
l'organisme maintient-il ce paramètre stable
? |
||||||||||||||||||||||||||||
|
La fonction maintenue stable (donc homéostatique), - malgré la période d'activité ou de repos (ce qui est net), - malgré l'effort (ce qui est très net), - malgré les repas (ce qui est moins net si l'on se contente de mesurer la glycémie à la veine du bras mais beaucoup plus net si on mesure la glycémie au niveau artériel céphalique par exemple) est donc la fonction de nutrition des cellules. |
|||||||||||||||||||||||||||||
|
La question qu'il faudrait se poser,
et dont la réponse dépasse bien sûr le
cadre d'un cours de 1ère S, est de
savoir comment l'homéostase est
réalisée (Thom dirait
"déployée") dans l'espace de
régulation qui contient tous les
états de tous les paramètres liés
à la fonction maintenue.
|
On remarquera que l'on peut ainsi parler d'homéostase cellulaire, populationnelle, sociale... |
||||||||||||||||||||||||||||
|
Courbes et expériences: |
- mesure du glycogène
hépatique après 3 repas sur 15 h (Nathan,
151-2a) |
- mesure de la glycémie à
la suite de l'injection de 20 mL de glucose à 5% dans
l'artère afférente au pancréas d'un
chien (bac) - taux de réabsorption
rénale du glucose (BG1-2002 p 145 -3) - différents récepteurs au glucose dans les cellules humaines (BG4-2001 p 774 -2) |
|||||||||||||||||||||||||||
|
C3 - Une application du principe d'homéostasie à la nutrition du tissu nerveux |
|||||||||||||||||||||||||||||
|
Dans le cadre de ce cours, et pour faire simple, mais bien sûr de façon non exhaustive, juste comme un exemple, on pourrait dire que la glycémie est la variable de l'homéostase énergétique du tissu nerveux. |
Le glucose sanguin assure en effet l'équilibre énergétique nécessaire aux cellules nerveuses, puisqu'elles ne peuvent faire de réserves de nutriment énergétique. |
||||||||||||||||||||||||||||
|
C3.1 - la glycémie est la variable de l'homéostase énergétique du tissu nerveux |
|||||||||||||||||||||||||||||
|
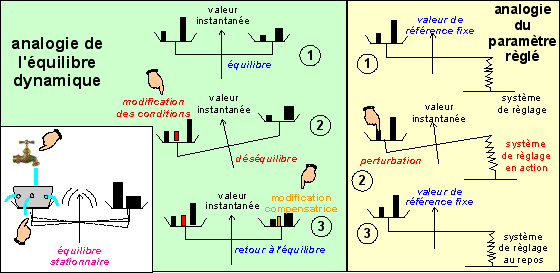
L'homéostase étant basée sur une analogie mécanique on peut présenter deux représentations simples: |
|||||||||||||||||||||||||||||
|
|
Selon le niveau d'observation où
l'on se place, on peut préférer l'une ou
l'autre des représentations: |
||||||||||||||||||||||||||||
|
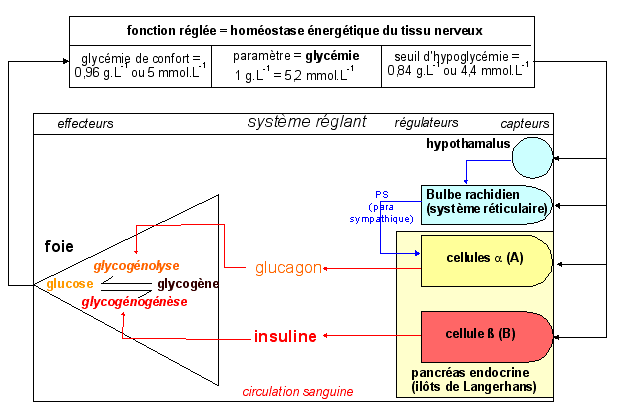
* modèle classique Pour décrire le système de régulation le formalisme habituellement proposé dans l'enseignement secondaire et issu de la cybernétique (voir ci-dessus) comporte deux rectangles (fonction réglée - système réglant), où l'on place les capteurs, régulateurs et effecteurs. |
|||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Dans cet exemple l'insuline et le glucagon sont clairement antagonistes quand à leur fonction hypo et hyperglycémiante. On notera que l'insuline possède, à l'inverse du glucagon, de nombreuses autres cellules cibles (et de nombreuses autres fonctions, que nous verrons ensuite) que les cellules hépatiques. Les cellules alpha et ß sont des capteurs sensibles à la glycémie du sang qui perfuse le foie. On notera aussi que, même si elle n'est pas représentée, la commande nerveuse existe aussi bien pour les cellules alpha que ß. Globalement la stimulation du système parasympathique active la libération de glucagon et inhibe la sécrétion d'insuline alors que celle de l'orsthosympathique a un effet antagoniste (voir système nerveux végétatif). |
Remarque: |
||||||||||||||||||||||||||||
|
Ce qui est profondément frustrant avec le schéma précédent c'est que le tissu vivant, qui consomme le glucose, semble ici étranger au système de régulation. Celui-ci est en quelque sorte extérieur au système: des organes contrôlent la fonction de nutrition d'autres organes. Alors que je pense que l'organisme fait un tout (la vie est une propriété non locale et c'est tout le travail d'une biologie théorique d'en montrer des propriétés ou fonctions locales). |
Je pense que le système vivant est à la fois celui qui consomme et celui qui règle la consommation ou du moins qu'il fait partie du système réglant. C'est pour cela que je préfère une modélisation globale du système sans se préoccuper de savoir qui règle et qui consomme. Le système vivant est alors une boîte noire qu'on renonce à ouvrir (du moins ouvrir "totalement", mais on peut avoir plusieurs niveaux d'approche) et dont on regarde le fonctionnement de l'extérieur en faisant varier quelques paramètres de contrôle (voir aussi une page en travaux pour une autre présentation et davantage de références). |
Je tiens à souligner combien cette partie est encore "prospective". |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Des conditions expérimentales au modèle: |
- la glycémie artérielle afférente au niveau du tissu nerveux céphalique correspond à un point stable dans le temps (qui résiste à de petites perturbations venant de l'activité (repos-effort), de la prise alimentaire (repas, jeune court...), de l'état physiologique (fièvre...), des phases veille-sommeil....). |
- ce point est considéré comme une singularité d'une application définie dans un espace de grande dimension qui représente le métabolisme. Ce point est appelé un point catastrophe. |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
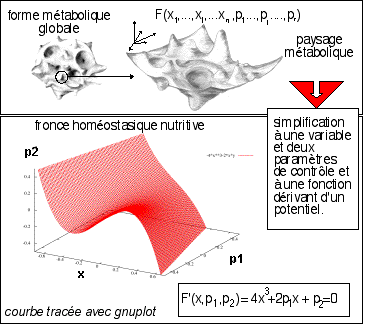
Faute de pouvoir connaître de la figure complète du métabolisme, l'idée est de réduire le problème, par des approximations simples, à un nombre de paramètres qui permette de le solutionner. C'est l'inestimable découverte de René Thom que d'avoir montré que non seulement le problème peut avoir des solutions mais qu'elles sont SIMPLES (géométriquement exprimées), en PETIT NOMBRE (7), TRÈS GÉNÉRALES (on peut faire des parallèles avec d'innombrables domaines des mathématiques ou de la physique). Tout phénomène présentant une singularité (un lieu où il se passe quelque chose de singulier(de discontinu) sur un fond continu), pour peu que l'on prenne les hypothèses simplificatrices exposées ci-dessous, peut s'expliquer, mathématiquement, à l'aide de ce que l'on a appelé la Théorie des catastrophes. |
On considère que le
phénomène étudié est
représenté par une fonction de
RnxRN : F(p1, ...,
pn, x1, ..., xN); les
pi étant les paramètres
externes, accessibles à l'expérimentateur,
et les xj, les variables internes, non
acessibles (on peut observer leur valeur mais pas les fixer
expérimentalement: ce sont elles qui sont
associées au phénomène observable).
Dans le cas d'un espace avec n æ 4 et N æ 2 René Thom
a prouvé, par des calculs non accessibles à
des non mathématiciens (c'est la notion de
déploiement universel d'une singularité
différentiable), qu'il existe 7 catastrophes
élémentaires et seulement 7. |
Je précise que tous ces modèles correspondant à des dynamiques, le temps est toujours un paramètre présent mais qui n'est représenté qu'à travers les autres paramètres de contrôle (ce n'est pas le temps qui agit, il n'est qu'une mesure de la vie... c'est une durée très bergsonienne). Au point catastrophe il existe un attracteur (au sens mathématique, voir page sur les modèles) du métabolisme dont la structure et la topologie reflètent la fonction biologique en ce point. |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
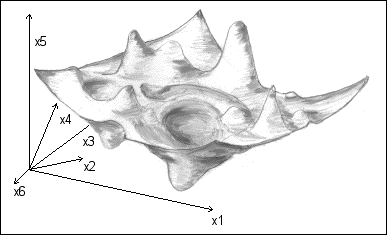
la forme métabolique imaginaire.... |
un détail... |
||||||||||||||||||||||||||||
 |
|
||||||||||||||||||||||||||||
|
Le métabolisme d'un organisme (au niveau de certaines fonctions locales qui le décrivent) est stable par rapport à de petites variations. Il peut donc être représenté par une FORME dans une ESPACE DE GRANDE DIMENSION (voire de dimension infinie). |
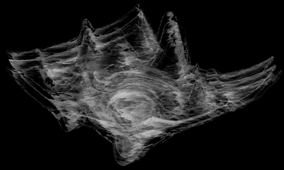
Une "représentation" du paysage épigénétique de Waddington repris par Thom comme figure de régulation métabolique de l'organisme dans un espace de grande dimension (non représentable... donc, évidemment, pour ce schéma le nombre de dimensions est de 3 même si 6 axes imaginaires sont indiqués) et les formes sont "lisses" alors qu'on les imagine très complexes. |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Conrad Hall Waddington, dans les années 1960, avait introduit la notion de paysage épigénétique « epigenetic landscape » comme un arbre de trajectoires descendantes du haut d'une colline hémisphérique pour décrire des évolutions divergentes des tissus embryonnaires. Cette figure a été reprise par Thom et voici sa traduction en motif en creux et bosses, les points les plus bas indiquant des points de stabilité des fonctions locales (un attracteur en mathématiques), les points élevés des domaines d'instabilité (bifurcation). La forme générale en creux étant une image de la fonction globale, par exemple ici la nutrition. La stabilité du paysage dans le temps et par rapport à de petites variations des paramètres de contrôle est une caractéristique importante de cette figure métabolique. |
Une image..... d'un paysage stable malgré les petites déformations.... |
||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
La figure globale du métabolisme est INACCESSIBLE de par sa complexité (nombre de variables) mais l'on peut dans chaque cas concret, FAIRE DES APPROXIMATIONS et réduire les variables à un nombre accessible à une résolution géométrique (3 ou 4). |
L'approximation la plus importante étant que la fonction du vivant étudiée localement en un point DÉRIVE D'UN POTENTIEL (noté F ou V selon les pages) et que l'on peut donc utiliser l'outil des équations différentielles. (voir page annexe) |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
Pour avoir un puits de potentiel présentant une symétrie selon deux directions opposées il faut envisager au moins deux paramètres externes p1 et p2 qui pourraient être (p1) le flux entrant de glucose dans la circulation (absorption du glucose par apport alimentaire, déstockage hépatique...) et (p2) le flux sortant de glucose de l'appareil circulatoire (par la consommation en glucose globale de l'organisme - qui pourrait rendre compte de l'activité musculaire principalement en s'efforçant de considérer que tous les autres paramètres sont fixes). |
La glycémie n'est plus alors un
paramètre mais bien une sortie (x) non
contrôlable mais observable. x est la
morphologie du système, stable face
à de petites perturbations ; on pourrait
aussi dire que c'est la réserve glucidique
sanguine ou le flux glucidique sanguin. Je
voudrais ainsi modifier la vision habituelle des
physiologistes qui, quand ils affirment que la
glycémie est stable ou contrôlée, y
voient un système cybernétique avec un
système de contrôle plus ou moins
localisé dans le système nerveux central et
nécessitant des capteurs et des
régulateurs. |
Attention ! ce qui est difficile à saisir est que, de façon inhabituelle, F(x) ne désigne pas le résultat observé mais c'est x qui est le résultat, la fonction reste cachée et F n'en est qu'un modèle. Pour "voir" le comportement du système il ne faut pas "regarder" les F(x) mais les x seulement. Les surfaces (qui donnent leur nom à la catastrophe) ou les courbes (projections ou ensemble de bifurcations) représentant les points singuliers de F (points catastrophiques) nous permettent de visualiser les différentes valeurs critiques de x en fonction des paramètres de contrôle (on approche ainsi ce que l'on appelle la structure de l'attracteur (ou des attracteurs): figure mathématique qui explique la stabilité de la fonction). Il ne faut donc pas confondre la forme du potentiel (qui approche la fonction cachée) et la forme de l'attracteur (ou des attracteurs en conflit) qui est représentée par l'ensemble des catastrophes. |
|||||||||||||||||||||||||||
|
On considère alors que la fonction de nutrition cachée dans la boîte noire du vivant est un potentiel que le vivant stabilise (minimise) par homéostasie. Ce potentiel à pour expression Fp1,p2(x)= (x**4) + p1*x**2 + p2*x (* représente l'opérateur multiplication et ** l'opérateur puissance). On ne peut pas représenter directement (en dimension 4) la fonction Fp1,p2(x) donc on se contente (en dimension 3) de la surface des points de l'espace de contrôle pour lesquels sa dérivée est nulle: c'est à dire F'p1,p2(x) = 0 ; et donc 4*x**3 + 2*p1*x + p2 = 0. Cette surface est une
fronce (cusp en
anglais) en rouge
ci-contre.
|
|
||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
L'intérêt de tels modèles réside dans leur efficacité compréhensive même si l'efficacité expérimentale est encore limitée (plus par manque d'utilisation que par défaut intrinsèque il me semble). On remplace une vision mécaniciste et matérialiste quasi magique du vivant par une vision pragmatique ouverte mais formalisée mathématiquement. |
Au lieu de dire que la physiologie de l'être vivant constitue un équilibre dynamique (ce qui n'explique rien et n'est en rien justifié si ce n'est par l'efficacité expérimentale du modèle, toute relative (que l'on s'interroge sur la notion d'hormone, très dépassée, qu'il serait possible d'intégrer dans un paramètre plus large de type informationnel, stimulant ou inhibiteur, d'un système; la concentration de la substance informationnelle (médiateur) n'étant plus qu'un paramètre - en relation avec beaucoup d'autres - de l'état du système), on formalise mathématiquement la fonction vitale en clarifiant les approximations faites et les conditions de validité (la fonction vivante modélisée dérive d'un potentiel et la vie consiste à minimiser ce potentiel). |
Cette modélisation est vraiment un travail scientifique et je crois que ce travail (pas mes petites explications bien sûr, mais les travaux des chercheurs autour des modèles thomiens) de biologie théorique est promis à un grand avenir. |
|||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
C3.2 - la glycémie est une variable de nombreuses fonctions |
|||||||||||||||||||||||||||||
|
L'essentiel des
données de cette partie proviennent du
Précis de Physiologie
publié chez Doin. |
|||||||||||||||||||||||||||||
|
Lors d'un repas ou d'un effort la glycémie varie fortement selon le point de mesure dans l'organisme. De nombreux mécanismes sont mis en jeu pour stocker les nutriments dans le premier cas et les mobiliser dans le second, et ils interfèrent fortement avec la variable glycémique. Présenter la physiologie de ces régulations conduit à des schémas trop complexes qui n'apportent à mon avis pas grand chose. |
Dans le cas d'un repas, d'un effort, d'un stress,..., la glycémie n'est qu'une variable parmi tant d'autres qui représente des fonctions très diverses aux très nombreux paramètres. |
Pour ces fonctions la glycémie n'est pas une variable stabilisée d'une façon globale (partout dans l'organisme) mais peut l'être localement comme c'était le cas pour la fonction énergétique nutritive du tissu nerveux. |
|||||||||||||||||||||||||||
|
C3.2.1 l'insuline est à la fois l'hormone du stockage du glucose et l'hormone de l'utilisation du glucose |
|||||||||||||||||||||||||||||
|
Nature chimique:
|
Synthèse:
|
||||||||||||||||||||||||||||
|
L'insuline est une hormone peptidique de 51 aa (deux chaînes (A et B) de 21 (n°66 à 86-COOH) et 30 (n°1-NH2 à 30) aa réunies par deux ponts disulfure (entre les aa n°7-72 et 19-85)) de poids moléculaire voisin de 6000 daltons (5733 daltons pour l'insuline bovine; un dalton (Da) est la masse de l'atome d'hydrogène: 1,7. 10-23 g). |
L'insuline est synthétisée
par les cellules ß des îlots de Langerhans
pancréatiques. |
||||||||||||||||||||||||||||
|
Modes d'action : |
|||||||||||||||||||||||||||||
|
Comme toutes les hormones protéiques elle se fixe à un récepteur membranaire au niveau de ses cellules cibles. Deux mécanismes d'activation sont évoqués : |
*Les complexes récepteurs membranaires-hormone se rassemblent dans une même région de la membrane qui s'invagine puis forme une vésicule (endocytose) qui pénètre dans la cellule. La vésicule est désagrégée par les lysosomes et l'hormone est libérée à l'intérieur de la cellule et active des systèmes enzymatiques cytoplasmiques. Ce mécanisme est notamment invoqué pour l'augmentation du nombre de récepteurs au glucose (GLUT 4) médiée par l'insuline chez certaines cellules (voir plus bas). |
* La liaison hormone-récepteur active sur la face cytoplasmique du complexe hormone-récepteur un système métabolique (dans le cas de l'insuline il s'agirait d'une activité enzymatique de type tyrosine kinase (commune chez les facteurs de croissance), c'est-à-dire que des molécules de substrats cytoplasmiques pourraient être phosphorylées au niveau de l'aa tyrosine, ce qui modifierait leur activité) que l'on peut qualifier de message hormonal ou message endocrine (message transporté par un médiateur endocrine ou hormone, en provenance des cellules endocrines, et dirigé vers la cellule cible). |
En fait, comme la cellule cible ne peut être considérée comme demandeuse d'information, le terme même d'information est probablement inadéquat, bien que consacré par l'usage (voir remarque du cours de Spécialité de TS). Les termes de médiateur et message sont peut-être plus exacts mais non moins porteurs d'idéologie. |
||||||||||||||||||||||||||
|
Fonctions (rôles): |
|||||||||||||||||||||||||||||
|
L'insuline possède principalement trois fonctions, c'est-à-dire trois rôles qui diffèrent selon les cellules cibles, leurs récepteurs et leur métabolisme. On pourrait dire que l'insuline est un message hormonal qui a plusieurs sens (non incompatibles) et une valeur (toujours hypoglycémiante) : |
* sur les cellules hépatiques,
musculaires et adipeuses , particulièrement
sensibles à l'insuline, l'insuline a une
fonction de stockage (du glucose circulant
mais aussi d'autres nutriments comme les aa ou les
lipides). L'insuline augmente la
glycogénogénèse musculaire et
hépatique, ainsi que la lipogénèse
adipeuse et hépatique. L'insuline inhibe par contre
la glycogénolyse hépatique et musculaire ainsi
que la lipolyse adipeuse et musculaire.
|
* sur les cellules musculaires et adipeuses l'insuline a une fonction de pénétration facilitée du glucose (mais aussi des AG pour les adipocytes). En effet, certaines cellules, comme les cellules nerveuses, mais aussi les cellules hépatiques, sanguines et les cellules du pancréas endocrine, sont naturellement très "ouvertes" au glucose (elles possèdent de nombreux récepteurs au glucose, de type GLUT 1, GLUT2 et GLUT 3, voir par exemple Roger Raynal, Biologie-Géologie n°4-2001 p 774 , fig 2). Mais les cellules musculaires et adipeuses sont normalement peu "ouvertes" au glucose c'est-à-dire que sans insuline, le glucose pénètre peu (les récepteurs au glucose (de type GLUT 4) sont peu nombreux) et elles ne consomment que peu de glucose. Par contre, en présence d'insuline (on les qualifient alors d'insulino-dépendantes), le glucose pénètre en grande quantité dans ces cellules (par augmentation du nombre de transporteurs membranaires de type GLUT 4 suite à l'activation de la transcription traduction des gènes de ce récepteur au glucose mais aussi à l'exocytose transitoire (suivie d'une endocytose dès que l'action de l'insuline cesse) de vésicules dont les membranes portent ces récepteurs - voir "Transport du glucose dans la cellule musculaire" dans l'EU, article "histologie" ou sur internet http://hometown.aol.com/_ht_a/drfatalis/Images/recrute.gif ) et l'utilisation du glucose y est fortement stimulée (glycolyse). Le glucose pénétrant dans une cellule y est immédiatement phosphorylé (transformé en glucose-6P). C'est le glucose-6P qui est le métabolite de départ des réactions de respiration ou fermentation cellulaire (par la glycolyse commune à ces mécanismes). La déphosphorylation ne peut être réalisée que dans le foie car les hépatocytes sont les seules cellules à posséder une glucose-6 phosphatase qui transforme le glucose-6P en glucose (les cellules rénales, parmi d'autres rares cellules, la possèdent aussi) et la membrane est imperméable aux composés phophorylés. L'insuline favorise l'entrée des AG circulants dans les adipocytes. |
|||||||||||||||||||||||||||
|
Remarque: L'insuline peut aussi être
considérée comme un facteur de
croissance. L'insuline est une
hormone dont on n'a pas fini de découvrir les
rôles. Elle active notamment la prolifération
et la croissance cellulaires in vitro et une famille
de facteurs de croissance lui est rattachée (IGF:
insulin-like growth factors) avec une nature
protéique, une structure et un mode d'action communs.
|
|||||||||||||||||||||||||||||
|
C3.2.2 le
glucagon est l'hormone des besoins en glucose
(hyperglycémiante)
|
|||||||||||||||||||||||||||||
|
Le glucagon est un petit peptide de 29 aa (3500 Da) sécrété (à partir d'un précurseur de 9000 Da) par les cellules alpha (A) situées à la périphérie des ilôts de langerhans (à partir d'un gène situé sur le bras long du chromosome 2) sous commande endogène (des propres cellules alpha) ou nerveuse (hypothalamique et bulbaire). |
Les cellules cibles sont les cellules hépatiques pourvues de récepteurs membranaires au glucagon. La fixation du glucagon à son récepteur active un système métabolique assez général (notamment par la synthèse d'AMP cyclique à partir de l'ATP) et conduit à une stimulation de la glycogénolyse et donc à la libération du glucose dans le sang (puisque les cellules hépatiques possèdent une glucose 6 phosphatase... voir plus haut). Le glucagon stimule aussi la néoglucogénèse hépatique et inhibe la glycogénolyse dans ce même organe. Enfin il stimule la libération des acides gras par les triglycérides stockés dans les adipocytes, il favorise donc la lipolyse dans ces cellules. |
Le glucagon stimule aussi la
sécrétion d'insuline par les cellules ß
voisines: c'est ce que l'on appelle un effet
paracrine (médiateur chimique agissant
sur de courtes distances sans transport par le sang: voir
TP). |
|||||||||||||||||||||||||||
|
C3.2.3 lors d'un repas l'insuline est libérée pour favoriser le stockage du glucose |
|||||||||||||||||||||||||||||
|
Lors d'un repas riche principalement en glucides (et surtout de sucres lents, c'est-à-dire complexes, comme l'amidon), l'insuline est sécrétée avant tout pour favoriser le stockage du glucose. Si le repas est même composé uniquement de glucides (et surtout de sucres rapides, c'est-à-dire simples, comme le glucose ou le fructose...) il peut y avoir une hypoglycémie transitoire due à l'action hypoglycémiante de l'insuline. C'est aussi ce que l'on observe lors de l'injection de glucose expérimentale. |
Lors d'un repas équilibré en glucides, acides gras (lipides) et protides, insuline et glucagon sont sécrétées simultanément et la glycémie reste équilibrée: il n'y a pas d'hyperglycémie postprandiale. Cela ne signifie cependant pas que la glycémie est "régulée". C'est vraiment un exemple d'équilibre dynamique (ou d'homéostase) sans avoir besoin de faire intervenir un mécanisme de régulation autour d'une valeur fixe. |
Lors d'un repas riche pris alors que les réserves hépatiques ne sont pas épuisées la glycémie on observera par contre une hyperglycémie transitoire. du fait du temps de latence de sécrétion et d'action de l'insuline. |
|||||||||||||||||||||||||||
|
Nous avons vu (TD analyses de courbes) que les réserves hépatiques en glucose sont de l'ordre de 100 à 120 g, ce qui constitue une réserve suffisante pour 10 à 12 heures de sommeil ou de repos (5 g.h-1 de glucose consommé pour les cellules nerveuses et la même quantité pour toutes les autres cellules des tissus périphériques). Au réveil, si les réserves hépatiques sont épuisées il est important de les reconstituer par un "petit déjeuner" sinon l'organisme consommera des AG pour les tissus périphériques mais les cellules nerveuses ne consommant que du glucose, le foie sera obligé de fournir du glucose par néoglucogénèse (à partir des AG ou des aa). Lors d'une prise alimentaire intervenant alors que la néoglucogénèse fonctionne, on observe une assez forte hyperglycémie étant donné que l'insuline met près de 2h à inhiber la néoglucogénèse. La vue et l'odorat sont déclencheurs d'une faible sécrétion d'insuline qui prépare le foie au stockage du glucose. Des stimuli mécaniques buccaux et gastriques provoquent ensuite une sécrétion d'insuline plus importante. Enfin, par voie hormonale, le transit intestinal stimule aussi les sécrétions pancréatiques. |
|||||||||||||||||||||||||||||
|
C3.2.4 lors d'un effort insuline et
glucagon sont libérés simultanément
pour permettre l'approvisionnement énergétique
des cellules musculaires et nerveuses
|
|||||||||||||||||||||||||||||
|
On a vu en classe de seconde que lors de l'effort l'organisme permet le travail musculaire grâce à une augmentation des débits ventilatoire et cardiocirculatoire. |
Le maintien d'un apport énergétique suffisant aux organes en fonctionnement n'est pas le seul fait des deux hormones étudiées ici. |
Lors d'un exercice bref c'est l'adrénaline qui est l'hormone principalement sécrétée. Les commandes sécrétoires d'insuline et de glucagon sont principalement nerveuses. |
|||||||||||||||||||||||||||
|
Un schéma des acteurs principaux (au programme de 1èreS) de la fonction d'homéostase nutritionnelle ou énergétique liée au glucose. 
|
|||||||||||||||||||||||||||||
|
Annexe |
|||||||||||||||||||||||||||||
|
http://www.ladocfrancaise.gouv.fr/brp/notices/044000493.shtml
(à
télécharger: le rapport Glucides et
santé : État des lieux, évaluation et
recommandations, AFSSA (Agence Française de
Sécurité Sanitaire des Aliments, octobre
2004); notamment ch 8, p 48 et annexe 4 : "index
glycémique", p 136).
|
|||||||||||||||||||||||||||||
|
Le glucose est absorbé sélectivement et activement (son absorption par les entérocytes consomme de l'énergie et peut atteindre une limite maximale) alors que le fructose est absorbé moins vite et à peu près proportionnellement à sa concentration dans la lumière intestinale. |
Pour de faibles quantités, le fructose est converti en glucose par les entérocytes mais pour de grandes quantités le fructose passe dans le sang et c'est dans le foie qu'il est transformé rapidement en glucose. Cependant la totalité du fructose peut ne pas être absorbée, et il peut donc être rejeté avec les excréments, ce qui n'arrive jamais pour le glucose. |
Le saccharose est hydrolysé en fructose et en glucose dans la lumière intestinale avant son absorption. Le glucose qui en résulte est absorbé encore plus rapidement que du glucose ingéré seul. |
|||||||||||||||||||||||||||
|
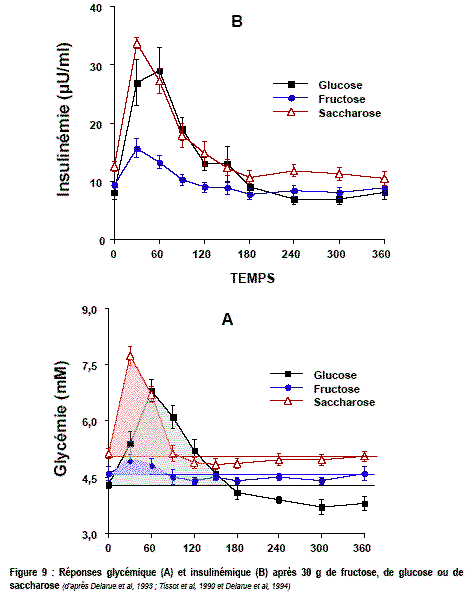
On utilise maintenant un indice appelé index glycémique pour évaluer la vitesse d'absorption d'un sucre (ou d'un aliment sucré) et la réponse glycémique de l'organisme. |
|||||||||||||||||||||||||||||
 (in rapport cité ci-dessus, modifié) |
L'index glycémique le plus utilisé est IGglucose qui est le rapport entre les aires d'hyperglycémie (fig.9 A) observées pour un sucre, à la suite de l'ingestion d'une quantité fixe de ce sucre (50g habituellement), et celle du glucose (en grisé ici), multiplié par 100. On utilise aussi la référence au pain de mie blanc soit IGpain. (Voir l'annexe de la référence de l'AFSSA pour les protocoles expérimentaux : quantité, durée et lieu des prélèvements sanguins (toutes les 30 min...), nombre de sujets...). (glucose =
100) fructose saccharose (glucose +
fructose) baguette purée de pomme de terre
instantanée Cornflakes, Kellogg's pain de mie blanc riz blanc Coca-Cola spaghetti pomme Le fructose ne provoque qu'une faible augmentation de la glycémie car sa présence dans la sang résulte principalement de sa transformation par le foie (la "fructosémie" maximale au niveau de la veine porte lors des tests (50g d'absorption de fructose ou de saccharose) ne dépasse pas non plus 2,2 mM, ce qui est une valeur faible). Il est en plus très facilement utilisé par les cellules du foie, du rein et de l'intestin. Le saccharose provoque une rapide mais fugace hyperglycémie du fait de l'absorption très rapide du glucose produit par hydrolyse du saccharose dans l'intestin. Le métabolisme du fructose est quasiment indépendant de l'insuline dont la sécrétion suit la glycémie. L'insuline joue un rôle plus important dans le cas du saccharose étant donné l'élévation rapide de la glycémie. |
||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
C4 - Les
diabètes: des hyperglycémies chroniques aux
sources diverses
|
|||||||||||||||||||||||||||||
|
Une source bien utile qui
complète et met à jour l'article paru dans
l'APBG : dont voici l'adresse sans les frames, tellement
gênantes: http://hometown.aol.com/_ht_a/drfatalis/Pages/diabetes.html
pour laquelle certaines images ne sont pas accessibles
(n'existent pas dans les répertoires
spécifiés)
|
|||||||||||||||||||||||||||||
|
Les diabètes (sucrés) sont des maladies multifactorielles avec une forte composante héréditaire dont le trait commun est une hyperglycémie chronique avec des symptômes pas toujours bien nets (et même parfois inexistants): soif intense, diurèse (quantité d'urine produite et rejetée) importante, perte de poids et trouble de la conscience aboutissant à un coma mortel (définition de l'OMS de 1985 citée approximativement). |
Étant donné
l'unicité du système hypoglycémiant on
peut dire que les diabètes, en tant
qu'hyperglycémie, résultent d'abord d'un
dérèglement du système
hypoglycémiant et donc de la synthèse, de la
libération par les cellules endocrines, du transport,
du mode d'action, ou de la sensibilité des cellules
cibles .... à l'insuline. Ainsi on distingue
deux types principaux (sur
5) de diabètes selon la
quantité d'insuline sécrétée:
|
||||||||||||||||||||||||||||
|
* les diabètes insulino-dépendants (DID) ou de type I pour lesquels la sécrétion d'insuline est très faible ou nulle mais dont le symptôme principal (hyperglycémie) peut être corrigé par des injections d'insuline; |
* les diabètes non insulino-dépendants (DNID) ou de type II qui représentent 90% des diabètes diagnostiqués en France et pour lesquels la sécrétion d'insuline est faible et l'injection d'insuline inefficace à faire baisser la glycémie. |
||||||||||||||||||||||||||||
|
L'hyperglycémie a des conséquences graves: - elle accroît la viscosité sanguine et endommage les vaisseaux (angiopathie touchant d'une part les petits vaisseaux pancréatiques, rénaux ou cardiaques et pouvant conduire à la cécité et d'autre part les gros vaisseaux conduisant à une athérosclérose (3/5 des diabétiques meurent de maladies cardio-vasculaires) - elle perturbe les sécrétions pancréatiques puisque les cellules endocrines pancréatiques (alpha et ß) sont directement sensibles à la glycémie - elle conduit à des modifications chimiques de certaines molécules circulantes comme l'hémoglobine qui fixe le glucose et perd une partie de son activité (elle est glycosylée). Le diabète de type I est assez bien compris. On le considère comme une maladie auto-immune dans laquelle le système immunitaire du malade fabrique des anticorps dirigés contre ses propres cellules ß productrices d'insuline et les détruit totalement en absence de traitement par injection d'insuline (qui peut préserver ainsi une bonne partie des cellules ß). Les mécanismes d'action des anticorps contre les cellules sont assez complexes et variés: certains anticorps sont dirigés contre l'insuline, d'autres contre des éléments membranaires (récepteurs notamment), d'autres encore activent des systèmes lytiques du complément, enfin, les plus toxiques activent des cellules cytotoxiques (mécanisme dit ADCC)... De nombreux gènes, notamment du complexe majeur d'histocompatibilité (CMH), présentent une liaison statistique avec la maladie (la fréquence allèlique (probabilité qu'un individu d'une population présente un allèle; cette fréquence est estimée à partir du % d'individus possédant tel allèle dans une population testée... voir cours de spécialité de TS) est plus forte dans la population diabétique que dans la population standard); on les qualifie souvent de gènes de prédisposition. Aucun cas de causalité directe, avec un déterminisme précis, démontré expérimentalement, n'a été mis en évidence, à ma connaissance. Le diabète de type II est mal compris. Trois éléments principaux semblent caractériser ce type de diabète: - une insulinorésistance des tissus périphériques, particulièrement des tissus musculaires squelettiques (la glycémie reste élevée même lorsque l'on élève l'insulinémie) - une perturbation de la sécrétion d'insuline qui est faible (en absence de traitement) - une synthèse de glucose exagérée. Deux grandes interprétations sont actuellement proposées: l'une privilégiant le rôle des cellules ß et l'autre privilégiant l'insulinorésistance en accord avec les résultats obtenus à partir de modèles animaux (animaux (rats, hamster, souris, lapins) chez qui on cherche à provoquer ou que l'on sélectionne comme présentant des symptômes voisins de la maladie humaine étudiée). On distingue trois phases d'installation d'un diabète de type II: une intolérance au glucose (une glycémie comprise entre 1,10 et 1,26 g.L-1 après 8 heures de jeune), le diabète de type II (si la glycémie à jeun est supérieure à 1,26 g.L-1, ce qui correspond à 25% des cas précédents), et enfin le stade des complications dégénératives avec les atteintes aux vaisseaux (on peut alors être amené à traiter le malade par des injections d'insuline). De nombreux gènes de prédisposition sont étudiés. |
|||||||||||||||||||||||||||||