|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
retour plan du cours de TS, accueil, programme TS 2004, panorama |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Plan |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Bases connues : cours de 1ère S (comparaison système immunitaire / système nerveux ; deux systèmes de relation) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Introduction
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
L'immunologie est la
science de l'immunité |
L'immunité désigne l'ensemble des mécanismes développés par un organisme pour se maintenir en bonne santé. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
« L'immunité est l'ensemble des mécanismes biologiques permettant à un organisme pluricellulaire de maintenir la cohérence des cellules et tissus qui le constituent, et d'assurer son intégrité en éliminant les substances étrangères et les agents infectieux auxquels il est exposé.» (Immunologie, J.P. Revillard, De Boeck Université, 1995) |
L'immunité a donc un double aspect: * l'intégrité de l'organisme (sa cohérence, son fonctionnement intégré; c'est l'immunité au sens plus ancien mais c'est aussi une ouverture sur un sens très actuel de système de communication tourné vers l'intérieur, comme nous le verrons) * et sa défense vis-à-vis des éléments étrangers ou antigènes- éléments susceptibles de déclencher une réponse immunitaire, après reconnaissance par des cellules immunitaires - (immunité au sens plus courant). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le programme nous
demande d'aborder le fonctionnement du système
immunitaire à partir de l'étude d'un
dysfonctionnement: le SIDA (syndrome de déficience
immunitaire acquise), maladie du système immunitaire.
Ce sera la seconde partie. La première sera
formée des bases censées être acquises
en classe de 3ème et que j'ai
préféré traiter déjà en
1èreS. Ces bases sont ici élargies avec des
documents remis en forme à partir de
l'ancien
cours de
terminale.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Les grandes caractéristiques du système immunitaire ont été présentées DE FAçON SIMPLIFIÉE dans le cours de 1ère S. |
Le système
immunitaire est le système de relation
tourné vers l'intérieur. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Ci-dessous la question est davantage détaillée, mais les connaissances de la page simplifiée sont à mon avis suffisantes, même en terminale. Ce qui suit est fourni à titre DOCUMENTAIRE. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1.1
Un système organique comprend des organes et des
cellules
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le système immunitaire comprend trois types d'organes:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Dans la partie ci-dessous nous verrons successivement: les cellules, les organes. Les molécules spécifiques seront traitées dans une autre partie. Il ne s'agit pas d'un
cours mais de documents qui permettent de répondre
aux questions que vous pouvez vous poser.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
En résumé: |
le système immunitaire comprend: |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
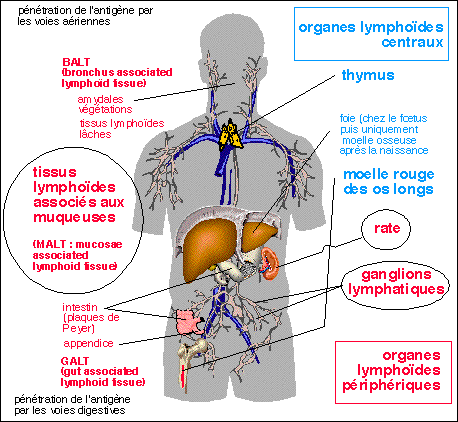
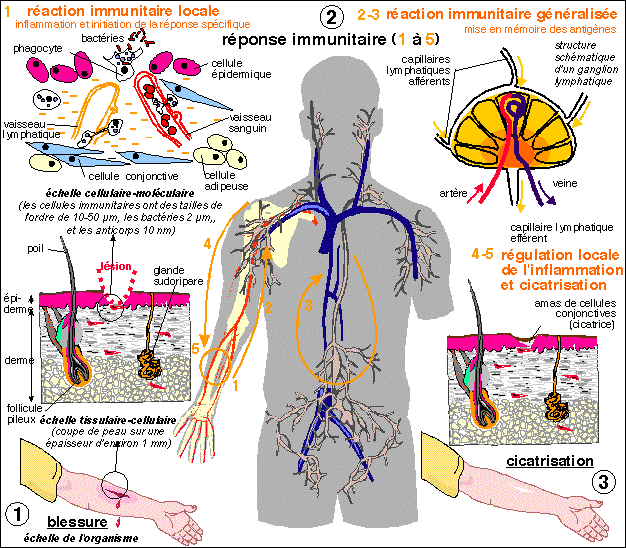
Un schéma de la réponse
immunitaire à une blessure superficielle dont la
principale qualité n'est certes pas la
précision.... l'objectif est de "montrer" la
profonde unité et la coordination de la
réponse immunitaire au niveau local et
général ainsi que le rôle
prépondérant des appareils circulatoires
lymphatiques et sanguins. La réponse est locale, puis
générale, puis de nouveau locale. Les
principales phases sont citées ci-dessous. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
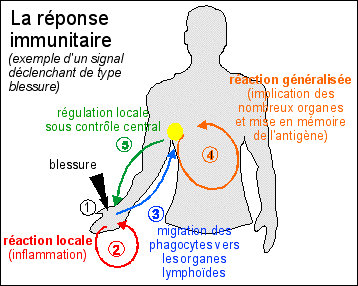
Quelques précisions sur les principales étapes des réponses immunitaires suite à une blessure superficielle : |
1 - inflammation : ensemble de réactions complexes de défenses non spécifiques de l'agent qui les a causées. Trois signes cliniques principaux : rougeur (dilatation des vaisseaux sanguins et donc augmentation du flux sanguin au niveau de la zone lésée), gonflement (souvent se forme un œdème, c'est-à-dire une poche de lymphe interstitielle formée à partir du plasma qui sourd entre les cellules endothéliales des vaisseaux sanguins distendus), chaleur (essentiellement due à l'afflux sanguin mais aussi à la libération de substances pyrogènes : capables de provoquer la fièvre), douleur (c'est l'œdème qui souvent comprime les terminaisons nerveuses du derme, mais il peut y avoir des toxines libérées par les bactéries infectieuses ou des substances libérées par les cellules lésées qui ont le même rôle..),. L'inflammation conduit à une altération de la fonction de l'organe ou du tissu lésé. Les mécanismes de l'inflammation reposent sur la libération de nombreuses substances chimiques qui causent tous ces événements. |
2 - on observe l'arrivée massive de globules blancs dont le rôle est de "capturer" les éventuelles bactéries ayant pénétré lors de la blessure et de nettoyer les tissus lésés en absorbant les cadavres des cellules mortes. Cette intense activité est appelée phagocytose (du grec phagein = manger) et les cellules des phagocytes. Cette phase est le point de départ de la réponse immunitaire spécifique qui va dépendre de l'antigène c'est-à-dire de la substance ou de l'organisme qui a été phagocyté. Un antigène est un élément susceptible de déclencher une réponse immunitaire spécifique. |
3 - les phagocytes qui ont
"capturé" l'antigène vont migrer vers
les ganglions lymphatiques ou les tissus
lymphoïdes les plus proches (ici les ganglions de
l'aisselle) et entrer en communication avec de
nombreuses autres cellules immunitaires du groupe des
lymphocytes. La communication est établie par voie
chimique (médiateurs endocrines, paracrines ou
autocrines: voir cours
de physiologie pour ces termes).
mais aussi par des contacts membranaires facilités
par le gonflement du ganglion au niveau duquel le flux de
lymphe augmente (lors d'une infection les ganglions
lymphatiques deviennent sensibles à la palpation,
parfois douloureuse). C'est ainsi que l'information
immunitaire (nature de l'antigène essentiellement) va
être transmise à tout l'organisme par
l'intermédiaire des cellules qui vont être
entrées en contact les unes avec les autres au niveau
des ganglions ou des tissus lymphoïdes. On assiste
alors à une généralisation de la
réponse immunitaire et à ce que l'on qualifie
de mise en mémoire de l'antigène. Cette
mise en mémoire de la nature antigènique sert
d'explication pour justifier qu'une réponse
immunitaire est souvent plus rapide lors de la seconde
exposition à un antigène, ce qui fonde
l'utilisation de vaccins qui sont des
préparations contenant des antigènes sans
pouvoir pathogène (du grec pathos = souffrir).
La réponse immunitaire elle-même dépend
de l'antigène est peut aller de la
sécrétion de substances neutralisant ou lysant
l'antigène (les anticorps par exemple qui sont des
glycoprotéines sécrétées par
certains lymphocytes) à une action de phagocytose ou
de lyse dirigée et stimulée par d'autres
cellules (la lyse d'une cellule est son
éclatement). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le système immunitaire est le
système de relation tourné vers
l'intérieur ; il est assez lent (utilise le
déplacement des cellules par les liquides internes),
dynamique, en perpétuel remaniement |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Lors d'une blessure accidentelle certains organismes étrangers pénètrent dans l'organisme. La plupart du temps ils sont déjà présents à la surface ou dans l'organisme mais ils changent de milieu et passent d'un milieu surveillé, confiné, à un nouvel espace, où ils ne sont pas les bienvenus. Les mécanismes non spécifiques de défense de l'homme mis en jeu à la suite d'une blessure, ou d'une lésion produite par un agent pathogène, sont regroupés sous le terme de réaction inflammatoire ou plus précisément d'inflammation. Cette réaction de type inflammatoire conduit à l'élimination des éléments étrangers essentiellement par phagocytose. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
L'inflammation est donc une réaction défensive de l'organisme. L'inflammation est non spécifique d'une cause particulière (par exemple un type de microbe), localisée (à une blessure ou à un tissu), et présente 5 caractéristiques : douleur, chaleur (élévation de température), gonflement (œdème) et rougeur, de la région atteinte et altération de la fonction du tissu lésé. Ces signes cliniques sont dus à des événements physiologiques et cellulaires qui sont extrêmement complexes et dont voici juste un aperçu : |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
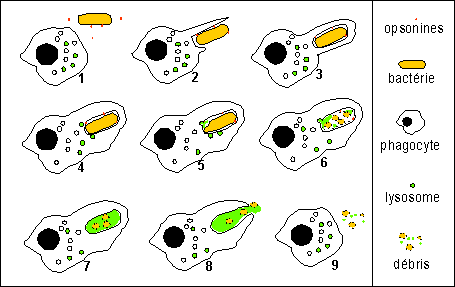
|
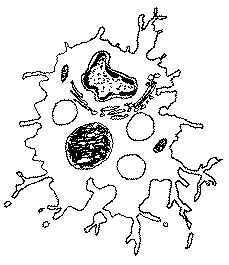
1-chimiotactisme,
déplacement du phagocyte attiré par la
bactérie (Remarque: dans certains cas la bactérie peut résister à la lyse et persister dans le cytoplasme du phagocyte et même s'y diviser et provoquer la mort de celui-ci, c'est alors le point de départ d'une infection) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Conclusion |
Le système immunitaire est de plus en plus considéré comme l'élément essentiel interne, tourné vers l'intérieur, c'est-à-dire vers la défense interne mais aussi le contrôle de toutes les fonctions internes. A chaque fois que l'on s'intéresse aux médiateurs au niveau d'une fonction (le programme nous demande par exemple de traiter la fonction reproductrice), on retrouve les médiateurs immunitaires. Le système immunitaire, au sens le plus large, comprenant des organes, des cellules et surtout le MILIEU INTÉRIEUR, semble être un bon candidat pour remplacer la notion de système endocrine.Il y a encore certainement beaucoup de travail à faire mais on peut déjà comprendre comment les relations entre populations cellulaires, au cours de l'embryogenèse, comme plus tard chez l'organisme adulte, passent par des mécanismes que l'on a souvent considéré comme faisant partie d'un système de défense mais que l'on pourrait voir comme un système de contrôle, d'intégration, réalisé par des médiateurs mais aussi par des contacts cellulaires. La fonction endocrine ne serait plus qu'un des aspects de la communication entre cellules réalisée notamment à l'aide des médiateurs. De la même façon que pour le
système nerveux (voir
cours de
1èreS),
on peut donc dire que : |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Sans avoir la prétention de faire un quelconque tour des aspects moléculaires du système immunitaires, tout à fait hors de portée de l'enseignant de SVT - surtout du fait de l'hégémonie de la biologie moléculaire dans la recherche - on peut essayer de faire un petit effort de synthèse pour présenter les éléments nécessaires à la compréhension des mécanismes immunitaires au niveau moléculaire, tout en insistant sur le fait que cette approche n'est probablement pas la plus pertinente à ce niveau d'enseignement. Les molécules du système immunitaire sont:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Les molécules membranaires de quelques cellules immunitaires |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
+ monocyte / macrophage |
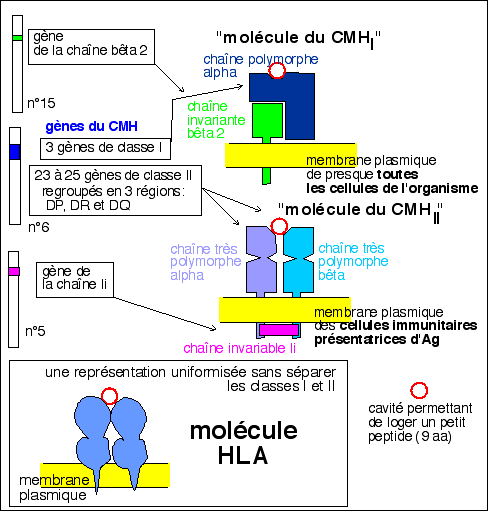
molécules du système HLA de classe I et II certaines lignées expriment aussi (avec une faible densité) les molécules CD4 |
schéma d'une molécule du
système HLA |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
CD = classe de différenciation = cluster of différenciation |
Ce nom à tout d'abord
désigné des types d'Ac (1, 2, 3...) qui
reconnaissent spécifiquement des marqueurs
membranaires des leucocytes : les CD4 étaient donc
des Ac qui reconnaissaient un même type (n°4) de
molécules membranaires.
Maintenant on donne le nom CD à la molécule
membranaire reconnue et l'Ac est désigné par
antiCD. voir par exemple un site (en anglais) répertoriant les différentes molécules en fonction de leur CD: http://www.sciencegateway.org/ resources/ prow/index.html Nous n'utiliserons les molécules CD que si c'est absolument nécessaire à la compréhension des spécificité d'une lignée cellulaire. Nous ne donnerons pas de schéma de la structure de ces diverses molécules. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
+ lymphocyte / plasmocyte |
Très complexe. Dans le secondaire (et jusque dans le programme) on a pris plusieurs mauvaises habitudes: 1 - celle de les scinder uniquement en
deux catégories: 2 - celle de considérer, abusivement, que les lymphocytes porteurs de marqueurs CD4+ sont LES lymphocytes auxiliaires (helpers), ce qui n'est pas du tout absolu; 3 - celle de considérer en conséquence que les lymphocytes T possédant les marqueurs CD8+ sont des lymphocytes cytotoxiques; ce qui et faux, d'autant plus qu'ils ne sont pas les seuls à les posséder... DONC : certains lymphocytes cytotoxiques portent les marqueurs CD4+ et les lymphocytes sécréteurs de cytokines qualifiés d'auxiliaires peuvent aussi posséder les marqueurs CD8+...(voir par exemple Immunologie de Revillard p 102 et ch 6-2 et 6-3 p 65 et s) Dans l'état actuel de nos connaissances (et surtout des miennes, c'est-à-dire de ce que j'ai pu comprendre sur ces marqueurs), il est peu prudent de qualifier une population cellulaire uniquement par ses marqueurs membranaires. Ce qui est justifiable en recherche, ne l'est pas quand on veut faire une synthèse à destination des élèves du secondaire. |
Actuellement les seuls marqueurs spécifiques de la lignée T sont les récepteurs des lymphocytes T (TCR = T cell receptor) et les complexes moléculaires CD3 (voir ci-dessus) schéma d'un récepteur
T |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Pour la lignée B les récepteurs (BCR = B cell receptors) sont des immunoglobulines (Ig) de même nature que les anticorps solubles (Ac), avec en plus, cependant, une chaîne lourde traversant la membrane et constituée d'une vingtaine d'aa hydrophobes et une très courte région cytoplasmique. Les chaînes de ces Ig pouvant provenir de différents groupes (M, D, G....), on leur adjoint le préfixe "m" on a ainsi des mIgM, mIgD, mIgG... schéma de la structure d'un
Ac |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
+ non spécifiques |
presque toute cellule de l'organisme infectée par un virus ou par un parasite intracellulaire (bactérie ou protiste) mais surtout les cellules épithéliales et endothéliales molécules du système HLA de classe I |
schéma d'une
molécule du système HLA |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
* majeur s'oppose à mineur. En effet ils existe d'autres systèmes d'histocompatibilité, qualifiés de mineurs. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Remarque importante : Une
difficulté de vocabulaire bien lourde à
traîner : le terme de
CMH
désigne un groupe de
gènes. Les
antigènes (molécules marqueurs de surface des
cellules) sont donc des produits du
CMH. MAIS CE NE SONT PAS LES SEULS. Il
devrait donc être interdit de parler des
molécules du CMH pour désigner les
seuls produits antigéniques de surface; par contre il
est très fréquent de parler des
molécules HLA, ce qui est
pourtant tout autant un abus de langage.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Découverte :
|
Gènes et produits :
Leurs produits ne sont donc pas tous des molécules intervenant dans la seule immunité...Le nombre de gènes connus est voisin de 30 (d'où le terme de multigènique). Pour chaque gène connu la liste des allèles détectés par des méthodes utilisant les sérums ne cesse de croître. Elle peut aller d'une dizaine à plusieurs dizaines d'allèles (famille multiallélique). Cette variabilité est qualifiée de polymorphisme : on recense plus de 1010 combinaisons allélique possibles chez un individu. Il existe d'autre part des mécanismes originaux de conversion génique par échange de séquence d'ADN entre gènes qui ont été mises en évidence lors de la maturation de certaines cellules...Bref tout cela est fort complexe. Déterminer les différents allèles pour les systèmes d'histocompatibilté s'appelle faire un groupage ou typage ABO ou HLA par exemple. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Les molécules HLA, antigènes
membranaires
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Antigènes :
|
Cellules :
Un autre groupe (classe II) est formé de molécules HLA dont la présence est strictement limitée à certaines cellules de l'organisme intervenant dans l'immunité (105 molécules par cellule par exemple pour les lymphocytes , les phagocytes, les cellules de l'épithélium (tissu de revêtement) intestinal ou encore de l'épithélium respiratoire. Cette répartition prouve clairement que les molécules HLA ne peuvent pas être considérées comme des déterminants exclusifs du soi, compris comme identité biologique (ni de l'identité moléculaire d'ailleurs). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Gènes :
Il existe un déséquilibre de liaison spécifique à certaines populations. En effet, on observe des différences entre groupes ethniques, certains allèles se retrouvent plus fortement associés dans certaines populations que ne le voudrait une distribution aléatoire.... C'est encore une preuve de la manipulation des gènes par la cellule et du fait que l'on travaille toujours sur une interprétation chromosomique de la liaison de tel ou tel caractère... |
Rôles : Les molécules HLA du premier groupe (classe I) sont supposées être responsables de la présentation des peptides (9 aa) issus de la dégradation permanente par chaque cellule de ses propres protéines (protéines endogènes). La cellule présenterait ainsi en surface en permanence des fragments des protéines qu'elle synthétise. Ces protéines seraient bien sûr modifiées dans le cas d'une infection virale, la cellule synthétisant alors les protéines virales. Les molécules HLA du second groupe (classe II) sont supposées présenter des peptides (9 aa) qui sont issus du milieu extérieur, ont été absorbés par la cellule (endocytose) puis dégradés. Il semblerait qu'il existe un seuil
à partir duquel la présentation des peptides
provoque une réaction immunitaire. Il serait
d'environ de 200 molécules HLA associées au
même peptide. La plupart des peptides
présentés par les molécules HLA sont
des fragments de ces mêmes molécules HLA. De
nombreuses séquences de peptides sont identiques
(homologues) à celles de peptides de
micro-organismes. Enfin, si le nombre théorique de
peptides possible est de 5.1011 (9 aa parmi 20
aa) , il semble que le nombre réel est beaucoup plus
restreint du fait de leur aptitude ou non à
établir des liaisons avec les molécules HLA
(essentiellement par 2 aa de la cavité des
molécules HLA).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Remarque : les modèles présentés ne sont pas très approximatifs... en effet, certaines chaînes glycoprotéiques, fortement globulaires, semblent avoir plusieurs domaines possédant chacun une partie intramembranaire et une partie cytoplasmique, ce qui rend la représentation dans l'espace très difficile... |
Remarque: les molécules du CMH (sans faire de distinction de classe) ou molécules HLA sont donc présentées en terminale comme des marqueurs du soi qui sont modifiés (soi modifié) par la présentation de déterminants antigéniques. A un sujet du type: "vous présenterez la notion de soi biologique et le rôle de ses marqueurs dans la réponse immunitaire" il faudrait traiter, sans hésitation, les "molécules du CMH" (différenciées ou non) et leur rôle dans la réponse immunitaire. Un antigène (Ag) est une molécule déclenchant pas sa structure une réaction immunitaire (reconnaissance par les cellules immunitaires et réponse immunitaire spécifique - voir plus loin). Un déterminant antigénique désigne plus précisément le fragment de l'antigène qui a le rôle antigénique. Remarque: Lorsque l'on parle de "présentation des déterminants antigéniques en association avec le soi (les molécules du CMH)" on fait ce me semble deux erreurs: les petits peptides présentés avec les "molécules du CMH" ne sont pas des antigènes s'ils ne déclenchent pas de réaction immunitaire. Et ensuite les "molécules du CMH" ne sont pas des marqueurs du soi (ni même du soi génétique), mais par contre les petits peptides le sont en quelque sorte. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Quelques marqueurs membranaires des cellules immunitaires... |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
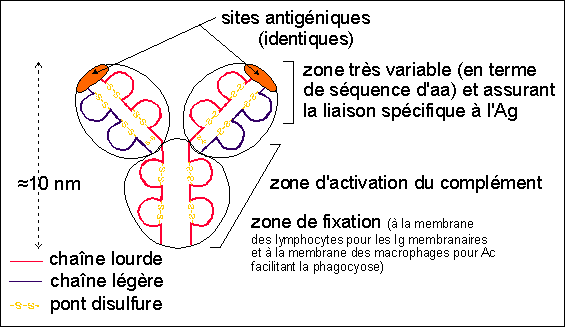
|
Un schéma d'une immunoglobuline (Ig) ou
anticorps (Ac)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
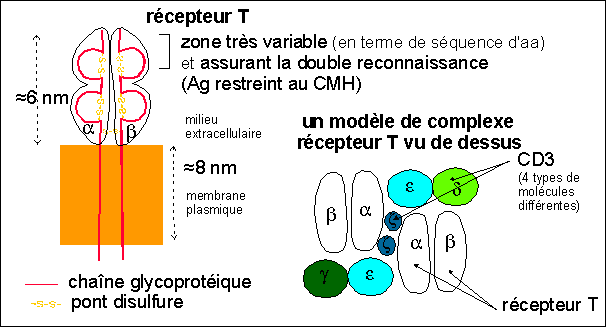
Un exemple de récepteurs membranaires des
lymphocytes T (rT)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Ce sont des protéines, le plus souvent glycolsylées ou glycoprotéines (possédant des glucides), sécrétées sous l'action d'un signal activateur (et non à un certain taux par des cellules toujours actives, même si leur activité est modulée par des paramètres physiologiques, comme le sont les hormones) par de nombreux types cellulaires (et non un seul type de cellule endocrine comme pour les hormones) et qui agissent sur des cellules-cibles pourvues de récepteurs spécifiques (comme pour les hormones). |
Cet ensemble de molécules est très hétérogène et regroupe :
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le complément |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le complément est un ensemble de plus d'une trentaine de protéines sériques (�5% de l'ensemble des protéines sériques) et membranaires (récepteurs et protéines régulatrices) qui jouent des rôles variés dans la réponse immunitaire non spécifique et spécifique à médiation humorale. |
Les protéines du complément sont essentiellement sécrétées par les cellules du foie, les cellules épithéliales intestinales et dans les monocytes et les macrophages. La demi-vie (temps nécessaire pour renouveler la moitié d'une quantité de protéine donnée) de certains éléments a été estimée à environ 24 heures, ce qui suggère que le complément est sécrété et utilisé en permanence. Certains gènes codant pour certaines fractions du complément appartiennent au CMH (chromosome 6, voir plus haut), d'autres sont situées sur des chromosomes variés (1, 5, 9, 11, 12, 19, X...) ; l'étude des fonctions des différentes fractions a surtout été réalisée à partir de malades présentant des déficits congénitaux en telle ou telle fraction. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
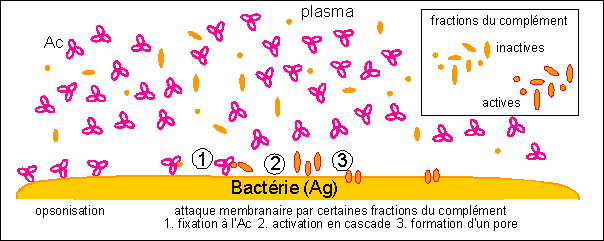
Les protéines du complément sont normalement sécrétées sous une forme inactive mais peuvent être activées soit par fixation aux Ac formant un complexe Ac-Ag (voie dite classique ou spécifique), soit après contact avec des particules ou des membranes (complexes immuns, toxines, virus, bactéries, parasites, cellules eucaryotes ... : voie alterne ou non spécifique). Se déroule alors une activation en cascade où chaque fraction du complément, une fois activée (souvent par coupure enzymatique de la molécule en deux sous-unités actives enzymatiquement), active à son tour une autre fraction,...et ainsi de suite. |
La voie classique d'activation du
complément par fixation d'une fraction à l'Ac
lui-même fixé sur une Ag (phase de
reconnaissance) puis activation en cascade des
différentes fractions (toutes les fractions ne sont
pas activées à chaque fois...).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Les protéines du complément peuvent se classer, selon leur rôle, en :
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Deux rôles essentiels des Ac : |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Ainsi les opsonines dont nous
avons parlé lors de la phagocytose sont des
éléments qui se fixent sur l'Ag et favorisent
la phagocytose. On a donc deux grand groupes de
molécules opsonisantes : |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Remarque: |
Le complément n'est pas au programme en tant que tel et il ne doit être envisagé que comme un élément associé aux Ac. Cependant, d'un point de vue plus général, il me semble intéressant de préciser quels sont les éléments plasmatiques participants à la défense de l'organisme : le complément ne représentant que 5% des protéines plasmatiques. Les trois autres systèmes reconnus sont : les systèmes de coagulation (composé de protéines dont la principale est le fibrinogène, associé aux plaquettes pour former le caillot), le système de contact (ensemble de protéines, parmi lesquelles on peut citer le facteur Hageman, qui interviennent dans l'inflammation notamment) et le système de la fibrinolyse (qui permet la destruction d'un caillot sanguin). Tous ces systèmes de protéines plasmatiques sont bien sûrs reliés entre eux et coordonnés. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||