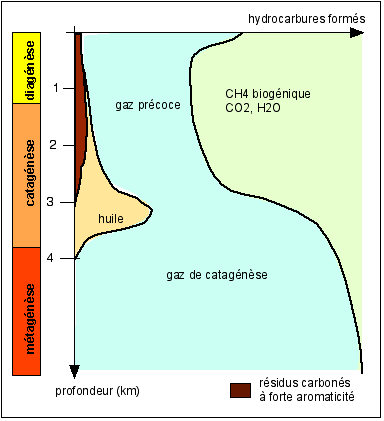
Un diagramme qualitatif montrant la genèse des hydrocarbures en fonction de la profondeur
(en supposant un gradient géothermique moyen). (d'après Enseigner la géologie, Nathan, p 193)
Sommaire de cette page:
roches non combustibles / /
roches combustibles / / l'eau,
une ressource du sous-sol / / la
géothermie / / le génie
civil
Le sous-sol est un thème qui peut être abordé en cycle 1 et surtout en cycle 2 (voir formulations sur les roches) car c'est la première approche de la notion de roche pour l'enfant. Sans faire l'objet d'une étude détaillée (notamment didactique), n'étant pas au programme du cycle 3, cette partie peut néanmoins faire l'objet d'une question au concours (CRPE). Voici donc quelques éléments de base (deux ouvrages de référence : Enseigner la géologie (collège-lycée), Nathan, 1992 et Géologie, objets et méthodes, Jean Dercourt et Jacques Paquet, Dunod, 1990)
Du point de vue disciplinaire, si la géologie est une science expérimentale qui a pour but la connaissance de la terre, la géologie appliquée met les connaissances géologiques au service de l'homme: ingénieur, artisan, commerçant, artiste, militaire, amateur de pierres précieuses...
* les matériaux de construction et autres
matières utilisées par les artisans et artistes
Selon l'usage (habitations, monuments, routes...) on
privilégie certaines caractéristiques
(résistance à l'écrasement, au gel, à la
cassure..., masse...). On exploite ainsi des roches meubles (sables,
loess, limons, argiles, graviers, lapilli...) ou cohérentes
(calcaires, granites, basaltes...).
Les matériaux modernes sont de plus en plus des
matériaux artificiels c'est-à-dire
élaborés par l'homme qui modifie les matériaux
naturels.
Ainsi le produit le plus utilisé par l'homme après
l'eau n'est pas une roche naturelle mais une "roche" artificielle: le
béton. C'est une roche au sens mécanique,
minéralogique du terme mais pas en ce qui concerne sa
genèse bien sûr. On fabrique le béton moderne
à partir d'un mélange de ciment, de sable, de graviers
et d'eau. Le ciment est une poudre obtenue en
mélangeant du gypse (CaSO4,2H2O) au produit de la
calcination (1500°C) d'un mélange de calcaire (80%) et
d'argile (20%) auquel on ajoute de silice, de l'alumine et de
l'oxyde de fer pour une faible part. Le ciment cristallise
réellement (lorsqu'il est appliqué contre du calcaire,
les cristaux du tobermorite: 3CaO,2SiO2,3H2O, principal
minéral du ciment cristallisé, croissent dans le
prolongement du réseau cristallin de la calcite). Le
béton très peu poreux est peu sensible au gel mais il
vieillit cependant.
Le gypse chauffé entre 100 et 140°C se transforme (perte
d'eau) en plâtre qui recristallise après
mélange avec de l'eau.
Le mélange calcaire-argile ne donne pas seulement le
ciment mais aussi, notamment avec du loess
(sédiment éolien périglaciaire contenant de
l'argile et du calcaire...), les briques,
tuiles, poteries, grès et
cérames (grès vitrifiés).
Faïences et porcelaines sont
fabriquées à partir de mélanges kaolinite
(argile blanche alumineuse très fine)-feldspath.
Le verre enfin résulte de la fonte de sable
siliceux puis de son refroidissement très rapide (trempe ou
vitrification).
La toute jeune (fin du XIXème siècle) science des matériaux (si l'on oppose, de façon certainement indue, science et technique ainsi que science et pratique (ars)...) tente d'unifier l'étude de tous les matériaux, tant naturels (pétrologiques ou biologiques...) qu'artificiels, à l'aide d'une analyse structurale physique et chimique. La manière la plus moderne de classer les matériaux consiste à examiner les mécanismes qui lient entre eux les atomes ou les molécules; on distingue cinq types principaux de liaison: liaison ionique, liaison covalente, liaison métallique, liaison moléculaire ou de Van der Waals et liaison hydrogène. De façon plus classique, on distingue aussi:
* les matières premières de l'industrie
chimique
Le pétrole et les charbons sont bien sûr utilisés
comme produits de base d'une industrie chimique (pétrolochimie
et carbochimie) qui fabrique des innombrables matières
"plastiques" et autres caoutchouc synthétiques.
L'acide sulfurique est ensuite le plus utilisé des acides
minéraux de l'industrie (allumettes, pharmacie, caoutchouc,
papier, pharmacie...); il est élaboré à partir
de soufre trouvé à l'état natif
(déposé par des fumerolles volcaniques ou
associé à l'hydrothermalisme ou encore aux
hydrocarbures) ou fabriqué à partir de la pyrite
(sulfure de fer: FeS2).
Les roches salines (sel (halite, NaCl), la sylvinite (KCl) et
phosphates) sont exploitées à partir de
dépôts anciens: gisement de sel lorrain par exemple,
gisement de sylvinite d'Alsace ou phosphates d'Afrique du Nord.
* les minerais:
Classiquement, on appelle minerai une substance naturelle
de laquelle il est possible d'extraire un
métal d'une façon rentable
économiquement. La qualification en minerai et non minerai
fluctue donc avec le marché mondial des métaux.
L'argile n'est pas un minerai d'aluminium alors que la bauxite, moins
riche en aluminium que l'argile, en est un. C'est un problème
de coût d'extraction. On retraite aussi actuellement des
résidus de l'extraction d'uranium car les techniques ont
évolué et il est devenu rentable de traiter ce qui
était auparavant un rebut.
Plus récemment, on tend à appeler
minerai tout matériau naturel
(pétrologique) à valeur économique (on
supprime la référence aux métaux, ce qui permet
d'y inclure les minéraux en général...).
La science de la genèse des gîtes métallifères est la métallogénie. Du point de vue géologique les gisements des minerais dépendent bien sûr du type de minerai: natif, sel, oxyde, carbonate... mais aussi des processus qui lui ont donné naissance; on trouve ainsi :
Un métal est un corps simple
caractérisé par un éclat particulier
(éclat métallique), conducteur de chaleur et
d'électricité.
Les métaux natifs exploités sont l'or, le platine et
plus rarement le cuivre, l'argent et le mercure.
De nombreux métaux sont extraits à partir de sels: les
sulfures sont des minerais fréquents de cuivre, plomb, zinc,
mercure, molybdène...; les chlorures sont aussi courants.
La plupart des minerais sont des oxydes ou des hydroxydes. Par
exemple les oxydes de fer (limonite, hématite,
goethite...), ou d'aluminium comme les bauxites (complexes de
kaolinite (argile=silicate d'alumine hydraté) et d'hydrates
d'alumine (gibbsite...)). L'uranium est extrait de la
pechblende, une forme impure de l'uraninite: l'oxyde
d'uranium: U2O.
Le diamant naturel (carbone cristallisé (avec uniquement des liaisons de covalence) dans le système cubique avec un atome central entouré de quatre autres atomes, sommets d'un tétraèdre) cristallise dans des roches très particulières comme les kimberlites (roches des cheminées volcaniques de Kimberley en Afrique du Sud ) qui contiennent des éclogites issues du manteau dans lesquelles on trouve ces diamants. La masse d'un diamant est donnée en carat (5 carats = 1 gramme ; 1 carat = 0,2 gramme); le plus gros diamant naturel connu fût trouvé en 1905: le Cullinan (du nom d'une mine d'Afrique du Sud) de 3106 carats (taillé en 105 pierres dont l'étoile d'Afrique (130,2 carats) et deux pierres de 530 carats et 317 carats exposées avec les bijoux de la couronne à Londres (le plus gros ornerait de sceptre britannique ... j'ai à ce sujet des sources divergentes...?)).
Les roches carbonées (qui contiennent du carbone mais aussi de l'hydrogène) brûlent au contact de l'air ce qui en fait des roches "énergétiques" (terme anthropomorphique). L'énergie calorifique dégagée lors de la combustion est non renouvelable et ces roches étant issues de processus très longs de diagénèse, on parle aussi d'énergie fossile, produite par la combustion de ces roches, même si, actuellement, des processus conduisant à la formation de telles roches carbonées sont sans aucun doute à l'œuvre. L'énergie emmagasinée par ces roches est une énergie chimique de liaison (liaisons covalentes C-C principalement) et une énergie chimique d'oxydo-réduction (la matière organique des roches carbonées est fortement réduite). Cette énergie chimique vient d'une part de la matière organique initiale qui s'est enfouie dans les sédiments: on peut donc la qualifier alors d'énergie solaire fossile car en fait toute énergie contenue dans la matière organique est issue de l'énergie solaire convertie en énergie chimique par les producteurs primaires (organismes photosynthétiques) puis transférée successivement aux différents membres des réseaux trophiques avec des pertes calorifiques à chaque niveau trophique (voir cours sur la nutrition). Cependant l'énergie des roches carbonées vient aussi (et surtout) des processus de maturation qui sont intervenus après l'enfouissement qui transforment une matière organique peu réduite (le terme de kérogène désigne la matière organique en cours de transformation après son enfouissement) en matière organique très réduite (et donc à haut pouvoir calorifique). Ces mécanismes comprennent dans les premiers mètres (on parle de diagénèse précoce) des transformations dues aux bactéries qui oxydent une bonne part de la matière organique. Contrairement donc à une idée persistante, les bactéries ne sont pas du tout les principales responsables de la formation des roches carbonées, même si elles y participent incontestablement. En effet, la principale transformation, qualifiée de diagénèse thermique, est due à l'augmentation de la température (et secondairement de la pression), elle-même due à l'enfouissement. C'est elle qui, par des réactions thermo-catalytiques conduit à une perte d'azote et surtout d'oxygène (CO2 et H2O) ce qui est une réduction. Plus bas encore (entre 1,5 à 4 km de profondeur) la matière carbonée très réduite subit un craquage thermique (catagénèse), aboutissant à une séparation entre une phase fluide (huiles et gaz MOBILES: on parle de fenêtre à huile pour désigner ce domaine de pression-température car c'est à cette étape que l'on observe des migrations et donc des accumulations) et en phase solide: qui sont des résidus carbonés (avec une grande quantité de résidus aromatiques). Des stages ultimes (métagénèse) peuvent conduire, au-delà de 4 km de profondeur à du graphite cristallin et à une libération de méthane (CH4).

Dans les stades précoces de diagénèse et de la catagénèse, ce qui permet de retrouver l'origine d'un produit organique combustible est sa signature géochimique représentée par différents marqueurs: les porphyrines dérivées de la chlorophylle, les géo-hopanoïdes, marqueurs de la paroi bactérienne. Dans le diagramme ci-dessous on utilise 2 marqueurs: le rapport atomique H/C et le rapport atomique O/C:
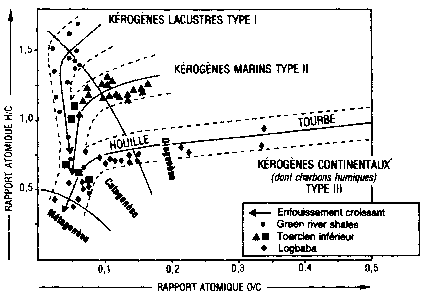
Diagramme de Van Krevelen: on distingue 3 grands types de
kérogènes avant la maturation où plus aucune
distinction n'est possible:
* kérogènes lacustres de nature alguaire,
pauvres en oxygène et riches en hydrogène
* kérogènes d'origine planctonique marine
(contenant notamment certaines algues comme les
tasmanacées...)
* kérogènes continentaux issus de la
décomposition de tissus végétaux
supérieurs (pauvres en H et riches en O) avec des spores,
des cuticules, des algues...
Il est important de ne pas associer trop vite un produit avec une
origine organique: certains charbons donnent des gaz naturels et on
cherche actuellement à prouver actuellement qu'ils peuvent
aussi donner des pétroles.
Le terme charbons (du latin carbona = charbon)
désigne des roches sédimentaires stratifiées,
combustibles, de couleur sombre, formées principalement de
débris végétaux. On distingue plus
précisément (voir Dictionnaire de
géologie , Masson, pour d'autres termes):
Les pétroles (du grec petrelaion = huile de
pierre) sont des hydrocarbures comportant
* des carbures saturés (paraffiniques) de formule Cn
H2n+2 (5�n�15, les bitumes correspondent à des carbures
saturés de même formule avec n>15, mais la
terminologie est fort complexe et les produits nombreux), liquides
à 20°C et de teinte d'autant plus sombre qu'ils sont
denses (0,83 à 0,96; de toute façon plus légers
que l'eau)
* et des hydrocarbures cycliques naphténiques de
formule Cn H2n-3
* et plus rarement des hydrocarbures cyclique aromatiques de
formule Cn H2n-6.
Le gaz naturel est un mélange de carbures saturés de formule Cn H2n+2 avec n<5 : méthane(1), éthane(2), propane(3), butane(4); dans les gisements ils peuvent être sous forme gazeuse (méthane et éthane) ou liquide (propane, butane) et coexistent ou non avec des pétroles ou des charbons.
La genèse de de kérogène en grande quantité dépend d'une part de la quantité d'apport de matière organique (plus la productivité est importante, plus on aura des chances de trouver une accumulation) et d'autre part des conditions de son enfouissement en milieu réducteur, à l'abri de l'oxygène (aussi bien en milieu marin profond où l'oxygène est renouvelé très lentement, malgré la faible productivité, que sous une faible couche d'eau (stable) d'une lagune marécageuse où l'oxygène n'est pas renouvelé assez vite pour l'énorme quantité de matière organique produite à oxyder).
Malgré la complexité des phénomènes,
si l'on tient absolument à relier la formation des roches
carbonées à leur contexte géodynamique, il me
paraît suffisant de savoir qu'en fonction de ce qui a
été dit au-dessus:
* dans le cas d'un gisement de charbon, on a toutes les chances que
le produit soit en place; on peut donc déduire de
l'étude du contexte géodynamique local les conditions
de formation du dépôt
* alors que dans le cas des gaz et pétroles, les produits sont
le plus souvent dans une roche réservoir (magasin),
poreuse ou fracturée, et il est parfois plus difficile de
trouver les roches mères au sein desquelles ils ont
pris naissance.
* les principaux contextes géologiques favorables
(paléomilieux) sont les suivants: lacs et marécages
d'un bassin intracontinental, lacs et marécages de bassins
d'effondrement (mer du Nord, bassins à la limite de marges
passives comme le bassin du Congo...), lagunes ou grands deltas
(Nigéria, Bornéo...), bassins orogéniques
(associés à la formation d'une chaîne de
montagne, comme par exemple le bassin de Vienne lié à
l'orogénèse alpine)...
A noter une petite expérience toute simple: fabriquer en classe des hydrocarbures...
(chapitre à part du fait de son importance: voir hydrogéologie).
La géothermie s'intéresse globalement au régime thermique du globe terrestre. En géologie appliquée elle s'attache à maîtriser l'exploitation de la capacité calorifique du sous-sol . Elle extrait cette énergie soit des roches directement (géothermie "sèche" pour laquelle on injecte des fluides pour récupérer l'énergie calorifique) soit des eaux chaudes circulantes dans le sous-sol (géothermie de sources et nappes chaudes). On distingue classiquement une géothermie basse énergie si les fluides impliqués (naturels ou injectés) atteignent 50 à 90°C et une géothermie haute énergie pour des températures de 150-300°C.
Deux éléments sont à prendre en compte:
* la température du sous-sol augmente avec la profondeur:
c'est le gradient géothermique.
* le contexte géodynamique: dans une croûte continentale
stable le gradient géothermique est de quelques degrés
Celsius par kilomètres alors que dans une zone
d'accrétion océanique ou dans une zone volcanique
insulaire ou continentale on peut atteindre 100°C par
kilomètre.
Si on ramène à la surface de la France, le calcul du
flux de chaleur par unité de surface (qui varie de quelques
dizaines à quelques centaines de milliwatts par mètre
carré) , on obtient un équivalent de 20 millions de
tonnes équivalent pétrole (tep) par an. On estime la
puissance géothermique de la Terre à 30 milliards de
kilowatts. Cependant la géothermie garde une place modeste
dans le bilan énergétique mondial (quelques fractions
de pour cent) du fait de l'inaccessibilité de la
ressource.
La géothermie sèche consiste à injecter un fluide froid dans un réseau fracturé de roches chaudes. On peut accélérer la fracturation en injectant le liquide sous pression. Ce type de géothermie est encore expérimental et est principalement limité aux zones à fort gradient géothermique.
La géothermie utilisant des eaux profondes chaudes
présente deux formes habituelles:
* les sources chaudes dont les plus spectaculaires sont les
sources chaudes à jaillissement intermittent (les geysers). Le
principe en est simple: des eaux météoriques
s'infiltrent en profondeur le long de fractures jusqu'à un
aquifère profond dont la température des fluides peut
atteindre 250 °C (la phase liquide est maintenue du fait de la
pression). La densité d'une telle eau chaude atteint 0,8 ce
qui la pousse à remonter. Au cours de l'ascension le long des
fractures, la pression diminuant, la phase gazeuse à tendance
à apparaître (ébullition) ce qui provoque le
jaillissement du geyser, le gaz poussant violemment à l'air
libre une petite colonne d'eau liquide. Le système est
auto-entretenu tant que les nappes sont approvisionnées.
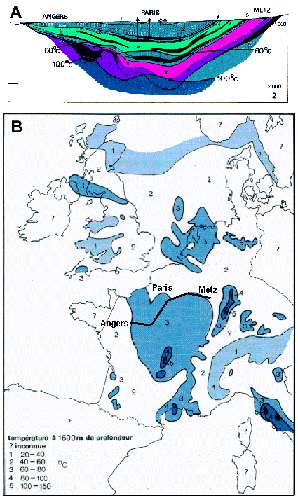
* les nappes phréatiques chaudes peuvent aussi
être exploitées par des forages comme les nappes du
Bassin Parisien présentées ci-dessous. L'eau chaude,
une fois utilisée pour alimenter des pompes à chaleur,
devrait être réinjectée pour éviter de
trop modifier les équilibres naturels (tant thermiques que
géochimiques).
Les grands ouvrages de génie civil mettent en jeu les connaissances de géologie et font donc partie de la géologie appliquée. Le terme génie civil est pris ici dans son acception la plus récente et désigne tous les ouvrages de constructions de grande ampleur (bâtiments, ponts, jetées, réservoirs, chaussées...) réalisée pour la société civile, quelqu'en soit la destination (usage civil ou militaire...). Une étude géologique préalable à tout ouvrage de génie civil, toute souhaitable qu'elle soit, est pourtant rarement entreprise, d'autant qu'elle ne garantie pas la sécurité de l'ouvrage. L'ingénieur voudrait des certitudes (résistance, étanchéité d'une couche, ...) que le géologue ne peut fournir. On parle d'ailleurs le plus souvent d'une étude des risques et de faisabilité plutôt que d'une expertise géologique, puisque si la géologie appliquée ne peut être une science exacte (non du fait de ses concepts mais dans ses prévisions).
Des exemples de grands ouvrages d'art (ponts, tunnel sous la manche, métropolitain...) ont été traités en cours de SVT dans cette optique dans les programmes du secondaire (1ère S, 1ère L et ES) mais sont actuellement abandonnés.